O diagnóstico diferencial entre o aneurisma e o pseudoaneurisma ventricular, embora difícil, é fundamental face às implicações terapêutica e prognóstica. O presente caso clínico realça o papel fulcral das técnicas de imagem não invasivas no diagnóstico diferencial destas entidades, possibilitando uma correta orientação dos doentes.
Distinguishing between ventricular aneurysm and pseudoaneurysm, although difficult, is of major importance due to the therapeutic and prognostic implications. The present case highlights the pivotal role of non-invasive imaging modalities for differential diagnosis between these entities in order to ensure appropriate management of these patients.
Com o advento da revascularização miocárdica precoce, observou-se um decréscimo na incidência das complicações mecânicas relacionadas com o enfarte agudo do miocárdio (EAM). Contudo, a rotura da parede livre do ventrículo esquerdo (VE), uma das mais temíveis complicações, pode ocorrer em 4% dos EAM, sendo responsável por cerca de até um quarto das mortes relacionadas com o evento isquémico1. Raramente, a rotura é contida pelo pericárdio aderente, originando uma cavidade delineada por tecido fibroso, na ausência de fibras musculares, é designada de pseudoaneurisma. Atendendo à sua composição, é grande o risco de rotura, ditando a necessidade de correção cirúrgica urgente. Face às implicações prognósticas e terapêuticas, o seu diagnóstico correto e atempado é fundamental. Contudo, a forma de apresentação clínica, os achados do exame objetivo, as alterações no Rx de tórax ou no eletrocardiograma (ECG) não são sensíveis ou específicos dos pseudoaneurismas ventriculares, nem permitem o diagnóstico diferencial com os verdadeiros aneurismas, que constituem complicações mais frequentes dos EAM. O presente caso clínico ilustra estas dificuldades diagnósticas e realça o contributo complementar das técnicas de imagem na identificação desta entidade3.
Caso clínicoOs autores descrevem o caso de um homem caucasiano de 72 anos, ex-fumador, com história prévia de prostatectomia transuretral e de doença cerebrovascular. De realçar que não estava a fazer qualquer tipo de medicação cardiovascular. Em fevereiro de 2009, sofreu dor torácica constritiva, prolongada, com irradiação dorsal e acompanhada de vómitos, mas não procurou cuidados médicos. Desde então, iniciou clínica de insuficiência cardíaca, com dispneia para esforços progressivamente menores, sem recidiva de dor torácica. Por agravamento dos sintomas, recorreu cerca de um mês depois ao serviço de urgência do nosso hospital, onde deu entrada em classe iv da New York Heart Association (NYHA). O ECG da admissão documentou sinais de EAM anterior não recente, não se tendo verificado subida dos marcadores de necrose miocárdica. A avaliação ecocardiográfica revelou disfunção sistólica severa do VE, com aneurisma apical (fig. 1), denso auto-contraste e trombo séssil, motivo pelo qual foi iniciada hipocoagulação oral.
Por suspeita de tuberculose pulmonar e franca deterioração do estado geral, foi decidida estratificação não invasiva inicial. O doente prosseguiu estudo no internamento da Medicina Interna, não tendo sido identificado agente microbiológico nas secreções brônquicas, suco gástrico ou hemoculturas.
Verificou-se descida progressiva dos marcadores sistémicos de inflamação, sem necessidade de instituir terapêutica antibiótica empírica. O doente teve alta cerca de 3 semanas após, tendo sido orientado para a consulta externa. Alguns meses mais tarde, foi de novo internado por agravamento do quadro de insuficiência cardíaca.
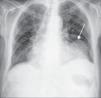
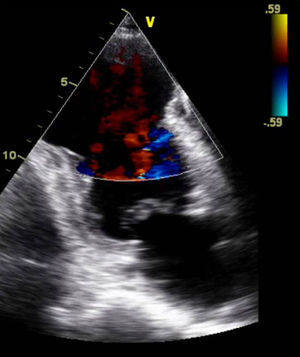
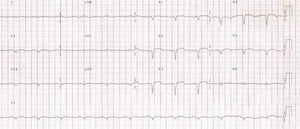
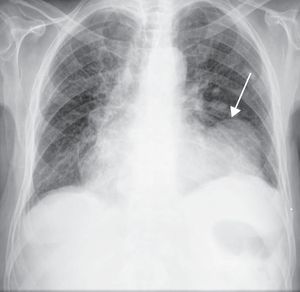
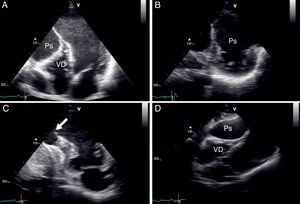
Apresentava no ECG sinais de EAM prévio (fig. 2) e no Rx de tórax observou-se a presença de uma massa adjacente à silhueta cardíaca (fig. 3). Repetiu ecocardiograma, que mostrou um volumoso aneurisma apical que se associava a imagem suspeita de pseudoaneurisma, com extensão ínfero-posterior e compressão do ventrículo direito (fig. 4).
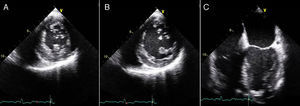
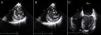
Ecocardiograma transtorácico bidimensional, incidência apical 4 cavidades (painel A), eixo curto (painel B), apical 2 cavidades (painel C) e subcostal (painel D), evidenciando a presença de pseudoaneurisma (Ps) ventricular esquerdo, de colo estreito (seta) e extensão ínfero-posterior, comprimindo o ventrículo direito (VD).
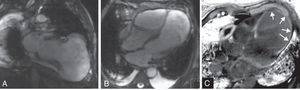
Face a estes achados, foi revertida a hipocoagulação oral e suspensa a terapêutica anti-agregante em curso. Para melhor esclarecimento anatómico com vista à planificação da cirurgia de correção, foi realizada ressonância cardíaca (RMC) que confirmou a presença de volumoso pseudoaneurisma, realçando-se toda a sua extensão e relação estreita com o ventrículo direito, condicionando compressão significativa do mesmo. As imagens de realce tardio permitiram definir a extensão da área de enfarte, certificando a presença de miocárdio viável ao nível dos segmentos médio-basais do ventrículo esquerdo (fig. 5).
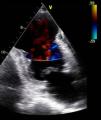
Ressonância magnética cardíaca, sequências cine (SSFP) nos planos eixo longo vertical (painel A) e 4 câmaras (painel B), confirmando a presença de volumoso pseudoaneurisma ventricular esquerdo. Imagens de realce tardio (PSIR) obtidas 10 minutos após a administração de gadolínio no plano 4 câmaras (painel C), observando-se área de retenção de produto de contraste transmural a envolver o aneurisma (seta).
Após coronariografia (que documentou oclusão da descendente anterior no segmento médio e estenose de 60% na coronária direita), foi submetido a ressecção cirúrgica do extenso falso aneurisma e exclusão do aneurisma VE, com reconstrução ventricular (cirurgia de dor) (fig. 6).
A recuperação inicial do doente foi lenta e arrastada, mas após a alta tem-se mantido clinicamente estável, em classe II NYHA. Repetiu ecocardiograma 3 meses após a intervenção cirúrgica que mostrou VE de dimensões normais, com compromisso ligeiro da função sistólica global e patch de ventriculoplastia normalmente inserido (fig. 7).
Ecocardiograma transesofágico bidimensional, eixo curto em sístole (painel A) e diástole (painel B) e 4 cavidades (em diástole, painel C) que mostra ventrículo esquerdo de dimensões normais, com função sistólica ligeiramente deprimida e patch de ventriculoplastia normalmente inserido e sem imagens de fluxo através do mesmo.
As complicações mecânicas no contexto de EAM são atualmente pouco frequentes em virtude da implementação eficaz de estratégias de revascularização precoce. Ainda que rara, a rotura cardíaca é um dos eventos mais temíveis em virtude de ser fatal na quase totalidade dos casos. Raramente, a rotura pode ser contida por pericárdio aderente ou tecido cicatricial, originando uma área sacular desprovida de elementos miocárdicos, a qual se designa de pseudoaneurisma. Atendendo à composição da sua parede, é grande o risco de expansão e rotura, impondo a necessidade de correção cirúrgica urgente. Em contraposição, o aneurisma ventricular representa o extremo da remodelagem maladaptativa consequente ao evento isquémico.
Consiste numa zona adelgaçada da parede ventricular (mantendo as habituais 3 camadas), de movimento discinético e apresentando um baixo risco de rotura.
Face a estas características, o aneurisma ventricular é habitualmente abordado de forma conservadora.
Raramente, estas 2 entidades coexistem4,5, não se podendo excluir a evolução do aneurisma ventricular complicada de rotura3,6, como possivelmente no caso clínico apresentado. Face às implicações prognóstica e terapêutica, é mandatório um diagnóstico correto e atempado do pseudoaneurisma.
Do ponto de vista clínico, os doentes podem encontrar-se assintomáticos (até 48% dos casos7) ou manifestar dor torácica recorrente, clínica de insuficiência cardíaca, síncope ou fenómenos tromboembólicos2,8. A morte súbita constitui a forma de apresentação do pseudoaneurisma ventricular em apenas 3% dos casos8.
Por seu lado, o exame físico é pouco distintivo, caracterizando-se por atenuação dos sons cardíacos, atrito pericárdico ou sopro de novo.
O ECG está alterado na maioria das situações, podendo evidenciar ondas Q patológicas ou persistência de supradesnivelamento do segmento ST nas derivações referentes ao território enfartado. Por seu lado, na telerradiografia torácica, estão presentes em mais de metade dos casos cardiomegalia e/ou uma massa adjacente ao contorno da silhueta cardíaca, como ilustrado na figura 3. Contudo, estes achados, ainda que frequentes, não são específicos, não permitindo identificar o pseudoaneurisma nem tão pouco distingui-lo do verdadeiro aneurisma ventricular. Assim, as modalidades de imagem cardíaca desempenham um papel fulcral no melhor esclarecimento desta entidade.
A ecocardiografia transtorácica é uma técnica de imagem não invasiva, acessível, usada comummente na avaliação inicial dos doentes com EAM, contribuindo não só para o seu diagnóstico, como também para definir o local e extensão do enfarte, identificar a presença de complicações mecânicas e fornecer informações que ajudam na estratificação do risco e do prognóstico. O diagnóstico diferencial dos pseudoaneurismas com os aneurismas ventriculares com base nos achados ecocardiográficos pode, contudo, constituir um verdadeiro desafio. Uma localização infero-postero-lateral2, um rácio < 0,5 entre a dimensão do orifício e o diâmetro interno máximo da região sacular9 assim como a presença no colo de fluxo turbulento, bidirecional, avaliado por Doppler de cor e pulsado10, constituem parâmetros sugestivos de se tratar de um pseudoaneurisma ventricular. Contudo, estes dados apresentam algumas limitações em relação à sua sensibilidade e especificidade2,3. De acordo com Frances et al., com base numa série de 290 doentes com pseudoaneurisma ventricular, a ecocardiografia transtorácica permitiu o diagnóstico definitivo em até um terço dos casos2. A capacidade diagnóstica pode ser melhorada com o recurso à ecocardiografia transesofágica (acuidade superior a 75%) ou ao produto de contraste (o qual permite otimizar a definição do contorno endocárdico bem como identificar a presença de distorção da normal geometria ventricular, como o pseudoaneurisma11.
A ventriculografia esquerda, por seu lado, tem sido considerada a modalidade de imagem gold standard, com uma acuidade diagnóstica da ordem dos 85%2. Os achados angiográficos característicos do pseudoaneurisma ventricular são a presença de uma região sacular de colo estreito e desprovida de vasos coronarianos adjacentes, retendo o produto de contraste no seu interior durante vários ciclos cardíacos12. Adicionalmente, o cateterismo cardíaco permite a deteção e caracterização de doença coronária, valvulopatia (particularmente mitral) e hipertensão pulmonar associadas, contribuindo para uma melhor planificação do tratamento cirúrgico a realizar. Contudo, trata-se de uma técnica invasiva, com exposição a radiação ionizante e que apresenta um risco real de embolização de material trombótico eventualmente presente.
Os avanços recentes permitiram a aplicação da tomografia axial computorizada na avaliação coronária não invasiva, bem como na caracterização anatómica tridimensional e funcional do miocárdio e pericárdio. A interrupção da continuidade do contorno endocárdico, originando uma área sacular pulsátil de colo estreito, aponta para o diagnóstico de pseudoaneurisma ventricular13. No entanto, o facto de não constituir uma modalidade de imagem muito acessível, de limitada resolução temporal, associado ao facto de requerer o uso de contraste iodado e expor o doente a radiação ionizante, tornam esta técnica um método de segunda linha neste âmbito14.
A RMC tem sido usada desde 1991 com o intuito de melhor diagnosticar os pseudoaneurismas ventriculares15,16. Trata-se de uma técnica de elevada resolução espacial e com capacidade de caracterização tecidular, permitindo identificar de forma não invasiva o pericárdio, a presença de trombo, assim como distinguir o tecido necrótico do miocárdio normal, o que nem sempre é possível com as outras modalidades de imagem. Para além de providenciar uma informação morfofuncional global (nomeadamente dos volumes e função sistólica ventriculares, bem como sobre a função valvular), a RMC fornece uma melhor definição morfológica do local, extensão e relação do pseudoaneurisma com as estruturas adjacentes. Por outro lado, a utilização de sequências de realce tardio contribuem para otimizar a localização e extensão da zona enfartada bem como a presença de miocárdio viável, contribuindo para uma melhor planificação da intervenção cirúrgica. Recentemente, o realce tardio pericárdico (não só adjacente à cavidade sacular, mas também junto ao miocárdio normal), foi proposto como um parâmetro útil na distinção entre o pseudoaneurisma do aneurisma ventricular verdadeiro, com uma sensibilidade de 100% e uma especificidade de 83%17. Considera-se que traduz a inflamação e fibrose pericárdicas decorrentes da passagem de sangue para o espaço pericárdico aquando da rotura.
Face a estas múltiplas vantagens, a RMC constitui uma modalidade de imagem muito atrativa, com enorme potencial na avaliação dos doentes com aneurismas versus pseudoaneurismas ventriculares. Dada a sua acessibilidade crescente e otimização das sequências de aquisição, esta técnica tem sido cada vez mais utilizada na prática clínica, mesmo em doentes com relativa instabilidade, como no caso apresentado. Acresce valor diagnóstico complementar ao da ecocardiografia, sobretudo nos doentes com janela acústica condicionada, e pela sua capacidade de caracterizar com precisão a extensão da área de enfarte e o número de segmentos viáveis, bem como as relações do pseudoaneurisma com a válvula mitral e músculos papilares. Esta avaliação é fundamental para uma correta planificação da técnica cirúrgica a implementar, que na maioria das vezes passa por uma cirurgia convencional, podendo, contudo, em casos selecionados passar pela transplantação cardíaca.
ConclusõesO diagnóstico diferencial entre os aneurismas e os pseudoaneurismas é particularmente difícil, mas fundamental, em virtude das implicações terapêuticas e prognósticas envolvidas. O incremento resolutivo das diferentes modalidades de imagem cardíaca não invasivas tem contribuído para um diagnóstico mais preciso e atempado, permitindo uma correta orientação dos doentes.
Conflito de interessesOs autores declaram não haver conflito de interesses.







![Imagens intra-operatórias evidenciando o ponto de entrada do pseudoaneurisma (painel A) e o aneurisma ressecado (painel B). O doente foi posteriormente submetido a reconstrução ventricular [cirurgia de Dor] (painel C).](https://static.elsevier.es/multimedia/08702551/0000003100000006/v1_201308021314/S0870255112000911/v1_201308021314/pt/main.assets/thumbnail/gr6.jpeg?xkr=ue/ImdikoIMrsJoerZ+w9znTMwFdb/TnkS0koegILxs=)