A cardioembolia representa uma das causas mais frequentes de lesões cerebrovasculares isquémicas, com prevalência estimada de 20-30% e implicações terapêuticas diretas que obrigam à sua correta avaliação. Apesar de a validação das escalas de risco cardioembólico (CHADS2 e, mais recentemente, CHA2DS2-VASc) em populações heterogéneas de doentes com fibrilhação furicular, desconhece-se ainda a sua validade em contexto de prevenção secundária cerebrovascular.
É objetivo deste trabalho estudar a sensibilidade e especificidade diferencial das escalas de risco cardioembólico como preditoras de fonte cardioembólica documentada por ecocardiograma transesofágico (ETE) numa população de doentes com AVC isquémico.
MétodosAplicámos as escalas CHADS2 e CHA2DS2-VASc a todos os doentes internados por evento cerebrovascular isquémico na Unidade de AVC/Enfermaria de Neurologia de um hospital central português com diagnóstico de fibrilhação auricular (prévio ou obtido durante/após o internamento), que realizaram ETE entre janeiro e agosto de 2011.
Definimos como presença de fonte cardioembólica a observação em ETE de autocontraste espontâneo na aurícula e apêndice auricular esquerdo ou trombos nas cavidades cardíacas esquerdas.
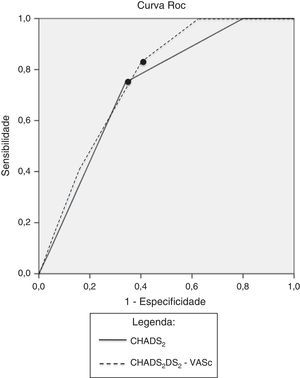
ResultadosAnalisámos 94 doentes, 66,0% do sexo masculino, idade média: 64,4 anos (desvio padrão: 14,2). Foi detetada fonte cardioembólica em 20 doentes. A análise de curva Receiver Operating Characteristic (ROC) identifica como preditores de fonte cardioembólica pontuação CHADS2 ≥ 4; sensibilidade: 75,0%, especificidade: 66,0%, p=0,014 e pontuação CHA2DS2-VASc ≥ 5; sensibilidade: 83,3%, especificidade: 58,0%, p=0,009.
ConclusõesAmbas as escalas apresentam sensibilidade significativa como preditoras de risco cardioembólico em contexto de prevenção secundária cerebrovascular. A escala CHA2DS2-VASc possui uma sensibilidade superior à CHADS2, sendo, no entanto, menos específica.
Cardioembolism is one of the most common causes of ischemic stroke, with an estimated prevalence of 20-30%, and correct diagnosis is essential given the therapeutic implications. Although stroke risk scores (CHADS2 and more recently CHA2DS2-VASc) have been validated in heterogeneous populations of patients with atrial fibrillation, their accuracy has not been ascertained for secondary stroke prevention. We set out to assess the sensitivity and specificity of the CHADS2 and CHA2DS2-VASc stroke risk scores as predictors of cardioembolic sources, documented by transesophageal echocardiography (TEE) in a population with ischemic stroke.
MethodsThe CHADS2 and CHA2DS2-VASc scores were applied to all patients admitted to the stroke unit/neurology ward of a Portuguese tertiary hospital with atrial fibrillation (diagnosed previously or during or after admission) who underwent TEE between January and August 2011.
The presence of a cardioembolic source was defined as the observation by TEE of spontaneous echo contrast in the left atrium and atrial appendage or thrombi in the left cardiac chambers.
ResultsWe studied 94 patients, 66.0% male, mean age 64.4 years (standard deviation 14.2). A cardioembolic source was detected in 20 patients. ROC curve analysis identified as predictors of cardioembolic source CHADS2 score ≥4 (sensitivity of 75.0%, specificity of 66.0%, p=0.014) and CHA2DS2-VASc score ≥5 (sensitivity of 83.3%, specificity of 58.0%, p=0.009).
ConclusionsBoth scores showed acceptable sensitivity as predictors of embolic risk in the context of secondary prevention of cardioembolic stroke. The CHA2DS2-VASc score has higher sensitivity than CHADS2 but lower specificity.
O acidente vascular cerebral (AVC) é a segunda causa de morte no mundo1, atingindo proporções particularmente alarmantes em Portugal, onde a taxa de mortalidade por AVC é de cerca de 200/100 000 habitantes, uma das mais elevadas da União Europeia2,3.
Do ponto de vista anatomopatológico e fisiopatológico, os acidentes vasculares cerebrais são divididos em dois grupos: isquémicos (80%) e hemorrágicos (20%)4. Os AVC isquémicos podem ser divididos segundo a classificação etiológica Trial of Org 10172 in Acute Stroke Treatment (TOAST) em cinco subtipos principais: aterotrombóticos, cardioembólicos, doença de pequenos vasos, outra causa conhecida, causa desconhecida5.
Uma etiologia cardioembólica é atribuída a cerca de 20 a 30% dos doentes com AVC isquémico6. Diversas patologias cardíacas aumentam o risco de ocorrência de AVC, sendo a fibrilhação auricular (FA) a sua causa mais comum7. Os fármacos anticoagulantes demonstraram reduzir eficazmente o risco de recorrência de AVC isquémico neste subtipo etiológico, estando, por isso, fortemente recomendada a sua utilização no contexto da prevenção primária e secundária8,9.
Com o objetivo de estratificar o risco de ocorrência de eventos cerebrovasculares cardioembólicos, foi criada a escala de risco CHADS210. Existem atualmente recomendações que relacionam a pontuação obtida com a aplicação desta escala e o plano terapêutico antitrombótico a adotar11. Recentemente, com o intuito de otimizar a anterior classificação, foi criada uma nova escala de risco cardioembólico, a CHA2DS2-VASc. Contudo, e apesar da sua validação numa população heterogénea de doentes com FA em prevenção primária12,13, desconhece-se ainda a sua validade em contexto de prevenção secundária cerebrovascular.
O ecocardiograma transesofágico (ETE) é um exame invasivo que dá uma boa informação anatómica da crossa da aorta, aurícula esquerda, apêndice auricular esquerdo, válvula mitral e válvula aórtica. Esta técnica é dotada de elevada sensibilidade e especificidade na deteção de fonte cardioembólica, possuindo uma capacidade três vezes superior ao ecocardiograma transtorácico (ETT) para atingir esse fim14.
O objetivo deste estudo é estudar uma possível associação entre as escalas de risco cardioembólico (CHADS2 e CHA2DS2-VASc) e a presença de fonte cardioembólica, identificada com recurso a ETE, em doentes com patologia cerebrovascular isquémica.
MétodosMateriais e populaçãoIncluímos no estudo todos os doentes internados na Unidade de AVC/Enfermaria cerebrovascular de Neurologia de um hospital central português com diagnóstico de FA (prévio ou obtido durante/após o internamento) que realizaram ecocardiograma transesofágico (ETE) para estudo de fonte cardioembólica entre janeiro e agosto de 2011.
O estudo por ETE foi realizado até cinco dias após o evento vascular no serviço de Cardiologia do mesmo hospital utilizando um ecocardiógrafo (GE Vivid 7 Dimension) equipado com uma sonda multiplanar transesofágica 6Tc RS. Foi definido como demonstração de fonte cardioembólica ativa a presença em ETE de trombos nas cavidades cardíacas esquerdas ou autocontraste espontâneo na aurícula e apêndice auricular esquerdos15.
Foram registadas as variáveis clínicas (hipertensão arterial, diabetes mellitus, coronariopatia, insuficiência cardíaca congestiva, tabagismo, dislipidémia, antecedentes pessoais de acidente vascular cerebral, alcoolismo), demográficas (sexo e idade) e analíticas dos doentes por consulta dos processos clínicos. O diagnóstico de FA foi assumido após visualização direta de exames complementares que o confirmavam. Nos doentes previamente anticoagulados (10; 10,6%) foi avaliada a eficácia da anticoagulação estudando o valor de INR à data da realização do ETE (± 72h).
Todos os doentes foram classificados de acordo com as escalas de risco vascular CHADS210 e CHA2DS2-VASc16. Comparámos todas as variáveis clínicas, demográficas e de risco cardiovascular para avaliar possíveis associações com presença de fonte cardioembólica.
Finalmente, avaliámos pontos de corte, sensibilidade, especificidade e valor preditivo positivo e negativo das escalas de risco cardioembólico como preditoras de cardioembolia ativa.
Análise estatísticaEfetuámos a análise estatística utilizando o software IBM SPSS Statistics 20.
Realizámos análise estatística descritiva com cálculo de média e desvio padrão (DP) para as variáveis quantitativas e do número absoluto (NA) e percentagem para as variáveis qualitativas.
Comparámos variáveis demográficas e prevalência de fatores de risco vascular, entre doentes com e sem fonte cardioembólica ativa utilizando o teste de chi-quadrado ou teste exato de Fischer, quando adequado para variáveis qualitativas e o teste t de Student para variáveis independentes com variáveis quantitativas.
Comparámos o valor obtido após a aplicação das diferentes escalas de risco cardioembólico e a data da realização do ETE com a presença ou não de fonte cardioembólica ativa documentada por ETE utilizando o teste U de Mann-Whitney para duas variáveis independentes.
Efetuámos curvas Reciever Operater Caractristic (ROC) para a determinação de valores de corte preditores de fonte cardioembólica na população total de doentes, assumindo igual importância de sensibilidade e especificidade para cada uma das escalas referidas. Esta análise foi então repetida na subpopulação de doentes não anticoagulados para avaliar a robustez dos resultados.
Definiu-se como significância estatística p < 0,05.
ResultadosPopulação estudadaDurante o período estudado, foram diagnosticadas doenças cerebrovasculares isquémicas (AIT/AVC) a 313 doentes. Destes, 94 doentes (30,0%) com diagnóstico de FA foram submetidos à realização de ecocardiograma transesofágico (ETE). O diagnóstico de FA havia sido obtido previamente a internamento em 66 (70,2%), durante este em 25 (26,6%) e após o internamento em 3 (3,2%). Identificámos fonte cardioembólica ativa em 20 doentes (21,3%) sendo caracterizada por autocontraste espontâneo nas cavidades cardíacas esquerdas em 19 doentes (20,2%), trombos nas cavidades cardíacas esquerdas em um (1,1%) e pela presença simultânea de ambos em oito (8,5%).
Apresentamos na Tabela 1 as características demográficas, fatores de risco vascular e resultados ecocardiográficos da população em estudo.
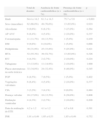
Prevalência de fatores de risco vascular na população em estudo
| Total de doentes | Ausência de fonte cardioembólica (n=74) | Presença de fonte cardioembólica (n=20) | p | |
| Idade | 64,4 ± 14,2 | 61,3 ± 14,3 | 75,7 ± 5,9 | < 0,001 |
| Sexo (masculino) | 62 (66,0%) | 49 (76,6%) | 13 (65,0%) | 0,919 |
| Alcoolismo | 9 (9,6%) | 6 (8,1%) | 3 (15,0%) | 0,364 |
| AP AVC | 6 (6,4%) | 4 (5,4%) | 2 (10,0%) | 0,337 |
| Coronariopatia | 11 (11,7%) | 10 (13,5%) | 1 (5,0%) | 0,439 |
| DM | 9 (9,6%) | 8 (10,8%) | 1 (5,0%) | 0,666 |
| Dislipidemia | 30 (31,9%) | 25 (33,8%) | 5 (25,0%) | 0,421 |
| HTA | 52 (55,3%) | 39 (52,7%) | 13 (65,0%) | 0,326 |
| ICC | 4 (4,3%) | 2 (2,7%) | 2 (10,0%) | 0,224 |
| Tabagismo | 13 (13,8%) | 11 (14,9%) | 2 (10,0%) | 1.000 |
| Placas ateromatosas na aorta torácica | 32 (34,0%) | 24 (32,4%) | 8 (40,0%) | 0,345 |
| FOP | 8 (8,5%) | 7 (9,5%) | 1 (5,0%) | 0,402 |
| Vegetações valvulares | 6 (6,4%) | 4 (5,4%) | 2 (10,0%) | 0,377 |
| CIA | 3 (3,2%) | 3 (4,1%) | 0 (0,0%) | 0,484 |
| Doença valvular | 16 (17,0%) | 10 (13,5%) | 6 (30,0%) | 0,808 |
| Disfunção ventricular | 4 (4,3%) | 2 (2,7%) | 2 (10,0%) | 0,209 |
| Data da realização do ETE | 4,2 ± 1,2 | 4,1 ± 1,2 | 4,5 ± 0,8 | 0,391 |
| INR | 1,91 ± 0,49 | 1,95 ± 0,53 | 1,85 ± 0,49 | 0,752 |
AP AVC: antecedentes pessoais de acidente vascular cerebral; CIA: comunicação intrerauricular; DM: diabetes mellitus; ETE: ecocardiograma transesofágico; FOP: foramen oval patente; HTA: hipertensão arterial; ICC: insuficiência cardíaca congestiva; INR: international normalized ratio.
Apresentam-se os valores de INR apenas para os doentes sob anticoagulação oral. Data da realização do ETE apresentada em dias após o evento vascular. As variáveis contínuas foram apresentadas como média ± desvio padrão e as variáveis qualitativas como número absoluto (%).
À data de alta hospitalar, 91 doentes (96,8%) estavam anticoagulados, tendo os restantes três (3,2%) contraindicação à sua utilização.
Risco cardioembólico e ecocardiograma transesofágicoA Tabela 2 apresenta a comparação realizada entre a pontuação obtida com a aplicação das escalas CHADS2 e CHA2DS2-VASc e a presença ou não de fonte cardioembólica ativa documentada por ETE.
Resultados da comparação entre as escalas de risco cardioembólico e a presença ou ausência de fonte cardioembólica
| Fonte cardioembólica ausente | Fonte cardioembólica presente | Total | p | |
| CHADS2 | 3,00 (3,00-4,00) | 4,00 (3,25-4,00) | 3,00 (3,00-4,00) | 0,009 |
| CHA2DS2-VASc | 4,00 (3,00-5,00) | 5,00 (5,00-6,00) | 4,50 (3,00-5,00) | 0,007 |
As pontuações das escalas estão apresentadas como mediana (intervalo inter-quartis).
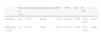
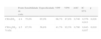
Apresentamos agora o estudo da sensibilidade, especificidade, valor preditivo positivo e valor preditivo negativo das escalas de risco CHADS2 e CHA2DS2-VASc na Tabela 3 e Figura 1. Na Tabela 4 apresentamos a análise das escalas de risco cardioembólico aplicadas na subpopulação de doentes não anticoagulados (n=84).
Resultados do estudo da curva ROC para as escalas de risco cardioembólico
| Ponto de corte | Sensibilidade | Especificidade | VPP | VPN | ASC | IC 95% | p | |
| CHADS2 | ≥ 4 | 75,0% | 66,0% | 33,3% | 81,4% | 0,720 | 0,587-0,872 | 0,014 |
| CHA2DS2-VASc | ≥ 5 | 83,3% | 58,0% | 35,7% | 85,4% | 0,746 | 0,617-0,874 | 0,009 |
ASC: área sob curva; IC 95%: intervalo de confiança de 95%; VPN: valor preditivo negativo; VPP: valor preditivo positivo.
Resultados do estudo da curva ROC para as escalas de risco cardioembólico incluindo apenas os doentes não anticoagulados (n=84)
| Ponto de corte | Sensibilidade | Especificidade | VPP | VPN | ASC | IC 95% | p | |
| CHADS2 | ≥ 4 | 75,0% | 65,9% | 66,7% | 87,8% | 0,746 | 0,579-0,913 | 0,028 |
| CHA2DS2-VASc | ≥ 5 | 87,5% | 56,8% | 41,7% | 92,5% | 0,790 | 0,642-0,937 | 0,010 |
ASC: área sob curva; IC 95%: intervalo de confiança de 95%; VPN: valor preditivo pegativo; VPP: valor preditivo positivo.
O presente trabalho teve como principal objetivo avaliar a sensibilidade e especificidade das escalas de risco cardioembólico CHADS2 e CHA2DS2-VASc como preditoras de fonte cardioembólica numa população de doentes cerebrovasculares.
Neste estudo, demonstrámos que a idade tem um peso determinante na presença de cardioembolismo, o que vai ao encontro dos resultados obtidos noutras investigações desta área17 e reflete a importância reforçada deste fator na nova escala de risco CHA2DS2-VASc. Não foi encontrada nenhuma associação significativa entre os restantes fatores de risco e demográficos avaliados e a presença de fonte cardioembólica, o que também tem sido referenciado em publicações anteriores18. O valor médio de INR nos doentes previamente anticoagulados encontra-se em valores subterapêuticos, não tendo sido verificada diferença com significado estatístico entre os doentes com e sem fonte cardioembólica documentada. Este dado deverá ser interpretado com precaução atendendo ao número reduzido da amostra de doentes previamente medicados com antivitamínicos K, mas alerta para a necessidade contínua de otimização posológica.
As variáveis utilizadas como indicadoras de fonte cardioembólica encontram-se já identificadas por diversos autores15,19,20 como eficazes na predição de fonte cardioembólica em doentes com FA. O facto de o ETE ser o exame com maior acuidade para a presença de autocontraste espontâneo na aurícula esquerda reforça a sua importância. No entanto, para doentes com FA e atendendo às indicações atuais da terapêutica anticoagulante, a Sociedade Europeia de Cardiologia não aconselha a sua realização por rotina, sugerindo-o apenas em circunstâncias particulares21. Não obstante, na fase aguda do evento cerebrovascular, o clínico assistente necessita frequentemente de informação segura do risco cardioembólico para planear a cronologia de introdução de terapêutica antitrombótica para um doente em particular, transformando os dados de ETE num complemento decisivo para essa decisão clínica, mesmo em doentes já com diagnóstico prévio de FA.
A análise das pontuações obtidas com a aplicação das escalas de risco cardioembólico CHADS2 e CHA2DS2-VASc revela que estamos perante uma população cujo risco de ocorrência de novo AVC é moderado ou elevado22, o que seria de esperar nesta população em particular.
Os resultados deste trabalho são explícitos quanto à validade destas duas classificações (CHADS2 e CHA2DS2-VASc) na identificação de risco cardioembólico, confirmando o seu valor mesmo em contexto de prevenção secundária cerebrovascular. Não obstante, a avaliação da sensibilidade e especificidade diferencial destas escalas revelou assimetrias. Com efeito, a classificação mais recente parece ser mais sensível na predição de fonte cardioembólica ativa, mas menos específica do que a anterior, não se registando diferenças significativas em valores preditivos positivos ou negativos.
Vários estudos demonstraram que os antivitamínicos K são eficazes na prevenção primária e secundária de eventos cerebrovasculares; no entanto, estão também associados a risco de complicações hemorrágicas, bem como a uma taxa considerável de abandono da terapêutica23. Estas desvantagens contribuem para que a adesão às recomendações internacionais, no que respeita à prevenção de eventos tromboembólicos, esteja longe do desejável24. Novos fármacos demonstraram possuir eficácia igual ou superior à varfarina na prevenção de acidentes cerebrovasculares, implicando um menor risco hemorrágico e não obrigando a controlo analítico regular25–28. Estes factos condicionam uma alteração da relação risco-benefício da terapêutica antitrombótica profilática na FA, obrigando à reconsideração a curto prazo do ponto de corte para benefício da prescrição de anticoagulante e indicando a necessidade de escalas de risco cardioembólico com maior sensibilidade para predição de eventos isquémicos. Atendendo às características da escala CHA2DS2-VASc indicadas neste trabalho, esta parece apresentar um perfil mais útil para esse fim.
Como principais limitações do nosso estudo, identificamos o seu caráter unicêntrico e o facto de o ETE não ser realizado imediatamente após o evento vascular, permitindo, assim, a possibilidade de existência prévia de trombos não visualizados por este exame à data da sua realização. Refere-se ainda que o caráter frequentemente paroxístico desta patologia implica que a ausência de fonte cardioembólica documentada em determinado momento não exclui a sua possível existência anterior ou posterior.
ConclusõesOs resultados deste trabalho são explícitos quanto à validade das escalas de risco CHADS2 e CHA2DS2-VASc na identificação de risco cardioembólico em prevenção secundária cerebrovascular. A nova escala CHA2DS2-VASc parece apresentar uma vantagem em relação à anterior classificação pelo seu ganho em sensibilidade, admitindo-se que a ligeira diminuição de especificidade desta escala, à luz das novas abordagens terapêuticas, não parece traduzir nenhuma perda para a decisão médica informada e individualizada, sendo suplantada pelo seu ganho em sensibilidade.
Responsabilidades éticasProteção de pessoas e animaisOs autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dadosOs autores declaram ter seguido os protocolos de seu centro de trabalho acerca da publicação dos dados de pacientes e que todos os pacientes incluídos no estudo receberam informações suficientes e deram o seu consentimento informado por escrito para participar nesse estudo.
Direito à privacidade e consentimento escritoOs autores declaram que não aparecem dados de pacientes neste artigo.
Conflito de interessesOs autores declaram não haver conflito de interesses.