Os novos anticoagulantes orais são opções emergentes para a prevenção e tratamento das doenças tromboembólicas. São cada vez mais usados na prática clínica pela facilidade do seu uso e pelos seus benefícios clínicos, mas a sua utilização mais generalizada carece de demonstração de custo‐efetividade. O objetivo do estudo A Review of Cost EFFectiveness of Novel ORal Anticoagulant Drugs (AFFORD) consistiu na realização de uma revisão sistemática dos estudos de custo‐efetividade dos novos anticoagulantes orais na prevenção do acidente vascular cerebral (AVC) na fibrilhação auricular não valvular (FA).
MétodosFoi realizada uma revisão sistemática da literatura nas bases de dados Pubmed, Embase, Scopus, Cochrane e Web of Knowledge para identificar todos os estudos de custo‐efetividade dos novos anticoagulantes orais na prevenção do AVC na FA.
ResultadosA pesquisa selecionou 27 estudos, 18 com dabigatrano, três com apixabano, dois com rivaroxabano e quatro com pelo menos dois destes fármacos. Os rácios custo‐efetividade incremental por anos de vida ajustados para qualidade foram de 30 405±16 101 euros para o dabigatrano 110mg, 17 566±16 902 euros para o dabigatrano 150mg, 8102±3252 euros para o dabigatrano ajustado à idade, 11 897±3341 euros para o apixabano e 17 960±12 005 euros para o rivaroxabano.
ConclusõesA presente revisão sistemática demonstra que os novos anticoagulantes orais são custo‐efetivos para a prevenção do AVC na FA.
Novel oral anticoagulants are emerging options for the prevention and treatment of thromboembolic diseases. They are increasingly used in clinical practice due to their simplicity of use and clinical benefits, but an important step is to evaluate their cost‐effectiveness. The aim of the AFFORD study (A Review of Cost EFFectiveness of Novel ORal Anticoagulant Drugs) was to perform a systematic review of cost‐effectiveness studies of novel oral anticoagulants for stroke prevention in non‐valvular atrial fibrillation (AF).
MethodsA systematic review of the literature was conducted by searching the PubMed, Embase, Scopus, Cochrane and Web of Knowledge databases to identify all cost‐effectiveness studies of novel oral anticoagulants for stroke prevention in AF.
ResultsThe search identified 27 studies, 18 with dabigatran, three with apixaban, two with rivaroxaban and four with at least two of these drugs. The incremental cost‐effectiveness ratios were 30 405±16 101 euros per quality‐adjusted life‐year (QALY) for dabigatran 110 mg, 17 566±16 902 euros/QALY for dabigatran 150 mg, 8102±3252 euros/QALY for age‐adjusted dabigatran, 11 897±3341 euros/QALY for apixaban and 17 960±12 005 euros/QALY for rivaroxaban.
ConclusionThe present systematic review demonstrates that novel oral anticoagulants are cost‐effective for stroke prevention in AF.
Anticoagulantes orais
Ano de vida ajustado para qualidade
Acidente vascular cerebral
Antagonistas da vitamina K
Dólar canadiano
Franco suíço
Fibrilhação auricular
Limite pré‐fixado à disponibilidade a pagar
Produto interno bruto
Rácio custo‐efetividade incremental
Dólar americano
Rand sul‐africano
As despesas em saúde têm crescido a um ritmo superior ao da criação de riqueza na maior parte dos países desenvolvidos. Em Portugal, a despesa do Estado em saúde per capita cresceu de 0,3 euros em 1972 para 989,4 euros em 20121. A despesa total passou de 2,8 em 1972 para 10 403,5 milhões de euros em 2012. Esta despesa correspondeu a 0,2% do produto interno bruto (PIB) em 1972 e cresceu para 6,3% do PIB em 2012. A despesa do Estado com medicamentos, que correspondeu a cerca de 17% da despesa total em saúde em 2010, tem acompanhado o crescimento da despesa em saúde1.
Todo este investimento na saúde traduz‐se numa melhoria dos seus indicadores, onde se destaca o aumento da esperança média de vida2.
Não obstante, existe uma maior consciencialização de que os recursos em saúde disponíveis para os procedimentos médicos, incluindo a terapêutica farmacológica, são cada vez mais limitados. Como tal, as avaliações económicas visam racionalizar estes recursos direcionando‐os eficientemente para onde são mais necessários.
É neste contexto que surge a análise custo‐efetividade, uma ferramenta que visa comparar o custo de uma intervenção de saúde com os ganhos em saúde esperados3. Esta intervenção pode ser entendida como qualquer atividade que usa recursos financeiros ou humanos e que tem como objetivo melhorar a saúde.
A fibrilhação auricular (FA) é a arritmia mais frequente na prática clinica4. O peso que esta patologia representa, em termos de morbilidade e mortalidade, mas também em termos económicos, é substancial. A prevenção do acidente vascular cerebral (AVC) pela administração de anticoagulantes é um dos principais objetivos no tratamento de doentes com FA5. A FA está associada a um estado pró‐trombótico, resultante da estase sanguínea intra‐auricular e de doença cardíaca estrutural, conduzindo a uma predisposição para a formação de trombos, particularmente no apêndice auricular esquerdo. Este estado pró‐trombótico predispõe ao embolismo cardíaco, fazendo com que os doentes tenham um risco cerca de cinco vezes superior de AVC e embolismo sistémico, em comparação com os indivíduos sem FA5. A terapêutica com anticoagulantes é a pedra angular para a prevenção e tratamento das doenças tromboembólicas6. Os novos anticoagulantes orais (ACO) representam um novo paradigma, já que apresentam uma maior facilidade de uso, bem como perfis farmacológicos mais favoráveis. Têm ainda um início de ação mais rápido e uma resposta anticoagulante mais previsível, conseguindo eliminar a necessidade de serem monitorizados6.
Foram realizados ensaios clínicos de fase III com quatro agentes para a prevenção do AVC em doentes com FA não valvular, que revelaram uma diminuição ou taxas semelhantes de tromboembolismo, hemorragia grave e efeitos adversos quando comparados com varfarina ou aspirina7–12.
Como resultado, uma aplicação ampla destes novos agentes pode conduzir a um aumento significativo dos doentes corretamente anticoagulados, muitos dos quais não recebiam sequer qualquer terapêutica devido às inconveniências e desvantagens dos antagonistas da vitamina K (AVK)4,5.
Todavia, sem meios adequados de controlo do nível de coagulação, a segurança e eficácia da aplicação destes novos fármacos a longo prazo, o tratamento de doentes com múltiplas comorbilidades e polimedicados, exigirá estudos observacionais mais extensos6. A falta de antídotos, de testes laboratoriais fiáveis, de evidência de segurança na prática clínica do mundo real e o custo elevado têm sido apontados como limitações importantes à sua utilização generalizada.
O estudo A Review of Cost EFFectiveness of Novel ORal Anticoagulant Drugs (AFFORD) é uma revisão sistemática dos estudos de custo‐efetividade dos novos ACO na prevenção do AVC na FA, com descrição dos resultados principais.
MétodosIdentificação de estudosA identificação de estudos foi conseguida através do uso de uma frase de pesquisa, «([adults AND humans] AND [«new oral anticoagulants» OR «new oral anticoagulation» OR «novel oral anticoagulants» OR «novel oral anticoagulation» OR «newer oral anticoagulants» OR «newest oral anticoagulants» OR «new generation oral anticoagulants» OR «oral direct thrombin inhibitor*» OR «new oral thrombin inhibitor*» OR «oral factor Xa inhibitor*» OR «orally active factor Xa inhibitor» OR «orally active thrombin inhibitor» OR rivaroxaban* OR dabigatran* OR apixaban* OR edoxaban*] AND [«cost‐effectiveness analysis» OR «cost‐effectiveness study» OR «cost‐effective» OR «cost‐effectiveness»] AND [«atrial fibrillation])», que foi utilizada em cinco bases de dados diferentes e consensuais no meio científico – Pubmed, Embase, Scopus, Cochrane e Web of Knowledge – para que pudessem ser encontrados estudos que estivessem integrados no objetivo deste estudo.
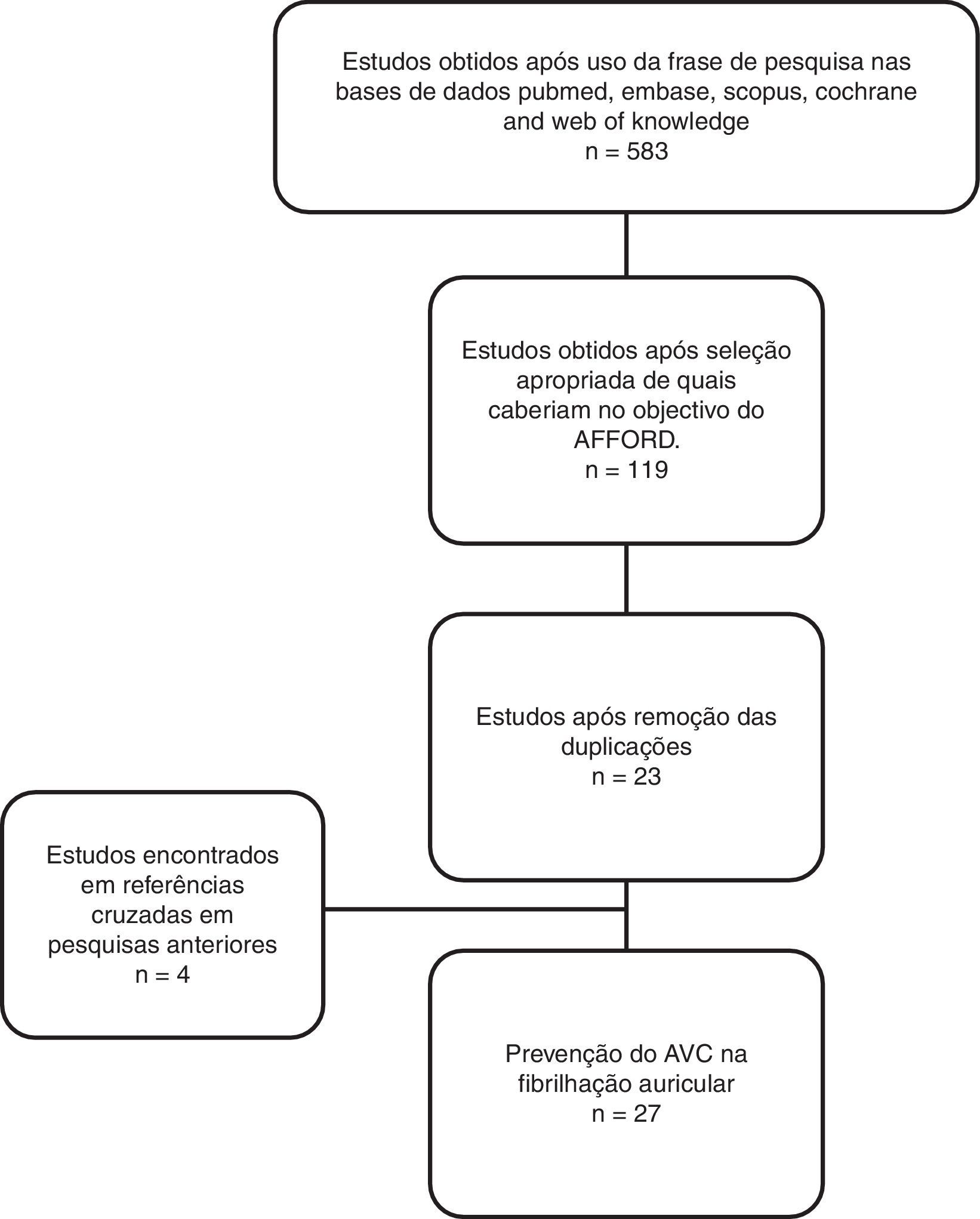
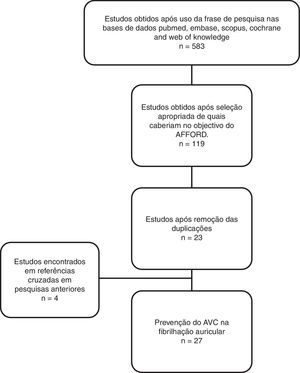
Pela pesquisa descrita anteriormente foram obtidos 533 estudos (Figura 1), que foram analisados pela leitura dos resumos e dos manuscritos, quando apropriado, com o objetivo de selecionar os estudos realizados em populações adultas que comparassem os novos ACO e os anticoagulantes tradicionais, através de uma análise de custo‐efetividade. Foram excluídos 414 estudos que não reuniam as condições descritas e 52 estudos publicados somente sob a forma de resumo.
Após eliminação dos estudos duplicados foram selecionados 23 artigos.
Além destes, foram selecionados mais quatro estudos publicados sob a forma de artigo que não apareceram na pesquisa nas bases de dados, quando se utilizou aquela frase de pesquisa. Três estudos foram encontrados nas referências bibliográficas dos manuscritos analisados e outro foi encontrado em pesquisas anteriores no Pubmed.
Colheita de dadosOs dados colhidos relativos ao modelo farmacoeconómico incluíram: 1) o país; 2) as comparações primárias – o novo ACO estudado e as doses, o anticoagulante comparador e os respetivos custos diários; 3) a estrutura do modelo e assunções, como modelos progenitores, a perspetiva do estudo; 4) os resultados do modelo incluindo o custo incremental, os anos de vida ajustados para a qualidade (AVAQ) e o rácio custo‐efetividade incremental (RCEI), o limite pré‐fixado à disponibilidade a pagar (LPFDP) por ano de vida ou por AVAQ ganho e as análises de sensibilidade.
Avaliação da qualidade dos estudosA qualidade dos estudos foi avaliada pelos investigadores, através da disponibilidade dos dados pré‐definidos nos modelos dos estudos selecionados, que estão incluídos nos critérios da escala Quality of Health Economic Studies13.
Análise estatísticaA natureza descritiva da presente revisão sistemática não se enquadrou numa análise estatística formal. As características e os resultados dos modelos farmacoeconómicos selecionados foram apresentados de forma qualitativa, com suporte nos valores de custo incremental, AVAQ, RCEI, LPFDP e percentagem nas análises de sensibilidade.
Para cada fármaco foram calculadas as médias e os desvios padrão dos RCEI por AVAQ, após conversão em euros, quando apropriado, utilizando a taxa cambial em 16/05/2014: 1 dólar americano (USD)=0,7321 euros; 1 dólar canadiano (CAD)=0,6736 euros; 1 libra esterlina=1,2267 euros; 1 franco suíço (CFH)=0,819 euros; 1 rand sul‐africano (ZAR)=0,0708 euros.
ResultadosDos 27 estudos selecionados na pesquisa efetuada (Tabela 1)14–40, a maioria é oriunda da Europa, com 11 estudos15,18,19,21,22,24,26–29,33 e dos Estados Unidos da América (EUA)14,16,20,31,32,34–36,38,39, com dez estudos. Com origem no Canadá foram encontrados três estudos17,27,30 e ainda dois da China23,30 e outro da África do Sul25.
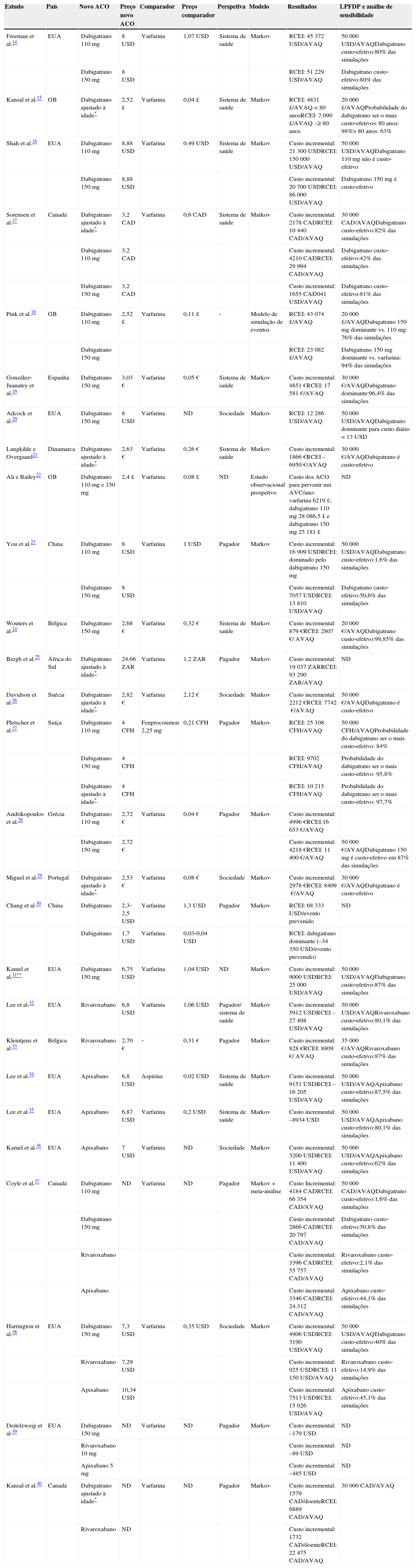
Características e resultados dos estudos de custo‐efetividade dos novos ACO na prevenção do AVC na FA
| Estudo | País | Novo ACO | Preço novo ACO | Comparador | Preço comparador | Perspetiva | Modelo | Resultados | LPFDP e análise de sensibilidade |
|---|---|---|---|---|---|---|---|---|---|
| Freeman et al.14 | EUA | Dabigatrano 110mg | 8USD | Varfarina | 1,07USD | Sistema de saúde | Markov | RCEI: 45 372USD/AVAQ | 50 000USD/AVAQDabigatrano custo‐efetivo:80% das simulações |
| Dabigatrano 150mg | 8USD | RCEI: 51 229USD/AVAQ | Dabigatrano custo‐efetivo:80% das simulações | ||||||
| Kansal et al.15 | GB | Dabigatrano ajustado à idade* | 2,52£ | Varfarina | 0,04£ | Sistema de saúde | Markov | RCEI: 4831£/AVAQ <80 anosRCEI: 7.090£/AVAQ –≥80 anos | 20 000£/AVAQProbabilidade do dabigatrano ser o mais custo‐efetivo<80 anos: 98%>80 anos: 63% |
| Shah et al.16 | EUA | Dabigatrano 110mg | 8,88USD | Varfarina | 0,49USD | Sistema de saúde | Markov | Custo incremental: 21 300USDRCEI: 150 000USD/AVAQ | 50 000USD/AVAQDabigatrano 110mg não é custo‐efetivo |
| Dabigatrano 150mg | 8,88USD | Custo incremental: 20 700USDRCEI: 86 000USD/AVAQ | Dabigatrano 150mg é custo‐efetivo | ||||||
| Sorensen et al.17 | Canadá | Dabigatrano ajustado à idade* | 3,2CAD | Varfarina | 0,6CAD | Sistema de saúde | Markov | Custo incremental: 2178CADRCEI: 10 440CAD/AVAQ | 30 000CAD/AVAQDabigatrano custo‐efetivo:82% das simulações |
| Dabigatrano 110mg | 3,2CAD | Custo incremental: 4210CADRCEI: 29 994CAD/AVAQ | Dabigatrano custo‐efetivo:42% das simulações | ||||||
| Dabigatrano 150mg | 3,2CAD | Custo incremental: 1655CAD041USD/AVAQ | Dabigatrano custo‐efetivo:81% das simulações | ||||||
| Pink et al.18 | GB | Dabigatrano 110mg | 2,52£ | Varfarina | 0,11£ | ‐ | Modelo de simulação de eventos | RCEI: 43 074£/AVAQ | 20 000£/AVAQDabigatrano 150mg dominante vs. 110mg: 76% das simulações |
| Dabigatrano 150mg | RCEI: 23 082£/AVAQ | Dabigatrano 150mg dominante vs. varfarina: 94% das simulações | |||||||
| González‐Juanatey et al.19 | Espanha | Dabigatrano 150mg | 3,03€ | Varfarina | 0,05€ | Sistema de saúde | Markov | Custo incremental: 4851€RCEI: 17 581€/AVAQ | 30 000€/AVAQDabigatrano dominante:96,4% das simulações |
| Adcock et al.20 | EUA | Dabigatrano 150mg | 8USD | Varfarina | ND | Sociedade | Markov | RCEI: 12 286USD/AVAQ | 50 000USD/AVAQDabigatrano dominante para custo diário <13USD |
| Langkilde e Overgaard21 | Dinamarca | Dabigatrano ajustado à idade* | 2,63€ | Varfarina | 0,26€ | Sistema de saúde | Markov | Custo incremental: 1866€RCEI – 6950€/AVAQ | 30 000€/AVAQDabigatrano é custo‐efetivo |
| Ali e Bailey22 | GB | Dabigatrano 110mg e 150mg | 2,4£ | Varfarina | 0,08£ | ND | Estudo observacional prospetivo | Custo dos ACO para prevenir um AVC/ano: varfarina 6219£; dabigatrano 110mg 28 086,5£ e dabigatrano 150mg 25 181£ | ND |
| You et al.23 | China | Dabigatrano 110mg | 8USD | Varfarina | 1USD | Pagador | Markov | Custo incremental: 16 909USDRCEI: dominado pelo dabigatrano 150mg | 50 000USD/AVAQDabigatrano custo‐efetivo:1,6% das simulações |
| Dabigatrano 150mg | 8USD | Custo incremental: 7057USDRCEI: 13 810USD/AVAQ | Dabigatrano custo‐efetivo:50,6% das simulações | ||||||
| Wouters et al.24 | Bélgica | Dabigatrano 150mg | 2,68€ | Varfarina | 0,32€ | Sistema de saúde | Markov | Custo incremental: 879€RCEI: 2807€/ AVAQ | 20 000€/AVAQDabigatrano custo‐efetivo:99,85% das simulações |
| Bergh et al.25 | África do Sul | Dabigatrano ajustado à idade* | 24,66ZAR | Varfarina | 1,2ZAR | Pagador | Markov | Custo incremental: 19 037ZARRCEI: 93 290ZAR/AVAQ | ND |
| Davidson et al.26 | Suécia | Dabigatrano ajustado à idade* | 2,82€ | Varfarina | 2,12€ | Sociedade | Markov | Custo incremental: 2212€RCEI: 7742€/AVAQ | 50 000€/AVAQDabigatrano é custo‐efetivo |
| Pletscher et al.27 | Suíça | Dabigatrano 110mg | 4CFH | Fenprocoumon 2,25mg | 0,21CFH | Pagador | Markov | RCEI: 25 108CFH/AVAQ | 50 000CFH/AVAQProbabilidade do dabigatrano ser o mais custo‐efetivo: 84% |
| Dabigatrano 150mg | 4CFH | RCEI: 9702CFH/AVAQ | Probabilidade do dabigatrano ser o mais custo‐efetivo: 95,8% | ||||||
| Dabigatrano ajustado à idade* | 4CFH | RCEI: 10 215CFH/AVAQ | Probabilidade do dabigatrano ser o mais custo‐efetivo: 97,7% | ||||||
| Andrikopoulos et al.28 | Grécia | Dabigatrano 110mg | 2,72€ | Varfarina | 0,04€ | Pagador | Markov | Custo incremental: 4996€RCEI:16 653€/AVAQ | |
| Dabigatrano 150mg | 2,72€ | Custo incremental: 4218€RCEI: 11 400€/AVAQ | 50 000€/AVAQDabigatrano 150mg é custo‐efetivo em 87% das simulações | ||||||
| Miguel et al.29 | Portugal | Dabigatrano ajustado à idade* | 2,53€ | Varfarina | 0,08€ | Sociedade | Markov | Custo incremental: 2978€RCEI: 8409€/AVAQ | 30 000€/AVAQDabigatrano é custo‐efetivo |
| Chang et al.30 | China | Dabigatrano | 2,3‐2,5USD | Varfarina | 1,3USD | Pagador | Markov | RCEI: 68 333USD/evento prevenido | ND |
| Dabigatrano | 1,7USD | Varfarina | 0,03‐0,04USD | RCEI: dabigatrano dominante (–34 350USD/evento prevenido) | |||||
| Kamel et al.31** | EUA | Dabigatrano 150mg | 6,75USD | Varfarina | 1,04USD | ND | Markov | Custo incremental: 9000USDRCEI: 25 000USD/AVAQ | 50 000USD/AVAQDabigatrano custo‐efetivo:87% das simulações |
| Lee et al.32 | EUA | Rivaroxabano | 6,8USD | Varfarina | 1,06USD | Pagador/ sistema de saúde | Markov | Custo incremental: 5912USDRCEI – 27 498USD/AVAQ | 50 000USD/AVAQRivaroxabano custo‐efetivo:80,1% das simulações |
| Kleintjens et al.33 | Bélgica | Rivaroxabano | 2,70€ | ‐ | 0,31€ | Pagador | Markov | Custo incremental: 828€RCEI: 8809€/ AVAQ | 35 000€/AVAQRivaroxabano custo‐efetivo:87% das simulações |
| Lee et al.34 | EUA | Apixabano | 6,8USD | Aspirina | 0,02USD | Sistema de saúde | Markov | Custo incremental: 9151USDRCEI – 16 205USD/AVAQ | 50 000USD/AVAQApixabano custo‐efetivo:87,5% das simulações |
| Lee et al.35 | EUA | Apixabano | 6,87USD | Varfarina | 0,2USD | Sistema de saúde | Markov | Custo incremental: –8934USD | 50 000USD/AVAQApixabano custo‐efetivo:80,1% das simulações |
| Kamel et al.36 | EUA | Apixabano | 7USD | Varfarina | ND | Sociedade | Markov | Custo incremental: 3200USDRCEI: 11 400USD/AVAQ | 50 000USD/AVAQApixabano custo‐efetivo:62% das simulações |
| Coyle et al.37 | Canadá | Dabigatrano 110mg | ND | Varfarina | ND | Pagador | Markov + meta‐análise | Custo Incremental: 4184CADRCEI: 66 354CAD/AVAQ | 50 000CAD/AVAQDabigatrano custo‐efetivo:1,6% das simulações |
| Dabigatrano 150mg | Custo incremental: 2866CADRCEI: 20 797CAD/AVAQ | Dabigatrano custo‐efetivo:50,8% das simulações | |||||||
| Rivaroxabano | Custo incremental: 3396CADRCEI: 55 757CAD/AVAQ | Rivaroxabano custo‐efetivo:2,1% das simulações | |||||||
| Apixabano | Custo incremental: 3346CADRCEI: 24.312CAD/AVAQ | Apixabano custo‐efetivo:44,1% das simulações | |||||||
| Harrington et al.38 | EUA | Dabigatrano 150mg | 7,3USD | Varfarina | 0,35USD | Sociedade | Markov | Custo incremental: 4906USDRCEI: 3190USD/AVAQ | 50 000USD/AVAQDabigatrano custo‐efetivo:40% das simulações |
| Rivaroxabano | 7,29USD | Custo incremental: 925USDRCEI: 11 150USD/AVAQ | Rivaroxabano custo‐efetivo:14,9% das simulações | ||||||
| Apixabano | 10,34USD | Custo incremental: 7513USDRCEI: 15 026USD/AVAQ | Apixabano custo‐efetivo:45,1% das simulações | ||||||
| Deitelzweig et al.39 | EUA | Dabigatrano 150mg | ND | Varfarina | ND | Pagador | Markov | Custo incremental: –179USD | ND |
| Rivaroxabano 10mg | Custo incremental: –89USD | ND | |||||||
| Apixabano 5mg | Custo incremental: –485USD | ND | |||||||
| Kansal et al.40 | Canadá | Dabigatrano ajustado à idade* | ND | Varfarina | ND | Pagador | Markov | Custo incremental: 1579CAD/doenteRCEI: 6889CAD/AVAQ | 30 000CAD/AVAQ |
| Rivaroxabano | ND | Custo incremental: 1732CAD/doenteRCEI: 22 475CAD/AVAQ |
As perspetivas mais seguidas nestes estudos foram do ponto de vista do sistema de saúde (11 estudos)14,19,21,24,26,29,33,35, do pagador (nove estudos)23,25–27,30,33,37,39,40 e da sociedade (três estudos)20,36,38.
O modelo escolhido pela grande maioria dos estudos (93%) foi o modelo de Markov14–17,19–21,23–40. Além deste modelo, um estudo utilizou um modelo de simulação discreta de eventos18 e foi realizado um estudo observacional prospetivo22.
O dabigatrano foi o fármaco mais estudado nesta indicação específica e foi analisado individualmente em 67% dos estudos apurados14–31. O apixabano foi analisado de forma particular em três estudos34–36 e o rivaroxabano em dois32,33. Todos os restantes compararam pelo menos dois dos novos anticoagulantes com a varfarina37–40.
O comparador mais utilizado foi a varfarina, na sua dose ajustada, sendo que a maior parte considerou o impacto da variabilidade no controlo do INR nos seus resultados. Apenas os estudos de Pletscher et al., que utilizou o fenprocoumon27, e o de Lee et al., que utilizou a aspirina34, não utilizaram a varfarina como comparador. O primeiro estudo utilizou o fenprocoumon por ser o AVK mais utilizado na Suíça, país de onde é oriundo este estudo. O segundo estudo baseou‐se nos resultados do ensaio clínico AVERROES, que comparou o apixabano com a aspirina em doentes com FA intolerantes aos AVK31.
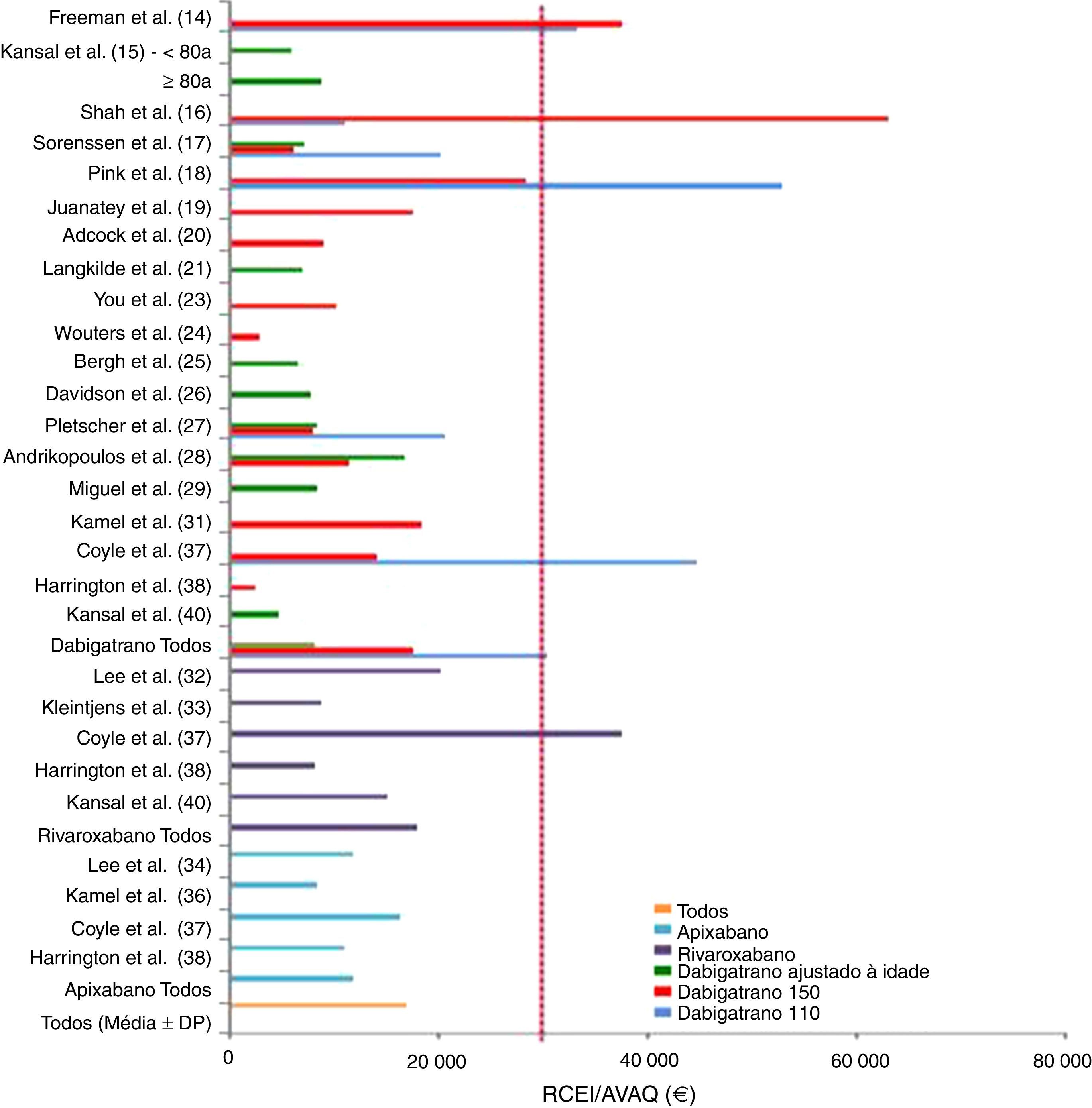
Em geral, todos os estudos apontaram para a existência de custo‐efetividade por parte dos novos ACO, uma vez que os RCEI ficaram bastante abaixo dos LPFDP, traçados pelos autores do estudo, mas em geral concordantes com os definidos pelos sistemas de saúde específicos, como limite para a comparticipação ou reembolso (Figura 2). A média dos RCEI por AVAQ foram de 30 405±16 101 euros para o dabigatrano 110mg, 17 566±16 902 euros para o dabigatrano 150mg, 8102±3252 euros para o dabigatrano ajustado à idade, 11 897±3341 euros para o apixabano e 17 960±12 005 euros para o rivaroxabano.
A tendência que se observou nos estudos em que o dabigatrano foi analisado em separado é que este anticoagulante na dose de 150mg foi mais custo‐efetivo, apesar da variabilidade verificada nas diversas análises de sensibilidade. O mesmo se observou na dose ajustada à idade (150mg 2x/dia para os doentes com idade inferior a 80 anos e 110mg 2x/dia para os restantes) que demonstrou custo‐efetividade em todas as análises que a incluíram15,17,21,25–27,29,40. A dose de 110mg além de ter, regra geral, um custo incremental mais elevado, não foi custo‐efetiva em 43% dos modelos que a analisaram em separado16,23,37.
Foi também incluída na revisão sistemática uma análise custo‐efetividade realizada em Portugal, sobre a utilização do dabigatrano na prevenção do AVC na FA, que utilizou nos seus cálculos, quer dados económicos quer custos de terapêutica praticados no nosso país. Esta análise concluiu de forma clara que a utilização do dabigatrano na prática clínica portuguesa é custo‐efectiva29.
No caso do rivaroxabano, como anteriormente referido, foram analisados dois estudos, um norte‐americano32 e outro belga33, e ambos mostraram que este agente foi custo‐efetivo na maioria das simulações realizadas nas análises de sensibilidade.
No que se refere aos três estudos específicos do apixabano, todos realizados nos EUA, este associou‐se a poupança no modelo que o comparou com a aspirina34 e noutro modelo que usou a varfarina como comparador35. No terceiro modelo revelou custo‐efetividade em 62% das simulações nas análises de sensibilidade36.
Nos estudos em que os três novos ACO foram comparados em simultâneo37–39, os resultados apontam para que o apixabano seja o mais custo‐efetivo, seguido pelo dabigatrano e rivaroxabano. Nos modelos de Coyle et al.37 e de Harrington et al.38 a conclusão é suportada pelo custo incremental e pela análise da sensibilidade. No modelo de Deitelzweig et al.39 o custo incremental foi negativo para os três ACO, indicando geração de poupança, mas o valor foi mais elevado para o apixabano. No modelo de Kansal et al.40 para a realidade canadiana o dabigatrano foi mais custo‐efetivo do que o rivaroxabano (RCEI 6889CAN/AVAQ vs. 22475CAN/AVAQ).
DiscussãoOs novos ACO mostraram ter vantagens farmacológicas quando comparados com os anticoagulantes tradicionais, que se traduziram geralmente em benefícios clínicos nos numerosos ensaios em diversos cenários clínicos7–12.
A presente revisão sistemática surge num contexto em que esta inovação farmacológica se começa a manifestar com uma utilização mais ampla destes novos agentes na prática clinica. Por serem terapêuticas mais dispendiosas, acarretam um maior peso em termos de custos para os sistemas de saúde e para os seus beneficiários.
O estudo AFFORD pretende agregar os estudos de análise económica dos novos ACO publicados, para perceber se há custo‐efetividade, ou seja, se os ganhos em saúde superam o custo desta nova terapêutica. Este estudo inclui pela primeira vez na metodologia de uma revisão sistemática de análises de custo efetividade, o cálculo da média da sua variável mais importante, o ICER por AVAQ, após conversão em euros dos estudos referidos a outras moedas.
Estes estudos são oriundos de diferentes partes do globo, estando representados países da América, Europa, África e Ásia, que apresentam diferentes modelos económicos, diferentes perspetivas económicas para a sua realização, diversos comparadores, preços variáveis das terapêuticas, diferentes formas de apresentação do resultado final e ainda diversos limites de disponibilidade para pagar. Por este motivo, um dos desafios na avaliação comparativa dos diferentes modelos consistiu na variabilidade das metodologias utilizadas.
Apesar desta variabilidade, os resultados são consistentes e demostraram custo‐efetividade dos novos ACO face às terapêuticas convencionais mais utilizadas, neste caso a varfarina na prevenção do AVC na FA.
Nesta revisão sistemática, os novos ACO que mais se destacam são o dabigatrano e o apixabano. O primeiro é o que possui maior número de estudos, relacionado com o facto de ser o mais antigo. É importante mencionar que os resultados dos estudos agora analisados estão intimamente relacionados com os resultados dos ensaios clínicos. No estudo RE‐LY, a utilização do dabigatrano na FA mostrou superioridade da dose de 150mg em termos de eficácia e da dose de 110mg na segurança, em comparação com a varfarina7,8. O dabigatrano na dose de 150mg e na dose ajustada à idade foi sempre custo‐efetivo e mostrou superioridade em percentagem elevada, acima de 80%, nas simulações das análises de sensibilidade. O apixabano mostrou superioridade, tanto em eficácia como em segurança, no estudo ARISTOTLE11, em comparação com a varfarina, e no estudo AVERROES10, em comparação com a aspirina.
É difícil comparar os resultados dos estudos que analisam os três fármacos em separado, porque são análises realizadas a partir de estudos e de ensaios clínicos com metodologias diferentes.
Os modelos estudados na prevenção do AVC na FA adotaram diferentes perspetivas, como pagador, sistema de saúde ou sociedade. As perspetivas do pagador e do sistema de saúde podem ser consideradas perspetivas coincidentes, uma vez que a perspetiva do pagador pode incluir companhias de seguros, entidades patronais ou o próprio governo que é quem gere o sistema de saúde na maior parte dos países. Já a perspetiva da sociedade é mais ampla porque considera o benefício para a comunidade como um todo. Teoricamente, todos os custos diretos e indiretos são incluídos na avaliação económica realizada a partir de uma perspetiva social3.
A presente revisão sistemática inclui três estudos37–39 em que os novos ACO foram analisados em simultâneo, o que permitiu estabelecer uma hierarquia em termos de desempenho farmacoeconómico. Embora sejam análises também diferentes entre si, todas apontam um resultado idêntico: os novos ACO são custo‐efetivos e o apixabano é o mais custo‐efetivo, seguido do dabigatrano e do rivaroxabano. No estudo de Deitelzweig et al.39 é referido que os três têm um custo incremental negativo pelo que geram poupança.
Outro ponto comum entre a maior parte destes estudos é o do modelo utilizado na análise económica. O modelo de Markov foi empregue em mais de 90% dos estudos analisados e consiste num modelo estatístico que permite simular a evolução dos doentes em ciclos de tempo até ao fim da sua vida. Em cada ciclo temporal é aplicada uma determinada probabilidade de ocorrência mutuamente exclusiva dos eventos mais importantes para a população em estudo. Podem ser utilizados diferentes desenhos deste modelo e também diferentes adaptações consoante a realidade de cada país ou consoante a orientação do próprio estudo económico29.
O estudo AFFORD tem também algumas limitações que devem ser referidas. Desde logo as comparações indiretas entre os novos ACO devem ser encaradas com reserva devido às diferentes metodologias utilizadas nos ensaios clínicos de eficácia e segurança. Também não existem guias internacionais padronizadas para a realização de análises económicas, o que coloca obstáculos a uma avaliação comparativa e precisa entre os diferentes modelos económicos41. Esta padronização é necessária, pois a preocupação crescente com a contenção de custos e racionalização dos recursos em saúde, origina uma proliferação de análises económicas que, para poderem ser comparáveis, devem obedecer a regras universais.
Outra limitação importante que pode ser apontada ao AFFORD é o facto de alguns autores dos estudos incluídos nesta revisão sistemática serem funcionários dos laboratórios de onde são oriundos os fármacos estudados, o que gera potenciais conflitos de interesse.
ConclusãoEm conclusão, o estudo AFFORD demostrou que os novos ACO são custo‐efetivos em comparação com as estratégias antitrombóticas convencionais, apesar de o seu elevado custo. Esta elação é verdadeira quer nos mais diversos contextos geográficos e sociais quer adotando diferentes metodologias de análise farmacoeconómica.
Responsabilidades éticasProteção de pessoas e animaisOs autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dadosOs autores declaram que não aparecem dados de pacientes neste artigo.
Direito à privacidade e consentimento escritoOs autores declaram que não aparecem dados de pacientes neste artigo.
Conflito de interessesOs autores declaram não haver conflito de interesses.


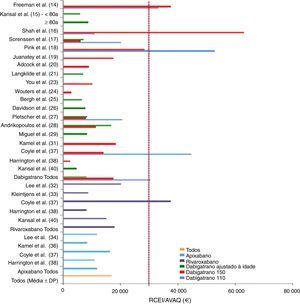 RCEI por
RCEI por 

