A pericardite constritiva é uma entidade clínica rara que pode colocar problemas diagnósticos. O método padrão para a confirmação do seu diagnóstico é o cateterismo cardíaco, com análise das curvas de pressão intracavitárias, as quais estão elevadas e, em telediástole, são iguais em todas as cavidades. O seu perfil diastólico em ambos os ventrículos apresenta o clássico aspeto dip-plateau e a diferença entre as pressões telediastólicas ventriculares não deve exceder 3-5mmHg. Infelizmente estes critérios clássicos nem sempre se verificam e, na verdade, a sensibilidade e a especificidade da igualização das pressões telediastólicas dos ventrículos é relativamente baixa e de valor limitado no doente individualmente considerado. Esta realidade evidencia a necessidade de utilizar as novas técnicas de imagem cardíaca, que podem tornar claro o que é duvidoso. O caso clínico aqui descrito é um bom exemplo.
Constrictive pericarditis is a rare clinical entity that can pose diagnostic problems. The gold standard for diagnosis is cardiac catheterization with analysis of intracavitary pressure curves, which are high and, in end-diastole, equal in all chambers. The diastolic profile in both ventricles presents the classic dip-and-plateau pattern and the difference between the diastolic pressures of both ventricles should not exceed 3-5mmHg. Unfortunately, these traditional criteria are not always present and in fact the sensitivity and specificity of equalization of diastolic pressures are relatively low and of limited value in individual patients. This highlights the need to use new cardiac imaging techniques to resolve any doubts. The case described here is a good example.
Homem de 78 anos de idade, caucasiano, internado por quadro grave de insuficiência cardíaca global descompensada (classe IV da NYHA), de predomínio clínico direito, com três meses de evolução e agravamento progressivo. Tinha diagnósticos prévios de hipertensão arterial, diabetes mellitus tipo 2, dislipidemia e hábitos tabágicos pregressos. Referia um internamento há 11 anos, em outra unidade hospitalar, por derrame pericárdico volumoso. Nesse mesmo internamento foi submetido a pericardiocentese evacuadora, com extração de 3.000 ml de líquido pericárdico compatível com exsudado, cuja etiologia não foi esclarecida (exames citológico e microbiológico, bacteriológico e micobacteriológico negativos). A tomografia computorizada (TC) do tórax era referida como tendo espessamento pleural e pericárdico, não investigados posteriormente. Negava antecedentes de tuberculose e tinha um teste de tuberculina negativo. Mantivera-se assintomático até três meses antes do atual internamento, quando se iniciou um quadro de falência cardíaca global, progressiva e incapacitante.
Do exame objetivoNa admissão ao Serviço de Cardiologia, o doente apresentava-se hemodinamicamente estável (tensão arterial 120/70mmHg), polipneico (24 cpm), sem cianose (saturação de O2 em ar ambiente de 94%) mas pálido. O pulso era cheio, arrítmico e simétrico. A auscultação cardiopulmonar revelou arritmia com tons hipofonéticos, presença de 3.° som precoce, sopro holossistólico no foco mitral com irradiação à axila e murmúrio vesicular diminuído nas bases de ambos os hemitóraxes, acompanhado de fervores crepitantes. Destacava-se marcado ingurgitamento venoso jugular, até ao ângulo mandibular, hepatomegália indolor (fígado palpável 10cm abaixo do rebordo costal direito na linha médio-clavicular), refluxo hepatojugular positivo e edemas dos membros inferiores, até ao joelho (+++/++++).
Dos exames auxiliaresNo eletrocardiograma (ECG), registou-se flutter auricular com bloqueio auriculoventricular variável e voltagem normal. Analiticamente, havia elevação marcada da velocidade de sedimentação (VS) (98mm) na ausência de leucocitose ou neutrofilía e proteína C reativa baixa (3mg/dL). A enzimologia hepática apresentava um padrão de congestão passiva (fosfatase alcalina e gama-GT mais elevadas do que as aminotransferases). O valor do NT-proBNP era normal (142 pg/mL). A radiografia (Rx) do tórax póstero-anterior mostrava um índice cardiotorácico normal, discreto derrame pleural bilateral e em perfil, uma imagem linear localizada à parede lateral do ventrículo esquerdo (VE), de aparência cálcica. No ecocardiograma, feito logo após a admissão, salientou-se a existência de um pericárdio espessado e hiperecogénico em toda a sua extensão. As cavidades ventriculares não estavam dilatadas, verificando-se moderado compromisso da função sistólica global do VE [fração de ejeção (FEj.) de 38%, método de Simpson biplano] e dilatação biauricular. As insuficiências mitrais e tricúspides eram ligeiras e o fluxo transvalvular tricúspide apresentava variação respiratória de cerca de 30%. O fluxo mitral não apresentava variação respiratória significativa e o tempo de desaceleração da onda E era de 120ms (média de 5 complexos). O estudo ecocardiográfico documentou ainda hipertensão pulmonar grave (pressão sistólica artéria pulmonar (PSAP) de 70mmHg) e dilatação da veia cava inferior (28mm), a qual apresentava reduzida variação respiratória (< 50%).
Diagnóstico provisórioFoi colocada como principal hipótese diagnóstica a pericardite constritiva (PC). A existência de doença coronária concomitante era uma hipótese a considerar, nomeadamente por se tratar de um doente com múltiplos fatores de risco cardiovasculares que apresentava função sistólica ventricular esquerda deprimida, assim como a hipótese de doença pulmonar (num doente com história pregressa de hábitos tabágicos e espessamento pleural), justificando um valor de PSAP elevado. Finalmente, não se podia excluir uma doença cardíaca mista, constritiva/restritiva.
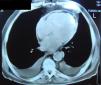
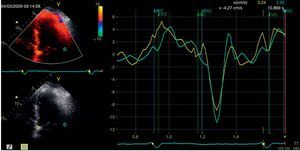
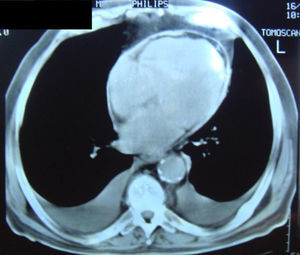
Dos exames complementares de diagnósticoNo estudo do nosso doente aplicámos então as novas modalidades ecocardiográficas, nomeadamente a determinação do strain do VE e o estudo da velocidade longitudinal do anel mitral em protodiástole (E’). Verificámos que o strain longitudinal do VE estava mantido, assim como a velocidade protodiastólica do anel mitral (E’ septal: 8,4cm/s; E/E’: 8,3) (Fig. 1), apresentando uma variação respiratória > 25%. Pelo contrário, o strain circunferencial estava reduzido, achados que corroboravam a hipótese de PC. À semelhança do exame realizado 11 anos antes, a TC do tórax documentou a existência de espessamento regular do pericárdio, desta vez com focos visíveis de calcificação pericárdica. Não se verificaram alterações pleuroparenquimatosas significativas (Fig. 2). Também a ressonância magnética (RM) cardíaca confirmou a existência de espessamento pericárdico, ligeiro, localizado às paredes ventriculares basais e medianas, atingindo na parede lateral do VE cerca de 3mm (normal < 2mm). Os volumes ventriculares e a FEj. do ventrículo direito eram normais. A FEj. do VE foi quantificada em 40% (moderadamente reduzida) e a insuficiência mitral era ligeira. Não foi efetuado estudo de realce tardio, por ausência de colaboração do doente na progressão do exame.
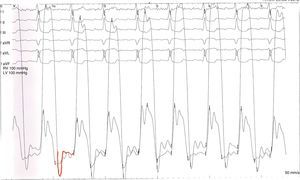
Ao 6.° dia de internamento e, apesar de seis dias de tratamento diurético, o exame hemodinâmico documentou elevação das pressões telediastólica do ventrículo esquerdo (22mmHg) e de encravamento pulmonar (22mmHg), e um índice cardíaco ligeiramente diminuído (1,87 L/min/m2). A hipertensão arterial pulmonar mantinha-se (pressão média da artéria pulmonar de 38mmHg). Apesar da curva de pressão do VE ser em forma de dip- plateau, o mesmo não se verificou na curva de pressão do ventrículo direito (VD). Além disso, as pressões telediastólicas das cavidades esquerdas apresentaram uma diferença > 5mmHg relativamente às direitas (Fig. 3), achado que não corroborava a hipótese de pericardite constritiva. A coronariografia excluiu a presença de lesões significativas e a ventriculografia mostrou compromisso da função sistólica global (FEj. 45%) e hipocinésia generalizada do ventrículo esquerdo.
Deparámo-nos assim com o diagnóstico de PC à luz da clínica, do laboratório (NT-proBNP normal) e dos exames de imagem não invasivos (Rx e TC do tórax, RM cardíaca). O eco-Doppler apresentava parâmetros que o apoiavam (padrão restritivo, fluxo transtricúspide com variação respiratória >25%) e outros que o refutavam (fluxo transmitral sem variação respiratória), sendo que as novas modalidades da ecocardiografia (estudo 2D-strain e Doppler tecidular do anel mitral) favoreciam a principal hipótese. O contrário se verificava com o estudo hemodinâmico.
No debate clínico, prevaleceu o diagnóstico de PC e como tal, o doente foi proposto para cirurgia de descorticação pericárdica, vindo esta a realizar-se 19 dias após a admissão.
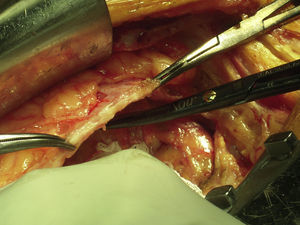
Dados da cirurgiaNo acto intra-operatório, constatou-se a existência de uma membrana pericárdica espessada, a qual foi completamente removida (Fig. 4). Foi efetuada biópsia pleural e pulmonar. O resultado anatomopatológico da peça enviada mostrou: «pericárdio com acentuado espessamento fibroso e focos de congestão e de infiltrado inflamatório crónico inespecífico; vários focos de calcificação distrófica». Mostrou ainda «pleura com áreas de espessamento fibroso com pigmento de antracose». No tecido pulmonar foram reconhecidas «áreas de enfisema e de fibrose intersticial, congestão e ligeiro infiltrado inflamatório crónico inespecífico focal».
Em relação à investigação etiológica efetuada durante o internamento, os exames realizados (hemoculturas, prova da tuberculina, doseamento da adenosina deaminase no sangue, serologias virais) foram negativos.
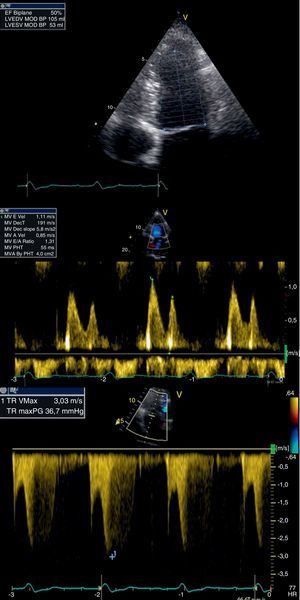
O pós-operatório decorreu sem intercorrências e o doente teve alta da nossa unidade hospitalar após um mês de internamento, francamente melhorado, apresentando-se, passados 29 meses, em classe funcional I da NYHA. O ecocardiograma do doente (Fig. 5), realizado em ritmo sinusal, apresenta melhoria da função sistólica global (FEj. Simpson biplano: 50%) assim como do strain circunferencial do VE. O tempo de desaceleração da onda E é de 191ms (superior ao inicial) e a razão onda E/onda A de 1,3, corroborando a melhoria da função diastólica. Não existe variação respiratória significativa dos fluxos valvulares e a PSAP foi estimada em 42mmHg (gradiente ventrículo direito-aurícula direita: 37mmHg), significativamente menor do que a da avaliação inicial, consequência provável da melhoria da função sistodiastólica ventricular esquerda. A veia cava inferior apresentava calibre e variação respiratória normais. Cerca de mês e meio após este último controlo cardiovascular, o doente apresentou pela primeira vez um quadro clínico de artrite reumatóide.
DiscussãoA PC é uma consequência rara mas grave da inflamação crónica do pericárdio, da qual resulta uma membrana fibrótica e rígida, que encarcera as cavidades cardíacas. A consequência hemodinâmica desta alteração anatómica é uma grave disfunção do enchimento diastólico ventricular, adicionalmente agravada pela disfunção sistólica que pode verificar-se como consequência da fibrose e atrofia miocárdica secundárias1. No caso apresentado, o doente apresentava disfunção sistodiastólica, consequência da evolução prolongada da pericardite constritiva. Habitualmente, existe um longo período entre a lesão pericárdica inicial e a existência de constrição1. No nosso doente, terão decorrido 11 anos.
O diagnóstico de pericardite constritiva deverá ser sempre considerado em doentes com sintomas predominantes de falência ventricular direita, tais como pressão venosa jugular aumentada, derrame pleural, hepatomegália, ascite e edemas periféricos. Para além destes aspetos sistémicos, é típico da PC a presença de 3.° som precoce (knock pericárdico), resultante da redução súbita do enchimento ventricular pela constrição pericárdica2. Casos mais graves cursam com hipotensão e colapso circulatório. O ecocardiograma convencional e Doppler é substancialmente importante para realizar o diagnóstico desta entidade, assim como para o diagnóstico diferencial com outras causas de falência ventricular direita3. Entre elas, pelas características semelhantes ao exame Doppler e ao exame hemodinâmico, a miocardiopatia restritiva (MCR) apresenta-se como o desafio mais difícil de superar. Particularmente no caso descrito, o compromisso da função sistólica ventricular esquerda, mais comum na MCR do que na PC, tornou este diagnóstico diferencial obrigatório. A variação respiratória dinâmica dos fluxos e a interdependência ventricular, que se verificam nos doentes com PC e não nos doentes com MCR, são os processos fisiopatológicos mais importantes neste diagnóstico diferencial1. Nos doentes com PC existe uma dissociação entre as pressões intratorácicas e intracardíacas, das quais resulta um decréscimo no enchimento do VE durante a inspiração. Da existência de um pericárdio rígido e inextensível resulta um aumento da interação ventricular e daí um aumento no enchimento do VD durante a inspiração. A ecocardiografia Doppler e Doppler tecidular têm um papel primordial na análise desta variação respiratória1. Quando subsistem dúvidas, as novas modalidades da ecocardiografia auxiliam no diagnóstico. Sabendo que na PC as propriedades mecano-elásticas do miocárdio estão relativamente preservadas na direção longitudinal, limitadas na direção circunferencial e que, apesar de a rotação da base e segmentos médios estar preservada, a rotação apical está marcadamente reduzida, conclui-se que o strain longitudinal e a velocidade do anel mitral em protodiástole (E¿) estão normais ou aumentados (ao contrário do que ocorre na MCR), o strain circunferencial e o net twist angle (diferença entre a rotação da base e a apical) estão reduzidos (à semelhança da MCR). No nosso doente, não foi avaliado o net twist angle.
Um valor de E’ mitral >8cm/segundo diferencia PC de MCR com uma sensibilidade de 89% e especificidade de 100%4. O estudo ecocardiográfico convencional, Doppler e 2D-strain, foi fundamental e decisivo no diagnóstico diferencial de PC versus MCR e permitiu-nos documentar a modificação das alterações cardíacas morfofuncionais pós-cirurgia de descorticação pericárdica. A melhoria da FEj. do VE pós-cirurgia apoia a hipótese de a disfunção sistólica ser secundária à inflamação crónica e fibrose do miocárdio subsequente ao processo de constrição pericárdica prolongado, facto que não sendo muito frequente confere ao nosso caso clínico alguma singularidade. O estudo de realce tardio por RM cardíaca, não efetuado no nosso caso pela razão atrás referida, permitir-nos-ia avaliar a existência de zonas de fibrose intramiocárdicas. No entanto, os valores iniciais normais do strain longitudinal assim como a recuperação da FEj. pós-cirurgia apoiam a ausência de fibrose intramiocárdica grave.
Ainda relativamente ao diagnóstico desta entidade, a TC do tórax e RM cardíaca detetam um pericárdio espessado, mas são meios de diagnóstico que providenciam informação meramente anatómica e não refletem necessariamente a alteração fisiopatológica presente5. No caso apresentado, estes dois exames apoiaram a nossa principal hipótese, documentando um pericárdio espessado, com focos de calcificação. No entanto, é importante lembrar que 18% dos doentes com PC comprovada cirurgicamente poderão apresentar um pericárdio normal e, portanto, a ausência de espessamento não refuta a hipótese de PC6.
Também a determinação do valor de NT-proBNP pode auxiliar no diagnóstico. Doentes com pericardite constritiva apresentam níveis de NT-proBNP normais (o verificado no caso apresentado) ou muito ligeiramente aumentados e, ao invés, doentes com miocardiopatia restritiva apresentam níveis muito elevados7. O fato de o doente ter desenvolvido recentemente um quadro de artrite reumatóide pode justificar o valor demasiado elevado de VS, uma vez que as alterações laboratoriais precedem frequentemente o quadro clínico neste tipo de patologia.
Quanto aos achados hemodinâmicos, a disfunção sistodiastólica ventricular esquerda permite-nos explicar a redução do índice cardíaco assim como a elevação das pressões telediastólica do VE, de encravamento pulmonar e da artéria pulmonar, esta última provavelmente também aumentada pela patologia pulmonar (enfisema) concomitante, documentado na biópsia pulmonar. Várias hipóteses foram colocadas para explicar a ausência de igualização das pressões telediastólicas ventriculares no nosso doente. A mais provável poderá ter sido a depleção de volume no momento do cateterismo cardíaco, ao 6.° dia de terapêutica diurética. Não foi efetuado bólus de fluido adicional, o que deverá ser feito para comprovar a existência de constrição, uma vez que o doente havia apresentado um episódio de edema agudo do pulmão, em contexto de crise hipertensiva, no dia anterior ao estudo hemodinâmico. É verdade que o cateterismo cardiovascular, que identifica o comportamento hemodinâmico típico destes doentes, tem sido considerado o método padrão (o gold-standard) para o diagnóstico. No entanto, num estudo recente, em que se utilizaram microcatéteres de alta fidelidade para diferenciação entre PC e MCR, o poder predizente dos critérios convencionais de PC foi apenas de 75%. Neste mesmo estudo, verificou-se que um novo critério - systolic area index, o qual estima a existência de interdependência ventricular aumentada quando superior a 1,1 - tem uma sensibilidade de 97% e um poder preditivo de 100% para identificar PC, documentada cirurgicamente8. Todavia, pese embora o estudo com micromanómetros possa conferir maior rigor ao registo das pressões intracavitárias, não parece preferível em relação aos novos métodos de imagem cardíaca, de execução mais fácil, rápidos, incruentos e fiáveis, os quais devem assumir um papel determinante para o diagnóstico dos casos equívocos de pericardite constritiva.
Conflito de interessesOs autores declaram não haver conflito de interesses.