A insuficiência valvular mitral (IM) é a valvulopatia mais comum e começa agora a ser alvo de abordagens percutâneas. O dispositivo MitraClip é virtualmente o único dispositivo com uma experiência considerável, ultrapassando atualmente as 20000 implantações.
ObjetivoDescrever a experiência inicial da terapêutica percutânea da IM com o dispositivo MitraClip.
MétodosDescrevem‐se os primeiros seis casos de MitraClip realizados nesta instituição (idade 58,5±13,1 anos), com IM 4+ de etiologia funcional e insuficiência cardíaca classe III ou IV (n=3) da New York Heart Association (NYHA), sem indicação cirúrgica ou recusados para cirurgia, com um follow‐up médio 290±145 dias avaliado clinicamente pela sobrevivência, classe funcional, teste da marcha dos seis minutos, estudo ecocardiográfico e determinação do proBNP.
ResultadosO sucesso do procedimento (IM ≤2+) foi de 100%, com um tempo de procedimento de 115,8±23,7mins, sem intercorrências intra‐hospitalares, alta entre o 4.° e 8.° dia e uma melhoria consistente no teste da marcha dos seis minutos (329,8±98,42 versus 385,3±106,95m) e da classe funcional (três dos pacientes com melhoria de duas classes funcionais NYHA). Na totalidade do follow‐up (290±145 dias) constatam‐se dois óbitos, em dois dos quatro pacientes que tinham sido considerados para transplantação cardíaca.
ConclusõesO procedimento de implantação do dispositivo MitraClip é seguro, com uma alta taxa de sucesso imediato nos pacientes com IM funcional. A médio prazo o benefício clínico parece esbater‐se ou anular‐se nos pacientes com insuficiência cardíaca mais terminal, nomeadamente nos pacientes a aguardar ou recusados para transplante.
Mitral regurgitation (MR) is the most common valvular disease and has recently become the target of a number of percutaneous approaches. The MitraClip is virtually the only device for which there is considerable experience, with more than 20 000 procedures performed worldwide.
ObjectiveTo describe our initial experience of the percutaneous treatment of MR with the MitraClip device.
MethodsWe describe the first six MitraClip cases performed in this institution (mean age 58.5±13.1 years), with functional MR grade 4+ and New York Heart Association (NYHA) heart failure class III or IV (n=3), with a mean follow‐up of 290±145 days.
ResultsProcedural success (MR ≤2+) was 100%. Total procedure time was 115.8±23.7 min, with no in‐hospital adverse events and discharge between the fourth and eighth day, and consistent improvement in the six‐minute walk test (329.8±98.42 vs. 385.33±106.95 m) and in NYHA class (three patients improved by two NYHA classes). During follow‐up there were two deaths, in two of the four patients who had been initially considered for heart transplantation.
ConclusionIn patients with functional MR the MitraClip procedure is safe, with both a high implantation and immediate in‐hospital success rate. A longer follow‐up suggests that the clinical benefit decreases or disappears completely in patients with more advanced heart disease, namely those denied transplantation or on the heart transplant waiting list.
A insuficiência valvular mitral (IM) – independentemente da sua gravidade – é atualmente a valvulopatia mais comum, com uma prevalência de 1,7%, atingindo os 10% na população com mais de 75 anos1.
Ainda assim, cerca de metade dos pacientes com IM grave não são referenciados para cirurgia, maioritariamente pela sua idade avançada, pelas comorbilidades ou pelo grau de disfunção ventricular esquerda2. Por outro lado, dos pacientes submetidos à cirurgia, apenas em 34‐53%3 é efetuada uma plastia por oposição à implantação duma prótese valvular.
A IM severa conduz, num lapso de tempo variável, a uma disfunção ventricular esquerda e consequente insuficiência cardíaca congestiva. A terapêutica médica, aliviando os sintomas, não altera a progressão da doença, o que se traduz numa mortalidade anual ≥5% na população sintomática4,5.
A IM divide‐se em dois tipos: a anatómica, na qual a disfunção está num dos elementos do aparelho valvular mitral (e.g., anel, folhetos ou cordas), e a funcional, em que a alteração reside numa alteração geométrica e/ou funcional do ventrículo esquerdo que altera a normal relação dos elementos desse aparelho.
Existe um fator adicional que explica a dimensão desta população com IM grave que não é referenciada para cirurgia: o benefício desta na IM funcional permanece controverso. Além de ter uma prevalência 5‐10 vezes superior à IM anatómica ou à estenose aórtica6, a IM funcional não tem uma indicação cirúrgica caucionada pelas guidelines europeias ou americanas: indicação IIb, a não ser que tenha indicação para cirurgia de revascularização miocárdica7. Isto é, um procedimento percutâneo na IM funcional não concorre, em termos fatuais, com a cirurgia.
O tratamento da IM foi, até recentemente, exclusivamente cirúrgico. Contudo, nos últimos anos desenvolveram‐se várias abordagens percutâneas, a mais aceite e consistente é efetuada através da implantação dum sistema de fixação designado por MitraClip (Abbott Laboratories, Abbott Park, IL, EUA).
A abordagem percutânea da IM tem sido efetuada por várias abordagens:
- A)
Anel: esta estrutura, que na realidade é a junção auriculoventricular esquerda1, tem a forma dum D e não é planar, apresentando uma elevação dos segmentos septal e lateral. O objetivo da anuloplastia cirúrgica é a diminuição do diâmetro septal‐lateral em ≥8mm8.
- B)
Folhetos valvulares: o folheto anterior está em continuidade fibrosa com os folhetos coronário esquerdo e não coronário da válvula aórtica e tem uma superfície maior, mas uma base menor – compreende apenas um terço do perímetro do anel – que o folheto posterior. A superfície de ambos os folhetos é cerca de 2,5 vezes a área do orifício valvular e, durante a sua excursão sistólica, coaptam numa altura que em média é de 8mm o que constitui uma «reserva de coaptação» em caso de dilatação do anel1.
- C)
Cordas tendinosas: elementos de conexão entre os folhetos valvulares e a parede livre ventricular via músculos papilares ou diretamente da parede ventricular (cordas basais).
- D)
Geometria ventricular: alterações da geometria ventricular esquerda, isquémicas ou de outra natureza podem produzir disrupções graves na dinâmica de coaptação mitral9. A discinesia pode alterar a orientação das cordas basais produzindo um efeito de repuxamento (tethering) no folheto posterior e a dilatação ventricular pode produzir um movimento apical dos músculos papilares, com um estiramento apical (tenting) dos folhetos e perda de coaptação.
A cirurgia de Alfieri é uma cirurgia para a IM grave por deficiente coaptação dos folhetos e consiste na sutura dos bordos livres dos segmentos médios dos folhetos anterior e posterior (scallops A2 e P2), associada a uma anuloplastia10, configurando a válvula num duplo orifício. Contudo, o mesmo grupo que introduziu esta cirurgia verificou que a omissão da anuloplastia produz muitas vezes um bom resultado hemodinâmico, o que veio a constituir o racional para a intervenção percutânea com MitraClip11.
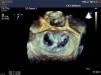
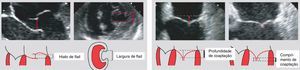
MétodosDum total de 20 doentes referenciados para este procedimento no decurso de dois anos selecionaram‐se seis para início desta terapêutica, após estudo ecocardiográfico transtorácico e transesofágico, Todos os pacientes tinham que ter uma IM 4+ funcional, estarem em classe III ou IV da New York Heart Association (NYHA), terem admissões prévias em insuficiência cardíaca e terem esgotado as opções terapêuticas, cirúrgicas ou outras (e.g., Cardiac Resynchronization Therapy Defibrillator – CRTD). A maioria dos pacientes referenciados estava a ser seguida em consultas de insuficiência cardíaca. Verificados os critérios clínicos, os potenciais candidatos tinham que cumprir os critérios anatómicos (Figura 1) para a implantação deste dispositivo. Embora com a disseminação da técnica se tenha vindo a verificar algum desvio face aos critérios anatómicos inicialmente propostos, estes devem ser escrupulosamente cumpridos nos centros que iniciam este procedimento: 1) o jato de regurgitação deve ser central, 2) comprimento de coaptação >2mm, 3) profundidade de coaptação acima do anel mitral <11mm, 4) se um dos folhetos for flail o hiato e a largura do segmento flail não deve ser ≥10 e ≥15mm, respetivamente. Estes critérios têm como consequência que os pacientes com uma extrema dilatação ventricular esquerda se autoexcluem deste procedimento, uma vez que a dilatação anular produz um grau de separação tal dos folhetos que anatomicamente se torna muito difícil a implantação do clip. Todos os registos ecocardiográficos foram revistos por um Proctor que decidiu da exequibilidade da técnica.
Demograficamente (Tabela 1) esta experiência inicial envolveu um grupo etário claramente baixo (média de idades 58,5±13,1 anos), com uma fração de ejeção (FEj) média de 29±10,36% e um European System for Cardiac Operative Risk Evaluation (EuroSCORE) logístico de 20,06±16,86. Quatro dos pacientes já tinham sido avaliados em consulta de transplantação cardíaca (e um deles recusado para transplante por resistências pulmonares fixas). Três dos pacientes teriam sido excluídos do EVEREST II12 (Endovascular Valve Edge‐to‐Edge Repair Study) por terem uma FEj <25% e/ou por terem uma dimensão telessistólica do ventrículo esquerdo >55mm (média dos pacientes 55,0±7,19mm).
Caracterização demográfica e clínica
| Paciente | Sexo | Idade | Fej (%) | Ever II | LVESdiam | ES log | ES II | Func | Org | IM | NYHA | Etiologia |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | F | 57 | 24 | N | 65 | 12,04 | 3,24 | S | ‐ | IV | IV | Isquémica |
| 2 | M | 62 | 45 | S | 48 | 10,73 | 1,64 | S | ‐ | IV | III | Miocardite |
| 3 | F | 48 | 22 | N | 59 | 12,04 | 4,50 | S | ‐ | IV | IV | Dilatada |
| 4 | M | 49 | 33 | S | 45 | 8,96 | 2,1 | S | ‐ | IV | III | Dilatada |
| 5 | M | 52 | 26 | N | 61 | 19,58 | 2,3 | S | ‐ | IV | IV | Dilatada |
| 6 | M | 83 | 38 | S | 52 | 57,03 | 9,5 | S | ‐ | IV | III | Isquémica |
Ever II: critérios do EVEREST II; ES log: EuroSCORE logístico; ES II: EuroSCORE II; FEj: fração de ejeção; Func: etiologia funcional; LVES diam: diâmetro telessistólico do VE em mm; Org: etiologia orgânica ou degenerativa.
Os pacientes selecionados efetuaram ecocardiograma transtorácico antes do procedimento, à altura da alta, ao 1°, 6° e 12° mês, além de avaliação clínica presencial, determinação de proBNP (pro Brain Natriuretic Peptide) e teste de marcha dos seis minutos na véspera do procedimento e ao 1.°, 6.° e 12.° mês pós‐implantação. Todos os pacientes assinaram o Consentimento Informado.
Definiu‐se sucesso do procedimento a redução da IM para um grau ≤2 na ausência de complicações12.
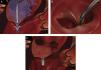
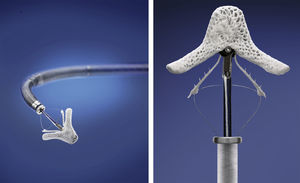
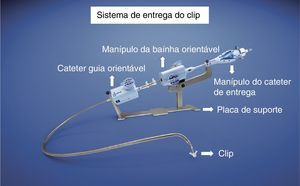
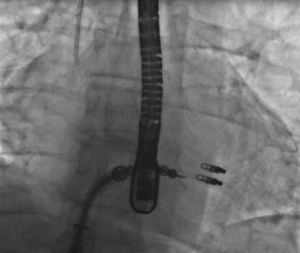
O MitraClip é um clip – em português a analogia mais aproximada seria uma mola de prender roupa – de crómio‐cobalto com 4mm de largura cujas duas extremidades são abertas e fechadas (o ângulo de abertura varia entre 0‐240°) através dum sistema de entrega com vários manípulos (Figuras 2 e 3) que permitem não só a abertura e encerramento dos braços, mas também a rotação e o deslocamento anterior, posterior, lateral e mediano do dispositivo (manobrabilidade tridimensional).
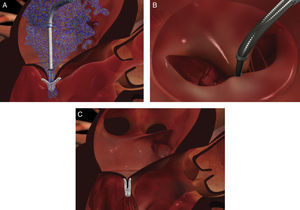
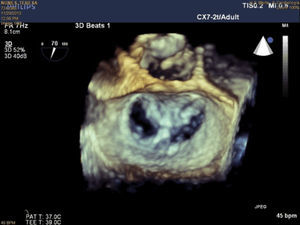
O procedimento é efetuado sob anestesia geral, através duma veia femoral e introdução dum sistema de entrega 24F que é conduzido até à aurícula esquerda após punção transeptal, sob monitorização fluoroscópica e, fundamentalmente, por ecocardiografia transesofágica. A disponibilidade de ecocardiografia tridimensional é imprescindível já que, entre outros, permite a visualização de dois planos ortogonais simultâneos (x‐plane) e assim o fine‐tuning da descida, colocação e preensão nos folhetos. O clip é conduzido até à base do fluxo regurgitante e prendido aos segmentos médios de ambos os folhetos, aproximando‐os, sendo libertado apenas quando a diminuição do jato for considerada adequada (Figura 4). Se não se consegue uma adequada preensão de ambos os folhetos, os braços do clip podem ser novamente abertos, os folhetos libertos e o clip retirado para a aurícula esquerda para novo reposicionamento. O número de clips implantado varia normalmente entre 1 a 4 e, após a sua implantação, forma‐se uma ponte fibrosa entre os dois folhetos constituindo um reforço adicional que diminui o potencial de distensão septal‐lateral.
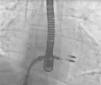
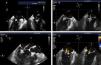
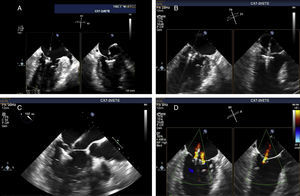
Os procedimentos foram realizados no laboratório de hemodinâmica do Serviço de Cardiologia do Hospital de Santa Marta, em Lisboa, sob anestesia geral, com monitorização ecocardiográfica transesofágica bi e tridimensional (Figura 5), com a presença de três Proctors (cardiologista de intervenção, cardiologista ecocardiografista e técnico do dispositivo) nos dois primeiros casos e com um (técnico do dispositivo) nos restantes. Após a punção transeptal é administrada heparina endovenosa de forma a obtermos um tempo de ativação da coagulação >250”; enquanto o sistema de entrega 22F do MitraClip é posicionado na aurícula esquerda através da bainha 24F colocada na veia femoral direita. Inicialmente colocamos um MitraClip na base do jato de regurgitação dividindo‐o em dois; se estes fossem de pequena dimensão implantaríamos o clip, caso mantivessem uma dimensão razoável adotaríamos uma estratégia de dois clips (Figura 6), implantando o primeiro numa posição mais mediana e o segundo mais lateral (Figura 7), confirmando a inexistência dum gradiente transmitral significativo antes de o libertarmos. Se nos defrontássemos com uma excessiva dificuldade na preensão dos folhetos, induzíamos um breve período de apneia – desconectando por alguns segundos o paciente do ventilador – e/ou um período de bradicárdia mais intensa com administração dum β‐bloqueante de semivida curta (esmolol). Por protocolo o paciente era extubado ainda na sala de hemodinâmica donde saía já acordado, permanecendo na UCI por 24 horas, após o que era transferido para a enfermaria. Dado que cinco pacientes faziam já anticoagulação oral com acenocumarol ou varfine e que o remanescente estava já sob ácido acetilsalicílico, apenas neste se associou clopidogrel durante um mês após o procedimento.
Implantação dum 2.° MitraClip; quando se assume a priori a necessidade dum 2.° clip o 1.° deve ser colocado mais medianamente e o 2.° mais lateralmente. A e B: confirmação em vários planos do posicionamento do MitraClip. C: momento de preensão dos dois folhetos da válvula mitral. D: após a libertação, com os jatos de regurgitação residual.
A análise estatística das variáveis quantitativas destes seis casos foi expressa em média ± DP.
ResultadosNos seis pacientes obteve‐se um sucesso do procedimento de 100% sem qualquer complicação quer durante a intervenção quer durante o seu internamento (média 6,2±1,48 dias).
Apesar de ser um procedimento moroso (115,8±23,7mins), o tempo de fluoroscopia é relativamente baixo (49,2±19,38mins), o que reflete o facto de este ser um procedimento que é sobretudo guiado por ecocardiografia transesofágica (Tabela 2).
Dados do procedimento e tempo de internamento
| Paciente | 1 | 2 | 3 | 4 | 5 | 6 | |
|---|---|---|---|---|---|---|---|
| Tempo de fluoroscopia (min) | 41 | 73 | 35 | 26 | 78 | 42 | 49,2±19,38 |
| Tempo de procedimento (min) | 80 | 155 | 110 | 105 | 135 | 110 | 115,8±23,7 |
| Tempo de dispositivo (min) | 60 | 130 | 85 | 85 | 100 | 90 | 91,7±20,9 |
| Dose acumulada (mGy) | 915 | 2680 | 1487 | 209 | 4456 | 2026 | 1962,2±1362,3 |
| N.° de clips | 1 | 2 | 1 | 1 | 2 | 1 | 1,3±0,47 |
| Dias internamento pós‐procedimento | 6 | 6 | 7 | 4 | 8 | 5 | 6,0±1,29 |
Tempo de procedimento: tempo decorrido entre a punção transeptal e a remoção do cateter guia orientável; Tempo de dispositivo: tempo decorrido entre a entrada do cateter guia orientável na aurícula esquerda através do septo interauricular e o momento em que o cateter de entrega do MitraClip é retirado para o interior do cateter guia orientável
A avaliação ecocardiográfica (Tabelas 3 e 4) revelou uma melhoria dos volumes ventriculares diastólicos (229,5±118,53 versus 182,5±88,24ml) e sistólicos (158,2±100,28 versus 127,2±57,71ml), da FEj (31,3±8,2 versus 37,3±6,11%) e da pressão sistólica da artéria pulmonar (44,5±16,75 versus 41,0±9,97mmHg).
Avaliação ecocardiográfica: evolução da IM e dos volumes ventriculares
| PT | IMb | IM1 | IM6 | IM12 | tdb | td1 | td6 | td12 | tsb | ts1 | ts6 | ts12 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | IV | I | II | I‐II | 443 | 390 | 403 | 337 | 360 | 315 | 312 | 228 |
| 2 | IV | I | II | II | 110 | 119 | 99 | 95 | 60 | 66 | 51 | 71 |
| 3 | IV | III | II‐III | a | 134 | 151 | 139 | a | 105 | 101 | 107 | a |
| 4 | IV | II | I | ‐ | 142 | 136 | 102 | ‐ | 96 | 101 | 76 | ‐ |
| 5 | IV | III | IVb | a | 317 | 262 | a | ‐ | 204 | 181 | a | ‐ |
| 6 | IV | I | ‐ | ‐ | 231 | 160 | ‐ | ‐ | 124 | 100 | ‐ | ‐ |
b, 1, 6 e 12: basal, um mês, 6 meses e 12 meses, respectivamente; IM: insuficiência mitral; PT: paciente; td: volume telediastólico do ventrículo esquerdo em ml; ts: volume telessistólico do ventrículo esquerdo em ml.
Avaliação ecocardiográfica: evolução da fração de ejeção (FEj) e da pressão sistólica da artéria pulmonar (PSAP)
| PT | FEjb | FEJ1 | FEj6 | FEj12 | PSAPb | PSAP1 | PSAP6 | PSAP12 |
|---|---|---|---|---|---|---|---|---|
| 1 | 24 | 17 | 23 | 33 | 33 | 33 | 38 | 33 |
| 2 | 45 | 44 | 44 | 25 | 24 | 35 | 32 | 42 |
| 3 | 22 | 33 | 23 | a | 78 | 58 | 62 | a |
| 4 | 33 | 26 | 25 | ‐ | 42 | 57 | 36 | ‐ |
| 5 | 26 | 19 | a | ‐ | 44 | 33 | a | ‐ |
| 6 | 38 | 37 | ‐ | ‐ | 46 | 40 | ‐ | ‐ |
b, 1, 6 e 12: basal, um mês, 6 meses e 12 meses, respetivamente.
No follow‐up ao mês (Tabela 5) destaca‐se clinicamente uma melhoria do estádio funcional de cinco dos seis pacientes, com regressão de 1‐2 (n=3) estádios da classe funcional NYHA. No follow‐up total constataram‐se três admissões hospitalares (um doente com duas admissões) e dois óbitos, envolvendo dois dos pacientes avaliados em consulta de transplantação cardíaca, um dos quais tinha sido recusado por resistências pulmonares fixas: um outro, o que objetivamente se encontrava num estádio mais terminal de insuficiência cardíaca antes do procedimento de MitraClip, foi readmitido cerca dum mês depois em insuficiência cardíaca congestiva vindo a falecer 84 dias após a admissão, não se tendo encontrado um dador compatível nesse lapso de tempo. Este foi, aliás, o único paciente que revelou um aumento substancial do proBNP ao mês de follow‐up; todos os outros demonstraram uma diminuição deste parâmetro laboratorial (557,8±376,73 versus 494,2±249,5ng/L). O segundo paciente, recusado para transplante, teve duas breves admissões hospitalares nos primeiros seis meses (antes da implantação do MitraClip a frequência de admissões era virtualmente mensal), tendo vindo a falecer em ambulatório ao 9° mês por morte súbita.
Follow‐up clínico e laboratorial
| Pt | proBNP pré | proBNP 1 mês | proBNP 6 meses | proBNP ano | TM pré | TM 1 mês | TM 6 meses | TM ano | NYHA basal | NYHA um mês | NYHA 6 meses | NYHA ano |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 724 | 632 | 477 | 506 | 310 | 390 | 487 | 472 | IV | II | II | II |
| 2 | 240 | 91 | 171 | 623 | 450 | 417 | 500 | 488 | III | I | I | II |
| 3 | 1226 | 1080 | 884 | ‐ | 264 | 325 | 340 | ‐ | IV | II | III | a |
| 4 | 276 | 275 | 198 | ‐ | 477 | 500 | 500 | ‐ | III | II | II | ‐ |
| 5 | 227 | 3123 | a | ‐ | 259 | 287 | a | ‐ | IV | IV | a | ‐ |
| 6 | 323 | 260 | ‐ | ‐ | 219 | 225 | ‐ | ‐ | III | II | ‐ | ‐ |
NYHA: classe de insuficiência cardíaca segundo a New York Heart Association; TM: Teste da marcha dos 6 minutos.
O teste da marcha ao mês revelou uma melhoria em todos os pacientes (329,8±98,42 versus 385,33±109,95m). Os quatro pacientes vivos no follow‐up total (290±140 dias) mantêm uma melhoria da classe funcional em um ou dois estádios (Tabela 5).
DiscussãoOs seis casos descritos constituem a nossa experiência inicial com o MitraClip. Este número representa, a par dum ainda curto follow‐up e da não adjudicação das avaliações ecocardiográficas a um laboratório independente, a principal limitação deste artigo e impede, per se, quaisquer generalizações. Ainda assim, o dado que mais ressalta é a segurança deste tipo de intervenção.
O início deste procedimento ocorreu após cerca de dois anos de seleção ativa de doentes, incluindo estudo detalhado da anatomia mitral por ecocardiografia transtorácica e transesofágica, havendo atualmente uma lista de oito pacientes em lista de espera, todos com IM grave e clínica de insuficiência cardíaca. A experiência mundial entretanto acumulada com este dispositivo parece demonstrar que numa fase inicial de experiência apenas um em cada três doentes referenciados para MitraClip é considerado adequado.
Este dispositivo tem marca CE desde 2008, mas o ensaio que esteve na base da aceitação pela FDA em 2013 foi o EVEREST II, que aleatorizou 279 doentes com IM 3+ ou 4+ para MitraClip versus cirurgia (reparação ou substituição). A randomização foi de 2:1, isto é, dois pacientes para Mitraclip para um referenciado para cirurgia. Os endpoints primários compostos foram divididos em eficácia e em segurança; o primeiro englobava ausência de morte, ausência de cirurgia por disfunção valvular mitral ou ausência de IM 3+ ou 4+ aos 12 meses; o segundo os eventos adversos major aos 30 dias.
Na eficácia demonstrou‐se uma taxa de 55% no grupo do MitraClip versus 73% na cirurgia (p=0,007), com uma mortalidade de 6% em ambos os grupos, cirurgia por disfunção mitral 20 versus 2% e IM 3+ ou 4+ 21 versus 20%. No endpoint de segurança o resultado foi de 15 versus 48% (p <0,001). Aos 12 meses ambos os grupos tinham diminuições nos volumes ventriculares, melhoria da classe funcional da NYHA e nos índices de qualidade de vida.
Em 23% (n=41) dos pacientes submetidos a MitraClip verificou‐se que mantinham uma IM 3+ ou 4+ antes da alta, tendo 28 sido referenciados para cirurgia. Dos pacientes submetidos inicialmente a cirurgia, 14% foram submetidos à implantação de prótese valvular e 86% a reparação mitral.
A transfusão de ≥2 unidades de sangue – fator com grande influência no prognóstico a longo prazo13 – constituiu o maior determinante dos eventos adversos major aos 30 dias. Contudo, mesmo excluindo estes, a taxa de eventos adversos permaneceu inferior no grupo do MitraClip.
Dois subgrupos do MitraClip revelaram uma eficácia não inferior à cirurgia: regurgitação mitral funcional e pacientes com ≥70 anos. Os dados entretanto publicados do follow‐up de quatro anos do EVEREST II revelam uma sobrevivência de 83% no grupo percutâneo e de 82% no grupo cirúrgico, além de ausência de diferença significativa no número de pacientes com IM 3+ e 4+14. A eficácia e segurança deste dispositivo, comparada com a terapêutica médica em pacientes de alto risco, foram entretanto confirmadas pelos registos europeus ACCESS‐EU15 e alemão TRAnscatheter Mitral valve Interventions (TRAMI))16. Com o mesmo objetivo, isto é, comparando o MitraClip com o standard‐of‐care da terapêutica médica, mas já sob a forma de ensaio aleatorizado, foram lançados nos EUA o estudo Clinical Outcomes Assessment of the MitraClip Percutaneous Therapy for Extremely High‐Surgical_Risk Patients (COAPT) e na Europa A Randomized Study of the MitraClip Device of Heart Failure Patients with Clinically Significant Functional Mitral Regurgitation (RESHAPE‐HF).
O dado demográfico que mais ressalta da nossa série é o baixo escalão etário (apenas um octogenário; média de idades 58,5±13,1 anos), o que é fundamental para determinar um EuroSCORE logístico de 20,06±16,86. Atendendo à importância da idade na determinação deste preditor de risco, a situação real destes casos poderá estar subestimada, como o parecem provar os dois óbitos não relacionáveis com o procedimento nos 12 meses subsequentes. Esta opção teve por base a intenção de disponibilizar este dispositivo a um grupo com uma maior sobrevida expectável, no intuito de retirar o maior benefício possível do procedimento. A escolha de pacientes já avaliados em consulta de transplantação cardíaca, por natureza mais jovens, pretendeu adiar substancialmente – idealmente por anos – a entrada em lista de espera de dador. Os resultados obtidos sugerem, porém, que alguns destes pacientes já estarão muito no extremo da história da natural da doença para virem a retirar benefício. A seleção dos pacientes constitui, de resto, o elemento mais importante já que o MitraClip existe para melhorar os sintomas e a evidência atual revela que em cerca de 25% dos casos não existe alívio sintomático com o MitraClip pelo que é importante tentar definir pré implantação quais os pacientes que não irão obter qualquer benefício do procedimento.
A análise de outras séries com predomínio de IM funcional17, incluindo o maior registo europeu e o que porventura mais se aproxima da nossa realidade, o ACCESS‐EU15, revelam que 72‐83% dos pacientes que atingem o ano de follow‐up mantêm‐se com IM ≤2+ e 79‐83% permanecem em classe I ou II da NYHA. O ACCESS‐EU revela um internamento um pouco superior ao nosso (7,7±8,2 dias, incluindo 2,5±6,5 dias na UCI), com uma melhoria consistente, tal como nos nossos casos, dos parâmetros ecocardiográficos e do teste da marcha dos seis minutos, cujo ganho médio de cerca de 60 metros é, aliás, semelhante ao da nossa série (55m). As séries europeias têm tempos de internamento superiores às americanas, cuja média é de cerca de três dias.
Em termos históricos houve uma divergência na abordagem norte‐americana e europeia. O EVEREST I18 e II são estudos americanos e a credibilidade inicial do MitraClip advém destes ensaios. Envolveram pacientes que teriam que ser também candidatos cirúrgicos. Contudo, a Europa interessou‐se sobretudo pelos pacientes que, a priori, seriam recusados para esses ensaios, isto é, pelos pacientes com IM funcional severa e insuficiência cardíaca congestiva, não considerados para cirurgia, muitos deles non‐responders da terapêutica de ressincronização, a maioria dos quais seguidos em consultas de insuficiência cardíaca e alguns, como foram aliás quatro dos nossos pacientes, recusados ou em listas de pré‐transplante. Isto é, os europeus posicionaram o MitraClip como um procedimento não concorrencial da cirurgia, num grupo de pacientes que não tinha alternativa não farmacológica. Neste sentido e contrariamente ao EVEREST II, em que 73% dos pacientes randomizados apresentavam uma IM degenerativa, todos os nossos seis casos tinham uma etiologia funcional. Deste facto decorre que, contrariamente ao que aconteceu na implantação de próteses aórticas por via percutânea, a possibilidade duma guerra de território (turf war) com a cirurgia é virtualmente inexistente.
Existem dois grupos que se destacam como particularmente atraentes para um procedimento de MitraClip: os pacientes com uma calcificação extensa do anel, uma vez que esta calcificação pode funcionar como um anel protésico em termos de sustentabilidade e impedir uma dilatação progressiva do anel, e os doentes com IM funcional severa com insuficiência cardíaca refratária à terapêutica farmacológica e de ressincronização (non‐responders)19.
Apesar do sucesso e disseminação deste procedimento, existem várias limitações potenciais20 desta abordagem: 1) o MitraClip reproduz duma forma incompleta a cirurgia de Alfieri ao não intervir no anel, o que poderá explicar a médio ou longo prazo o reaparecimento duma IM importante; 2) a quantificação da IM – sobretudo a residual após implantação do clip – durante um procedimento com anestesia geral nem sempre é fácil, mas aqui o problema é comum à cirurgia; 3) o potencial de substituirmos uma IM por uma estenose mitral, embora até à data não existam casos descritos21; 4) ausência de informação de durabilidade e eficácia a longo prazo.
Entretanto, com a generalização deste procedimento, os critérios anatómicos iniciais começam a ser expandidos com a publicação de casos de IM excêntrica e de variações à técnica inicial proposta (e.g., the zipping procedure, com implantação de quatro ou cinco clips).
Além do MitraClip existe um crescente número de abordagens da IM por via percutânea, algumas das quais em fase ativa de implantação. Estes dispositivos dividem‐se em duas grandes classes conforme atuem no anel ou noutro dos componentes do aparelho valvular mitral.
Na maioria das cirurgias da IM procede‐se a uma intervenção sobre os dois principais componentes valvulares: folhetos e anel. Não é pois de estranhar a extensa investigação sobre intervenções percutâneas no anel, que aliás antecede o desenvolvimento do MitraClip.
Existem duas formas de anulopastia percutânea, a indireta e a direta. O Carillon Mitral Contour System (Cardiac Dimensions) é um dispositivo de anuloplastia indireta, através do seio coronário, composto por duas âncoras de nitinol nas extremidades unidas por um elemento central também de nitinol. Envolve um cateter de entrega 9F, com acesso pela veia jugular interna e exige um movimento de tensão manual de 4‐5cm antes da libertação final, sendo o procedimento monitorizado quer com ecocardiografia transesofágica (grau de IM) quer sob coronariografia esquerda (exclusão de compressão coronária). Atualmente é o único dispositivo de anuloplastia percutâneo aprovado na União Europeia.
Contrariamente aos devices de anulopastia indireta, feita através do seio coronário, existem abordagens de anuloplastia direta em que se acede diretamente ao anel, tal como a técnica cirúrgica. Mais complexa do que a abordagem pelo seio coronário, o acesso é feito retrogradamente pela artéria femoral, colocando‐se o cateter no ventrículo esquerdo por baixo do folheto posterior, procedendo‐se à aplicação duma espécie de âncoras em volta do anel, unidas por uma sutura. A tensão exercida nesta sutura aproxima as âncoras, diminuindo assim a circunferência do anel (sistema Mitralign). Outro sistema de anuloplastia direta é o Cardioband, que utiliza um acesso transeptal e tem sido utilizado exclusivamente na IM funcional.
Dado o potencial dos pacientes submetidos a MitraClip virem a médio ou a longo prazo a refazerem o grau original de IM, a associação dum procedimento de anuloplastia parece conceptualmente atrativa. Esta associação reproduziria com maior precisão o procedimento cirúrgico. Este parece ser o conceito mais promissor22 enquanto se desenvolve uma prótese mitral percutânea para implantação numa válvula mitral nativa.
ConclusãoA nossa experiência inicial com o dispositivo MitraClip confirmou a extrema segurança do procedimento num grupo de pacientes com insuficiência cardíaca e IM funcional 4+ não considerados para cirurgia, três dos quais teriam sido excluídos do EVEREST II e quatro também já avaliados em consulta de pré‐transplante.
O curto follow‐up impede uma adequada análise da eficácia, mas a ausência de reintervenção, cirúrgica ou não, a melhoria da classe funcional, dos volumes ventriculares e do teste da marcha dos seis minutos e a regressão consistente do valor de proBNP sugere que esta não é despicienda. Contudo, a implantação de MitraClip em pacientes já avaliados em consulta de transplantação parece não alterar a história natural da doença.
Responsabilidades éticasProteção dos seres humanos e animaisOs autores declaram que os procedimentos seguidos estavam de acordo com os regulamentos estabelecidos pelos responsáveis da Comissão de Investigação Clínica e Ética e de acordo com os da Associação Médica Mundial e da Declaração de Helsinki.
Confidencialidade dos dadosOs autores declaram que não aparecem dados de pacientes neste artigo.
Direito à privacidade e consentimento escritoOs autores declaram que não aparecem dados de pacientes neste artigo.
Conflito de interessesOs autores declaram não haver conflito de interesses.