A Síndrome da Apneia do Sono (SAS) é uma doença respiratória prevalente, com expressão marcada na população com doença cardiovascular. O diagnóstico é baseado na polissonografia. Nos doentes com dispositivos eletrónicos cardíacos (DEC), a prevalência de SAS pode atingir 60%. O objetivo deste estudo foi avaliar o valor dos DEC no rastreio de SAS.
MétodosEstudo prospetivo que incluiu doentes com DEC com algoritmo de apneia do sono. Foi ativada a função de resposta em frequência e realizada a poligrafia simplificada. Foram recolhidos os dados do dispositivo no dia em que foi realizada a poligrafia.
ResultadosA amostra incluiu 29 doentes, com uma idade média de 76,1 anos, 71,4% do género masculino. A prevalência de SAS foi de 77%. Para SAS grave a concordância entre a polissonografia e o pacemaker foi de Kappa = 0,54 (p = 0,001), IC 95% (0,28, 0,81) (concordância moderada); para SAS moderada a grave, a concordância foi de Kappa = 0,73 (p < 0,001), IC 95% (0,49, 0,976) (concordância substancial). Para SAS grave obtiveram‐se: sensibilidade 60%, especificidade de 100%, valor preditivo positivo de 100%, valor preditivo negativo de 60% e acurácia diagnóstica de 75%; para SAS moderada a grave: sensibilidade de 90%, especificidade de 83%, valores preditivo positivo de 90% e negativo de 87,5%, com acurácia diagnóstica de 87,5%.
ConclusãoA SAS é altamente prevalente nos portadores de DEC. Os valores obtidos através destes dispositivos apresentam uma correlação positiva forte com o índice de Apneia‐Hipopneia, o que faz deles uma boa ferramenta de rastreio de SAS grave.
Sleep Apnea Syndrome (SAS) is a prevalent respiratory disease with marked expression in the population with cardiovascular disease. The diagnosis is based on polysomnography. In patients with cardiac implantable electronic devices (CIED), the prevalence of SAS may reach 60%. The objective of this study was to evaluate the value of DEC in the SAS screening.
MethodsProspective study that included patients with CIED with sleep apnea algorithm. The frequency response function was activated and simplified polygraphy was performed. The data of the device were collected on the day of the polygraph.
ResultsThe sample included 29 patients, with a mean age of 76.1 years, 71.4% of the male gender. The prevalence of SAS was 77%. For SAS, the agreement between polysomnography and the Pacemaker was Kappa = 0.54 (p = 0.001), 95% CI (0.28, 0.81) (moderate agreement); for moderate to severe SAS, the agreement was Kappa = 0.73 (p <0.001), 95% CI (0.49, 0.976) (substantial agreement). Severe SAS was obtained: sensitivity 60%, specificity 100%, positive predictive value 100%, negative predictive value 60% and diagnostic accuracy 75%; for moderate to severe SAS: sensitivity of 90%, specificity of 83%, positive predictive values of 90% and negative of 87.5%, with a diagnostic accuracy of 87.5%.
ConclusionSAS is highly prevalent in patients with CIED. The values obtained through these devices have a strong positive correlation with the Apnea‐Hypopnea Índex, which makes them a good tool for the screening of severe SAS.
A Síndrome da Apneia do Sono (SAS) é uma doença respiratória prevalente, provocada por colapsos intermitentes da via aérea, que originam interrupções ou alterações no normal fluxo respiratório durante o sono (apneias ou hipopneias). A soma de apneias e hipopneias por hora permite a determinação do Índice de Apneia‐hipopneia (IAH) e estas associadas a RERAs (respiratory effort‐related arousals), do Índice de distúrbio respiratório (RDI)1.
As apneias podem ser de causa obstrutiva (SAOS), entidade mais prevalente, ou de causa central (CSA), quando o número de eventos de causa central é superior a 50% da totalidade dos eventos respiratórios detetado pelo estudo poligráfico do sono1.
A SAS é uma patologia muito prevalente, havendo estudos que demonstram que a prevalência de IAH > 5 pode atingir os 20% e que a prevalência de IAH>15 pode chegar a afetar mais de 15% da população adulta2. Na população com mais de 70 anos, há registo de uma prevalência de Síndrome de Apneia Obstrutiva do Sono (SAOS) tão alta quando 20%3. No subgrupo de doentes com doença cardiovascular, a SAS pode atingir 47‐83% dos doentes, dependendo da patologia específica4. No caso particular dos doentes portadores de dispositivos eletrónicos cardíacos implantáveis (DECI), a prevalência da SAS pode atingir os 60%5.
O objetivo deste trabalho foi avaliar o valor dos dispositivos eletrónicos cardíacos implantáveis no rastreio da SAS.
MétodosForam incluídos 29 doentes, com dispositivos eletrónicos cardíacos (pacemakers, cardioversores‐desfibrilhadores implantáveis, sistemas de ressincronização cardíaca), implantados entre janeiro de 2013 e janeiro de 2015 com algoritmo de deteção de eventos de apneia/hipopneia de sono (Kora™100DR, Reply™200DR da Livanova; Vitalio™Pacemaker, Incepta™CRTD,CRT‐D, Incepta™CDI e Invive™ CRT‐P).
Foi obtida autorização da Comissão de Ética do Hospital, assim como o consentimento informado dos doentes antes da sua inclusão no estudo.
Foram recolhidos dados demográficos, antropométricos e clínicos dos doentes.
Os dispositivos da Livanova têm o algoritmo SAM (sleep apnea monitoring – monitorização de apneias do sono) que deteta apneias, definidas por período entre dois ciclos respiratórios com dez a 60 segundos de duração, e hipopneias, caraterizadas por uma redução de pelo menos 50% na amplitude de um ciclo respiratório. O algoritmo SAM tem a capacidade de destacar os indivíduos com SAS grave, sendo esses definidos pela presença de mais de 20 eventos por hora (correlação com IAH > 30/hora), de acordo com resultados validados no estudo Dream6.
Os dispositivos da Boston Scientific utilizados têm a capacidade de detetar eventos de apneia e hipopneia através do ApneaScan™ e APScan™, que têm também a capacidade de distinguir os pacientes com SAS grave, utilizando para isso um valor cut‐off de 30 (correlacionado com IAH > 30). Os doentes realizaram poligrafia simplificada com o equipamento ApneaLink plustm (Resmed Corporation, Powaym Calif), capacitado de sensor de esforço, uma cânula de fluxo nasal e oxímetro, com monitorização cardiopulmonar, quantificando‐se os eventos de apneia e hipopneia, de roncopatia e presença de padrão respiratório de Cheyne‐Stokes (CSB), sempre com monitorização contínua da frequência cardíaca e da SpO2. Os resultados foram avaliados no Serviço de Pneumologia, sempre pela mesma equipa clínica. Definiram‐se como apneias, eventos em que houve ausência de fluxo respiratório com duração igual ou superior a 10 segundos. Foram igualmente definidas hipopneias reduções de 30% na amplitude do fluxo de um ciclo respiratório sempre que acompanhadas por queda de pelo menos 3% na saturação periférica de O2.
O diagnóstico de Síndrome de Apneia do Sono (SAS) foi então estabelecido sempre que se constatou um IAH superior a cinco eventos/hora, associado a sintomas caraterísticos ou aumento de risco cardiovascular1 ou por um IAH superior a 15/hora, mesmo na ausência de sintomas.
Nos doentes em quem foi confirmado o diagnóstico de SAS e após observação por pneumologia e confirmação nos casos discordantes, por polissonografia tipo 2 (estudo polissonográfico em ambulatório), foi iniciado tratamento por pressão positiva: CPAP, Bi‐nível ou Servoventilação autoadaptativa, de acordo com as recomendações internacionais e com a patologia identificada.
Após confirmação do diagnóstico os doentes foram monitorizados pelo DECI, para avaliação da adesão à terapêutica.
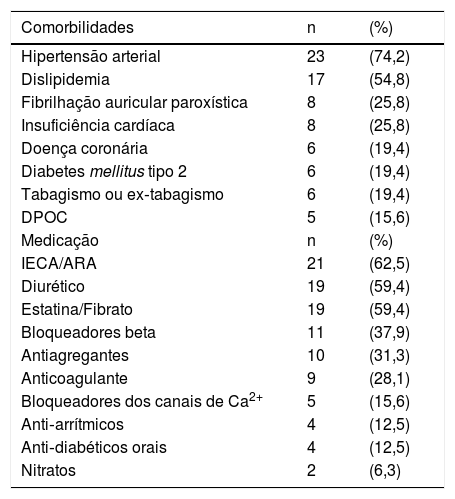
ResultadosForam avaliados 29 doentes, 21 do sexo masculino (71,4%) e 8 do sexo feminino (27,6%), com idade média de 76,1 anos (± 9,8). O índice de massa corporal (IMC) médio foi de 26,8 kg/m2 (± 4,2). A Tabela 1 indica a prevalência de comorbilidades e terapêutica médica dos doentes, sendo a hipertensão arterial (HTA) a patologia mais frequente (74,2%). Na avaliação ecocardiográfica 63,3% dos doentes apresentavam função sistólica ventricular esquerda normal. O dispositivo implantado foi um pacemaker definitivo em 23 doentes (disfunção do nó sinusal em 13 doentes e nos oito restantes distúrbios da condução auriculoventricular), todos de dupla câmara programados em modo DDDR, sistema de ressincronização cardíaca com cardioversor‐desfibrilhador implantável em cinco doentes e um cardioversor‐desfibrilhador implantável de dupla câmara num doente. Em 15 doentes o dispositivo era da empresa Livanova e em 14 doentes da empresa Boston Scientific, havendo portanto uma distribuição equitativa.
Comorbilidades e terapêutica. IECA/ARA – Inibidores da enzima conversora de angiotensina/anatagonistas dos recetores da angiotensina
| Comorbilidades | n | (%) |
|---|---|---|
| Hipertensão arterial | 23 | (74,2) |
| Dislipidemia | 17 | (54,8) |
| Fibrilhação auricular paroxística | 8 | (25,8) |
| Insuficiência cardíaca | 8 | (25,8) |
| Doença coronária | 6 | (19,4) |
| Diabetes mellitus tipo 2 | 6 | (19,4) |
| Tabagismo ou ex‐tabagismo | 6 | (19,4) |
| DPOC | 5 | (15,6) |
| Medicação | n | (%) |
| IECA/ARA | 21 | (62,5) |
| Diurético | 19 | (59,4) |
| Estatina/Fibrato | 19 | (59,4) |
| Bloqueadores beta | 11 | (37,9) |
| Antiagregantes | 10 | (31,3) |
| Anticoagulante | 9 | (28,1) |
| Bloqueadores dos canais de Ca2+ | 5 | (15,6) |
| Anti‐arrítmicos | 4 | (12,5) |
| Anti‐diabéticos orais | 4 | (12,5) |
| Nitratos | 2 | (6,3) |
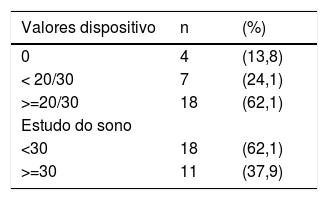
Na análise do dispositivo verificou‐se que quatro doentes não tinham registos de eventos, sete apresentavam eventos com valores < 20‐30/hora e 18 doentes valores > 20‐30/hora (Tabela 2).
No estudo poligráfico 18 doentes (62%) apresentavam valores de IAH < 30/hora, 20 doentes (68,9%) valores > 15/hora e 11 doentes (37,9%) valores de IAH > 30/hora.
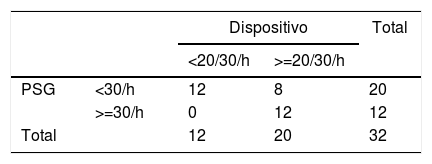
Da análise conjunta dos dados do dispositivo e do estudo poligráfico do sono (Tabela 3), verificou‐se que os 11 casos que na poligrafia tiveram um IAH superior ou igual a 30/hora, tinham todos valores do dispositivo ≥ 20/30/hora. No entanto há sete casos cujo resultado da poligrafia do sono foi inferior a 30/hora e no dispositivo os valores são ≥ 20‐30/hora. A concordância entre a poligrafia e o pacemaker foi de Kappa = 0,54 (p = 0,001), IC 95% (0,28, 0,81) (concordância moderada).
Quando avaliada a concordância dos dois métodos, de acordo com valores de IAH da poligrafia > 15/hora (identificando doentes com SAOS moderada e grave), observa‐se que dos 20 casos com IAH > 15/hora, 18 têm valores do pacemaker ≥ 20/30. Houve dois casos em cujo resultado do estudo poligráfico do sono o IAH foi inferior a 15/hora e no dispositivo os valores são ≥ 20/30/hora. A concordância entre a poligrafia e o dispositivo foi de Kappa = 0,73 (p < 0,001), IC 95% (0,49, 0,976) (concordância substancial).
Quando correlacionamos os valores do dispositivo > 20/30/hora com valores de PSG > 30/hora destacamos: sensibilidade 60%, especificidade de 100%, valor preditivo positivo de 100%, valor preditivo negativo de 60% e acurácia diagnóstica de 75%; para valores de poligrafia > 15/hora: sensibilidade de 90%, especificidade de 83%, valores preditivo positivo de 90% e negativo de 87,5%, com acurácia diagnóstica de 87,5%.
A média do índice de massa corporal não foi significativamente diferente para os indivíduos com poligrafia < 30/h e ≥ 30/h (26,75 versus 26,98, p = 0,886).
DiscussãoAs recomendações internacionais apontam a polissonografia (PSG) como o método de referência para o diagnóstico de pacientes com suspeita de SAS1, sendo que o estudo em ambulatório com monitor portátil também pode ser utilizado em pacientes com uma probabilidade pré‐teste elevada de SAS moderada a grave, sem outras patologias do sono e sem outras comorbilidades médicas major7. A polissonografia regista o número de apneias e hipopneias, determinando um valor IAH e RDI, enquanto que a poligrafia simplificada apenas apresenta o resultado em IAH. Embora a poligrafia simplificada, em regime de ambulatório, tenha minimizado os custos inerentes ao internamento destes doentes, dada a elevada prevalência desta patologia e não exequibilidade através dos cuidados de saúde primários, a lista de espera para a sua realização mantém‐se problemática em muitos centros. A associação significativa da SAS a morbilidade cardiovascular, nomeadamente, hipertensão arterial8–10, síndrome coronária aguda11 ou arritmias, supraventriculares, onde se incluiu a fibrilhação auricular12–15, e mesmo ventriculares14, doença coronária, insuficiência cardíaca e cerebrovascular16–20 impõe a realização deste exame atempadamente quando existem sintomas sugestivos desta síndrome.
Na população de doentes portadores de dispositivos eletrónicos cardíacos, onde a prevalência desta patologia é significativa, a sinalização de eventos de apneia e hipopneias pode ser uma triagem conveniente para a realização de polissonografia.
Cerca de 37,9% dos doentes apresentaram na poligrafia valores de IAH ≥ 30/hora e 68,9% valores > 15/hora, traduzindo uma prevalência elevada de SAS nesta população de doentes, o que está de acordo com os dados encontrados na literatura. A média de idade da amostra em estudo foi de aproximadamente 76,1 ± 9,8 anos, o que pode justificar a prevalência elevada da SAS. Defaye et al. estudaram uma amostra cuja média de idade era de 73,8 ± 19,1, obtendo uma prevalência de 78%3,6.
Curiosamente a média do IMC nos grupos com IAH ≤ 30/hora versus > 30/hora, não foi estatisticamente distinta, reforçando a importância de não desvalorizar sintomas de SAOS em doente com IMC mais baixos.
Verificou‐se uma concordância moderada entre os valores do dispositivo e de IAH > 30/hora na PSG, aumentado esta concordância para um grau substancial, quando se consideram valores de PSG >15/hora, incluindo então doentes com SAS moderada, com implicações terapêuticas. Para valores de IAH na PSG > 30/hora o algoritmo do dispositivo teve uma sensibilidade 60%, especificidade de 100%, valor preditivo positivo de 100%, valor preditivo negativo de 60% e acurácia diagnóstica de 75%; para valores de polissonografia > 15/hora: sensibilidade de 90%, especificidade de 83%, valores preditivo positivo de 90%, valor preditivo negativo de 87,5%, com acurácia diagnóstica de 87,5%. Os valores são concordantes com os reportados na literatura6. Estes dados reforçam o papel dos DEC no rastreio de SAS moderada a grave, com implicações importantes no diagnóstico, tratamento e, consequentemente, qualidade de vida dos doentes.
A elevada prevalência de SAS na população com DEC implantado traz duas implicações: a necessidade de os cardiologistas estarem mais sensibilizados para o rastreio clínico desta síndrome e a confirmação através de polissonografia e no caso específicos dos DEC com algoritmos de deteção, o registo dos valores e o envio desta preciosa informação, muitas vezes subvalorizada, para os cardiologistas assistentes dos doentes. Por outro lado, a possibilidade da monitorização pelo DEC após instituição da terapêutica com CPAP/BiNível/ servoventilação é de extrema utilidade clínica, no sentido de avaliarmos a compliance do doentes à terapêutica instituída para a sua SAS, com estudos a apontarem valores de adesão tão baixos como 65‐80%21.
Embora de forma mais inequívoca, há estudos que sugerem uma otimização da programação do pacemaker no sentido de reduzir os eventos de apneia e hipopneia. Uma metanálise de 2009 avaliou vários ensaios que tinham por objetivos a avaliação da eficácia de um overdrive auricular noturno no tratamento da SAS. Os resultados foram díspares, tendo uma parte dos estudos mostrado eficácia desta estratégia, e outra parte refutado esta possibilidade22,23. Garrigue et al. mostraram que um overdrive auricular noturno 15 batimentos por minuto acima da FC média do doente diminuiu em cerca de 60% o IAH24,25. Pensa‐se que isto ocorra por dois mecanismos diferentes. O primeiro prende‐se com a melhoria associada do output cardíaco e com uma diminuição da congestão pulmonar com consequente regularização da respiração. O outro mecanismo traduz a inversão de um estado hipervagal noturno e estabilização da respiração ao atuar em neurónios aferentes simpáticos14. Este estudo demonstrou, no entanto, que indivíduos sem sinais de IC e sem indicação para dispositivos de tratamento anti‐bradicardizante não beneficiam do overdrive auricular como estratégia terapêutica e que os doentes com Síndrome de Apneia de Sono Central (CSA) eram os que mais beneficiavam desta terapêutica alternativa.
Neste contexto, os dispositivos eletrónicos com capacidade de deteção de eventos de apneia surgem como alternativa mais custo‐efetiva para deteção da SAS e potencialmente para o seu tratamento26,27.
ConclusõesA prevalência de SAS é elevada nos doentes portadores de dispositivos eletrónicos cardíacos. Há vários dispositivos, até agora de duas empresas, com algoritmos capazes de registar eventos de apneias e hipopneias, que devem sinalizar doentes para a realização de polissonografias que permitam a confirmação do diagnóstico. Este estudo demonstrou uma correlação significativa entre os valores registados nos dispositivos e na polissonografia.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.