No enfarte agudo do miocárdio com supradesnivelamento do segmento ST (EAMcST) é inequívoco o benefício do uso de dupla antiagregação plaquetar. O tempo ideal para administrar a dose de carga do inibidor do recetor P2Y12 (DC‐iP2Y12) é pouco consensual e motivo de debate. O principal objetivo do trabalho foi caracterizar a prática usada em Portugal e avaliar o impacto prognóstico da estratégia de administração da DC-iP2Y12, se antes ou durante/após angioplastia primária (AP).
MétodosEstudo multicêntrico, retrospetivo, baseado no Registo Nacional de Síndromes Coronárias Agudas, com inclusão de doentes com EAMcST e AP realizada de 1/10/2010 a 19/09/2017. Estabelecidos dois grupos: DC‐iP2Y12 pré‐AP (PRE‐DC‐iP2Y12) e DC‐iP2Y12 durante ou após AP (CAT‐DC‐iP2Y12).
ResultadosIncluídos 4123 doentes, 66,3% do grupo PRE‐DC‐iP2Y12 e 32,4% do grupo CAT‐DC‐iP2Y12. Numa análise multivariada o uso de PRE‐DC‐iP2Y12 foi preditor de HEMATS (endpoint composto por hemorragia major, transfusão de sangue e queda de hemoglobina (Hb > 2g/dL), queda de Hb>2g/dL e reenfarte. Não se verificaram diferenças entre grupos no MACE (endpoint composto por morte hospitalar, acidente vascular cerebral e reenfarte) e morte hospitalar.
ConclusõesO uso de PRE‐DC‐iP2Y12 associou‐se a um aumento do risco hemorrágico, sendo preditor do outcome composto de hemorragia (HEMATS) e de queda de Hb>2g/dL, sem diferenças significativas na mortalidade e no MACE, o que coloca em questão o benefício desta estratégia.
In ST‐segment elevation myocardial infarction (STEMI) the benefit of dual antiplatelet therapy is unequivocal, but the optimal time to administer the loading dose (LD) of a P2Y12 inhibitor is the subject of debate and disagreement. The main aim of this study was characterize current practice in Portugal and to assess the prognostic impact of P2Y12 inhibitor LD administration strategy, before versus during or after primary percutaneous coronary intervention (PCI).
MethodsThis multicenter retrospective study based on the Portuguese National Registry on Acute Coronary Syndromes included patients with STEMI and PCI performed between October 1, 2010 and September 19, 2017. Two groups were established: LD before PCI (LD‐PRE) and LD during or after PCI (LD‐CATH).
ResultsA total of 4123 patients were included, 66.3% in the LD‐PRE group and 32.4% in the LD‐CATH group. Prehospital use of a P2Y12 inhibitor was a predictor of the composite bleeding endpoint (major bleeding, need for transfusion or hemoglobin [Hb] drop >2g/dl), Hb drop >2g/dl and reinfarction. There were no differences between groups in major adverse events (MAE) (in‐hospital mortality, reinfarction and stroke) or in‐hospital mortality.
ConclusionsPrehospital use of a P2Y12 inhibitor was associated with an increased risk of bleeding, predicting the composite bleeding outcome and Hb drop >2g/dl, with no differences in mortality or MAE, calling into question the benefit of this strategy.
Nos doentes com o diagnóstico de enfarte agudo do miocárdio com supradesnivelamento do segmento ST (EAMcST) é inequívoco o benefício do uso de dupla antiagregação plaquetar com ácido acetilsalicílico (AAS) e um inibidor do recetor P2Y12 (iP2Y12).1,2 Durante vários anos, o iP2Y12 com mais robustez científica e amplamente usado foi o clopidogrel. Com os resultados dos estudos comparativos entre o clopidogrel e o ticagrelor3 e prasugrel4, estes passaram a ser os fármacos de primeira linha no tratamento do EAMcST.1,2
O tempo ideal para administrar a dose de carga do iP2Y12 (DC‐iP2Y12) é um tema pouco consensual e amplamente debatido, sendo o Atlantic (Administration of Ticagrelor in the Cath Lab or in the Ambulance for New ST Elevation Myocardial Infarction to Open the Coronary Artery)5 o único grande estudo randomizado a estudar a questão. O Atlantic concluiu que o uso pré‐hospitalar de ticagrelor é seguro (não aumenta complicações hemorrágicas) mas não apresenta benefício na taxa de reperfusão na angioplastia primária (AP) em comparação com o uso de ticagrelor apenas no laboratório de hemodinâmica (LH). No entanto, a diferença do uso de ticagrelor no LH ou no pré‐hospitalar foi de apenas 31 minutos (min), o que não reflete a realidade da maioria dos países.5
Relativamente ao clopidogrel, a evidência de que o seu uso pré‐hospitalar tenha benefício em comparação com o seu uso apenas no LH é pouco robusta.6–9 Existe apenas um pequeno estudo randomizado que mostra uma tendência para a redução de eventos (reenfarte, revascularização urgente e morte, p = 0,09) com o pré‐tratamento com clopidogrel7, enquanto a restante evidência provém de registos e estudos retrospetivos que mostram uma redução da mortalidade com o pré‐tratamento com clopidogrel.6,8
Com base nestes dados, as atuais recomendações internacionais dão indicação para administrar a DC‐iP2Y12 precocemente, preferencialmente no pré‐hospitalar.1,2
Não se encontrando a prática da vida real refletida nos estudos científicos, é importante verificar nos registos existentes qual será o verdadeiro impacto do pré‐tratamento com a DC‐iP2Y12.
ObjetivoCaracterizar a prática portuguesa no tempo de administração da DC‐iP2Y12, se antes ou durante/após AP, e avaliar o impacto prognóstico de cada uma das estratégias escolhidas. Para avaliar a segurança foi utilizado o endpoint composto Hemats (hemorragia major [definido pela classificação Gusto], necessidade de transfusão de sangue e queda de Hb > 2g/dL) e para avaliar prognóstico utilizado o endpoint composto Mace (mortalidade, reenfarte não fatal e acidente vascular cerebral [AVC]).
MétodosDesenho do estudoEstudo multicêntrico, retrospetivo, descritivo e correlacional baseado no Registo Nacional de Síndromes Coronárias Agudas (RNSCA). Foram incluídos todos os doentes com diagnóstico de EAMcST submetidos a AP e a DC‐iP2Y12 de 1/10/2010 a 19/09/2017. Foram estabelecidos dois grupos, um com doentes com DC‐iP2Y12 efetuada antes da AP (PRE‐DC‐iP2Y12) e outro grupo com doentes que efetuaram DC‐iP2Y12 durante ou após AP (CAT‐DC‐iP2Y12). Foram avaliados preditores para o uso de uma ou outra estratégia e foi avaliado o impacto prognóstico e de segurança consequente de cada estratégia.
Seleção de doentesForam incluídos todos os doentes com ≥18 anos, registados no RNSCA de 1/10/2010 a 19/09/2017, com diagnóstico de EAMcST revascularizados com AP. O diagnóstico de EAMcST foi definido como a presença de dor torácica ou equivalente anginoso nas últimas 48 horas associados a supradesnivelamento do segmento ST em derivações contíguas segundo os critérios definidos nas recomendações europeias1.
Foram excluídos os doentes que não possuíssem os dados necessários para identificar o tempo de administração da DC‐iP2Y12.
Colheita de dadosForam colhidos dados demográficos; antecedentes pessoais relevantes; fatores de risco cardiovascular; localização do EAMcST; meio de transporte para o hospital; local de admissão hospitalar; forma de admissão hospitalar; admissões em hospital sem laboratório de hemodinâmica (LH). Foram calculados os tempos Sintomas‐1.° Contacto Médico (S‐1CM), 1.° Contacto Médico‐Balão (1CM‐B), Sintomas‐Balão (S‐B) e Porta‐Balão (P‐B). Foram avaliados dados do internamento na admissão, dados da coronariografia, fração de ejeção ventricular esquerda (FEVE) e medicação prévia, administrada no internamento e na alta. Foram ainda avaliados efeitos adversos durante o internamento (mortalidade, reenfarte não fatal, acidente vascular cerebral [AVC], Mace [endpoint composto pelas três variáveis anteriores], hemorragia major (definido pela classificação Gusto), necessidade de transfusão de sangue e queda de Hb>2g/dL e Hemats [endpoint composto pelas três variáveis anteriores]).
Endpoints do estudoO endpoint primário do estudo foi avaliar o impacto prognóstico e a segurança de utilizar a DC‐iP2Y12 ante da AP ou durante/após a AP. O prognóstico foi avaliado pelo endpoint composto Mace e a segurança pelo endpoint composto Hemats.
Análise estatísticaFoi efetuada uma análise descritiva das variáveis definidas para a caracterização da amostra. As variáveis contínuas são apresentadas como média e desvio‐padrão. As variáveis categóricas são apresentadas numericamente em percentagem. Foi efetuada uma análise comparativa entre os grupos definidos para cada uma das variáveis, sendo aplicado o teste de qui‐quadrado para as variáveis categóricas e o teste t de Student para as variáveis contínuas. Foi definido um limiar de significância estatística correlacional de 95%, com um p < 0,05. Para apresentação dos preditores para a escolha da estratégia foi utilizado um método de regressão logística, sendo considerado um p < 0,05 para a significância estatística. Para avaliação do prognóstico e segurança foi realizado método de regressão logística incluindo a variável CAT‐DC‐iP2Y12, sendo um OR superior a 1 indicativo que o CAT‐DC‐iP2Y12 é preditor para a ocorrência da variável e um OR inferior a 1 indicativo que o PRE‐DC‐iP2Y12 é preditor para a ocorrência da variável. Nestas análises, o modelo de regressão logística foi ajustado para as diferenças entre grupos para diminuir o impacto da heterogeneidade entre grupos.
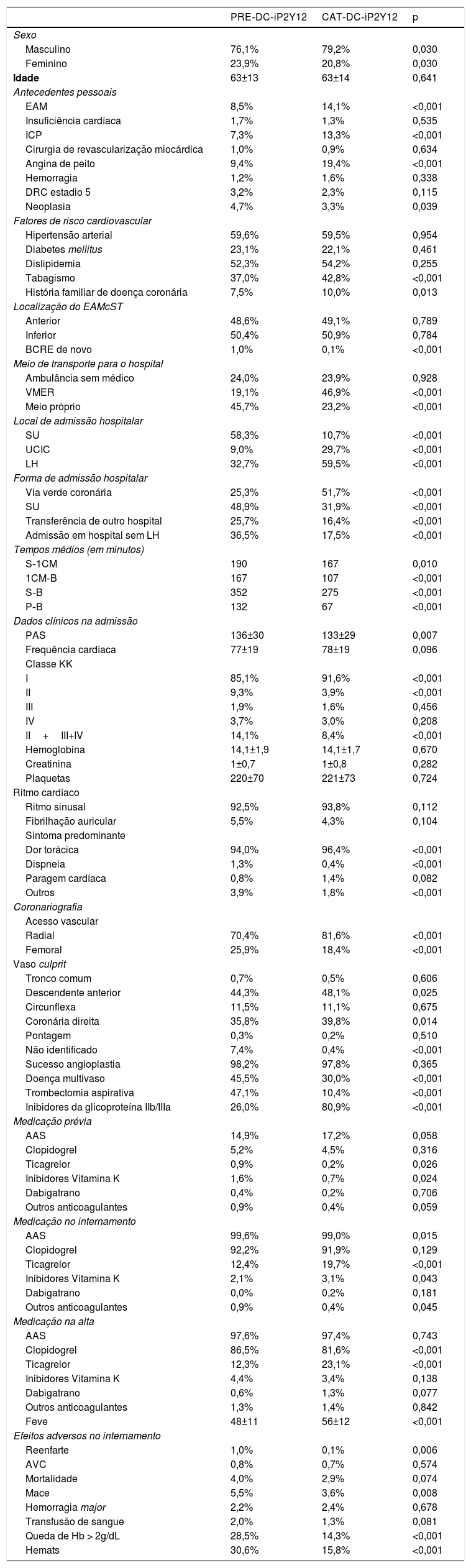
ResultadosAnálise da amostra e comparação entre gruposForam incluídos na seleção do estudo 6757 doentes com o diagnóstico de EAMcST, 5238 submetidos a AP. Destes, 54 (1,0%) foram excluídos por não terem feito DC‐iP2Y12, 3 (0,1%) excluídos por falta de informação relativamente ao uso de DC‐iP2Y12 e 1058 (20,2%) excluídos por falta de informação relativamente ao tempo de administração da DC‐iP2Y12. A amostra final foi de 4123 doentes, 2774 (66,3%) eram do grupo PRE‐DC‐iP2Y12 e 1349 (32,4%) do grupo CAT‐DC‐iP2Y12. A caracterização e a comparação entre grupos encontram‐se descritas na Tabela 1. O sexo masculino é mais prevalente no grupo CAT‐DC‐iP2Y12, sendo a idade sobreponível nos dois grupos. Relativamente aos antecedentes pessoais e fatores de risco vascular, os antecedentes de EAM, intervenção coronária percutânea (ICP), angina de peito, tabagismo e história familiar de doença coronária foram mais frequentes no grupo CAT‐DC‐iP2Y12, enquanto o antecedente de neoplasia foi mais frequente no grupo PRE‐DC‐iP2Y12. O transporte pré‐hospitalar mais frequente no grupo PRE‐DC‐iP2Y12 foi por meio próprio, enquanto no grupo CAT‐DC‐iP2Y12 foi com viatura médica de emergência e reanimação (VMER). O local de admissão preferencial no grupo PRE‐DC‐iP2Y12 foi o serviço de urgência (SU) e o do CAT‐DC‐iP2Y12 a unidade de cuidados intensivos cardíacos ou o LH. A VVC favoreceu o uso de CAT‐DC‐iP2Y12, enquanto uma admissão em hospital sem LH e no SU favoreceu o uso de PRE‐DC‐iP2Y12. A localização de enfarte indeterminado com bloqueio completo de rame esquerdo (BCRE) de novo e a não identificação de um vaso culprit na coronariografia foram mais frequentes no grupo PRE‐DC‐iP2Y12. Os tempos de atraso até à AP foram inferiores no grupo CAT‐DC‐iP2Y12. O sintoma predominante de dor torácica foi mais prevalente no grupo CAT‐DC‐iP2Y12. A taxa de doentes em classe Killip Kimball (KK) II ou superior foi superior no grupo PRE‐DC‐iP2Y12, enquanto a pressão arterial sistólica (PAS) foi mais baixa no grupo CAT‐DC‐iP2Y12. A doença multivaso e a trombectomia aspirativa foram mais frequentes no grupo PRE‐DC‐iP2Y12 e o aceso radial e o uso de inibidores da glicoproteína IIb/IIIa mais frequentes no grupo CAT‐DC‐iP2Y12. O sucesso da AP foi sobreponível nos dois grupos. Na medicação usada, tanto no internamento, como na alta, houve uma maior preferência pelo ticagrelor nos doentes do grupo CAT‐DC‐iP2Y12, enquanto os doentes com terapêutica prévia com ticagrelor e inibidores da vitamina K receberam mais frequentemente PRE‐DC‐iP2Y12.
Caracterização e comparação entre grupos
| PRE‐DC‐iP2Y12 | CAT‐DC‐iP2Y12 | p | |
|---|---|---|---|
| Sexo | |||
| Masculino | 76,1% | 79,2% | 0,030 |
| Feminino | 23,9% | 20,8% | 0,030 |
| Idade | 63±13 | 63±14 | 0,641 |
| Antecedentes pessoais | |||
| EAM | 8,5% | 14,1% | <0,001 |
| Insuficiência cardíaca | 1,7% | 1,3% | 0,535 |
| ICP | 7,3% | 13,3% | <0,001 |
| Cirurgia de revascularização miocárdica | 1,0% | 0,9% | 0,634 |
| Angina de peito | 9,4% | 19,4% | <0,001 |
| Hemorragia | 1,2% | 1,6% | 0,338 |
| DRC estadio 5 | 3,2% | 2,3% | 0,115 |
| Neoplasia | 4,7% | 3,3% | 0,039 |
| Fatores de risco cardiovascular | |||
| Hipertensão arterial | 59,6% | 59,5% | 0,954 |
| Diabetes mellitus | 23,1% | 22,1% | 0,461 |
| Dislipidemia | 52,3% | 54,2% | 0,255 |
| Tabagismo | 37,0% | 42,8% | <0,001 |
| História familiar de doença coronária | 7,5% | 10,0% | 0,013 |
| Localização do EAMcST | |||
| Anterior | 48,6% | 49,1% | 0,789 |
| Inferior | 50,4% | 50,9% | 0,784 |
| BCRE de novo | 1,0% | 0,1% | <0,001 |
| Meio de transporte para o hospital | |||
| Ambulância sem médico | 24,0% | 23,9% | 0,928 |
| VMER | 19,1% | 46,9% | <0,001 |
| Meio próprio | 45,7% | 23,2% | <0,001 |
| Local de admissão hospitalar | |||
| SU | 58,3% | 10,7% | <0,001 |
| UCIC | 9,0% | 29,7% | <0,001 |
| LH | 32,7% | 59,5% | <0,001 |
| Forma de admissão hospitalar | |||
| Via verde coronária | 25,3% | 51,7% | <0,001 |
| SU | 48,9% | 31,9% | <0,001 |
| Transferência de outro hospital | 25,7% | 16,4% | <0,001 |
| Admissão em hospital sem LH | 36,5% | 17,5% | <0,001 |
| Tempos médios (em minutos) | |||
| S‐1CM | 190 | 167 | 0,010 |
| 1CM‐B | 167 | 107 | <0,001 |
| S‐B | 352 | 275 | <0,001 |
| P‐B | 132 | 67 | <0,001 |
| Dados clínicos na admissão | |||
| PAS | 136±30 | 133±29 | 0,007 |
| Frequência cardíaca | 77±19 | 78±19 | 0,096 |
| Classe KK | |||
| I | 85,1% | 91,6% | <0,001 |
| II | 9,3% | 3,9% | <0,001 |
| III | 1,9% | 1,6% | 0,456 |
| IV | 3,7% | 3,0% | 0,208 |
| II+III+IV | 14,1% | 8,4% | <0,001 |
| Hemoglobina | 14,1±1,9 | 14,1±1,7 | 0,670 |
| Creatinina | 1±0,7 | 1±0,8 | 0,282 |
| Plaquetas | 220±70 | 221±73 | 0,724 |
| Ritmo cardíaco | |||
| Ritmo sinusal | 92,5% | 93,8% | 0,112 |
| Fibrilhação auricular | 5,5% | 4,3% | 0,104 |
| Sintoma predominante | |||
| Dor torácica | 94,0% | 96,4% | <0,001 |
| Dispneia | 1,3% | 0,4% | <0,001 |
| Paragem cardíaca | 0,8% | 1,4% | 0,082 |
| Outros | 3,9% | 1,8% | <0,001 |
| Coronariografia | |||
| Acesso vascular | |||
| Radial | 70,4% | 81,6% | <0,001 |
| Femoral | 25,9% | 18,4% | <0,001 |
| Vaso culprit | |||
| Tronco comum | 0,7% | 0,5% | 0,606 |
| Descendente anterior | 44,3% | 48,1% | 0,025 |
| Circunflexa | 11,5% | 11,1% | 0,675 |
| Coronária direita | 35,8% | 39,8% | 0,014 |
| Pontagem | 0,3% | 0,2% | 0,510 |
| Não identificado | 7,4% | 0,4% | <0,001 |
| Sucesso angioplastia | 98,2% | 97,8% | 0,365 |
| Doença multivaso | 45,5% | 30,0% | <0,001 |
| Trombectomia aspirativa | 47,1% | 10,4% | <0,001 |
| Inibidores da glicoproteína IIb/IIIa | 26,0% | 80,9% | <0,001 |
| Medicação prévia | |||
| AAS | 14,9% | 17,2% | 0,058 |
| Clopidogrel | 5,2% | 4,5% | 0,316 |
| Ticagrelor | 0,9% | 0,2% | 0,026 |
| Inibidores Vitamina K | 1,6% | 0,7% | 0,024 |
| Dabigatrano | 0,4% | 0,2% | 0,706 |
| Outros anticoagulantes | 0,9% | 0,4% | 0,059 |
| Medicação no internamento | |||
| AAS | 99,6% | 99,0% | 0,015 |
| Clopidogrel | 92,2% | 91,9% | 0,129 |
| Ticagrelor | 12,4% | 19,7% | <0,001 |
| Inibidores Vitamina K | 2,1% | 3,1% | 0,043 |
| Dabigatrano | 0,0% | 0,2% | 0,181 |
| Outros anticoagulantes | 0,9% | 0,4% | 0,045 |
| Medicação na alta | |||
| AAS | 97,6% | 97,4% | 0,743 |
| Clopidogrel | 86,5% | 81,6% | <0,001 |
| Ticagrelor | 12,3% | 23,1% | <0,001 |
| Inibidores Vitamina K | 4,4% | 3,4% | 0,138 |
| Dabigatrano | 0,6% | 1,3% | 0,077 |
| Outros anticoagulantes | 1,3% | 1,4% | 0,842 |
| Feve | 48±11 | 56±12 | <0,001 |
| Efeitos adversos no internamento | |||
| Reenfarte | 1,0% | 0,1% | 0,006 |
| AVC | 0,8% | 0,7% | 0,574 |
| Mortalidade | 4,0% | 2,9% | 0,074 |
| Mace | 5,5% | 3,6% | 0,008 |
| Hemorragia major | 2,2% | 2,4% | 0,678 |
| Transfusão de sangue | 2,0% | 1,3% | 0,081 |
| Queda de Hb > 2g/dL | 28,5% | 14,3% | <0,001 |
| Hemats | 30,6% | 15,8% | <0,001 |
Legenda: PRE‐DC‐iP2Y12: Dose de carga do inibidor do recetor P2Y12 antes da coronariografia; CAT‐DC‐iP2Y12: Dose de carga do inibidor do recetor P2Y12 durante/após coronariografia; EAM: Enfarte agudo do miocárdio; ICP: Intervenção coronária percutânea; DRC: Doença renal crónica; EAMcST: Enfarte agudo do miocárdio cm supradesnivelamento do segmento ST; BCRE: Bloqueio completo de remo esquerdo; VMER: Viatura médica de emergência e reanimação; SU: Serviço de urgência; UCIC: Unidade de cuidados intensivos cardíacos; LH: Laboratório de hemodinâmica; S‐1CM: Tempo sintomas‐1.° contacto médico; 1CM‐B: Tempo 1.° contacto médico‐balão; S‐B: Tempo sintomas‐balão; P‐B: Tempo porta‐balão; PAS: Pressão arterial sistólica; KK: Killip‐Kimball; AAS: Ácido acetilsalicílico; Feve: Fração de ejeção do ventrículo esquerdo; AVC: Acidente vascular cerebral
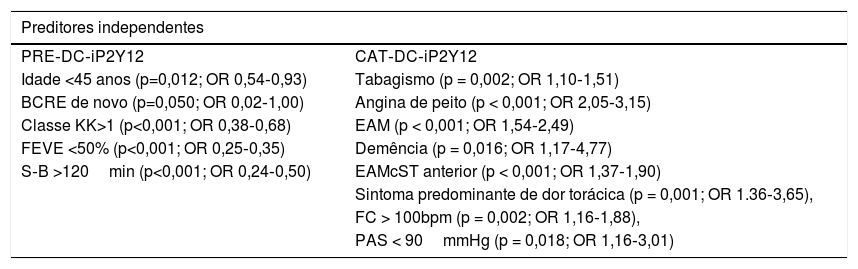
Para o uso de PRE‐DC‐iP2Y12 foram identificados como preditores a idade < 45 anos, a presença de enfarte de localização indeterminada com BCRE de novo, classe KK > 1, Feve < 50% e tempo S‐B > 120min. Para o uso de CAT‐DC‐iP2Y12 foram identificados como preditores antecedentes de tabagismo, angina de peito, EAM e demência, localização de EAMcST anterior, sintoma predominante de dor torácica, frequência cardíaca (FC) >100/min e PAS <90mmHg (Tabela 2).
Preditores para a escolha da estratégia PRE‐DC‐iP2Y12 ou CAT‐DC‐iP2Y12
| Preditores independentes | |
|---|---|
| PRE‐DC‐iP2Y12 | CAT‐DC‐iP2Y12 |
| Idade <45 anos (p=0,012; OR 0,54‐0,93) | Tabagismo (p = 0,002; OR 1,10‐1,51) |
| BCRE de novo (p=0,050; OR 0,02‐1,00) | Angina de peito (p < 0,001; OR 2,05‐3,15) |
| Classe KK>1 (p<0,001; OR 0,38‐0,68) | EAM (p < 0,001; OR 1,54‐2,49) |
| FEVE <50% (p<0,001; OR 0,25‐0,35) | Demência (p = 0,016; OR 1,17‐4,77) |
| S‐B >120min (p<0,001; OR 0,24‐0,50) | EAMcST anterior (p < 0,001; OR 1,37‐1,90) |
| Sintoma predominante de dor torácica (p = 0,001; OR 1.36‐3,65), | |
| FC > 100bpm (p = 0,002; OR 1,16‐1,88), | |
| PAS < 90mmHg (p = 0,018; OR 1,16‐3,01) |
Legenda: PRE‐DC‐iP2Y12: Dose de carga do inibidor do recetor P2Y12 antes da coronariografia; CAT‐DC‐iP2Y12: Dose de carga do inibidor do recetor P2Y12 durante/após coronariografia; BCRE: Bloqueio completo de remo esquerdo; KK: Killip‐Kimball; Feve: Fração de ejeção do ventrículo esquerdo; S‐B: Tempo sintomas‐balão; EAM: Enfarte agudo do miocárdio; EAMcST: Enfarte agudo do miocárdio cm supradesnivelamento do segmento ST; FC: Frequência cardíaca; PAS: Pressão arterial sistólica.
Nos dados de prognóstico, em comparação simples, os doentes do grupo PRE‐DC‐iP2Y12 tiveram uma Feve inferior (48 ± 11 versus 56 ± 12, p < 0,001), mais reenfarte (1,0% versus 0,1%, p = 0,006), mais Mace (5,5% versus 3,6%, p = 0,008), mais queda de Hb > 2g/dL (28,5% versus 14,3%, p < 0,001) e mais Hemats (30,6% versus 15,8, p < 0,001). Não se verificaram diferenças na mortalidade intra‐hospitalar, AVC, hemorragia major e necessidade de transfusão.
Preditores para os endpoints de prognóstico e segurançaForam identificados como preditores de Mace o sexo feminino (p = 0,003; OR 1,22‐2,69), idade > 75 anos (p < 0,001; OR 1,78‐3,84), FC > 100/min (p = 0,014; OR 1,12‐2,76); PAS < 90mmHg (p < 0,001; OR 1,94‐5,63), classe KK > 1 (p < 0,001; OR 1,76‐4,03), Feve < 40% (p < 0,001; OR 2,68‐6,33) e doença multivaso (p = 0,002; OR 1,24‐2,69). O tempo de administração da DC‐iP2Y12 não foi preditor para Mace (p = 0,882; OR 0,60‐1,54).
Foram identificados como preditores de Hemats sintoma predominante de paragem cardíaca (p = 0,005; OR 1,42‐7,60), FC > 100/min (p = 0,001; OR 1,23‐2,12), classe KK >1 (p < 0,001; OR 1,36‐2,33), tempo S‐B >120min (p < 0,001; OR 1,37‐2,65), Feve < 40% (p = 0,031; OR 1,02‐1,64), doença multivaso (p = 0,001; OR 1,15‐1,68) e uso de PRE‐DC‐iP2Y12 (p < 0,001; OR 0,37‐0,58).
Na avaliação dos endpoints individuais o uso de PRE‐DC‐P2Y12 foi ainda preditor de queda de Hb > 2g/dL (p < 0,001; OR 0,32‐0,51), reenfarte (p = 0,03; OR 0,05‐0,88) e IC (p < 0,001; OR 0,39‐0,66). O tempo da DC‐iP2Y12 não foi preditor de hemorragia major (p = 0,311; OR 0,77‐2,25), transfusão de sangue (p = 0,724; OR 0,46‐1,71) e morte (p = 0,652; OR 0,64‐2,02).
DiscussãoDiferenças entre gruposDa análise comparativa dos dois grupos em estudo existe uma grande heterogeneidade nas características demográficas e clínicas basais dos grupos. O grupo PRE‐DC‐iP2Y12 parece possuir, numa análise global, condições que lhe condicionam um pior prognóstico. Analisando os antecedentes, verificámos que no grupo CAT‐DC‐iP2Y12 há maior prevalência de antecedentes que atestam e confirmam o diagnóstico de doença coronária, como o são os antecedentes de EAM, ICP ou angina estável. Este resultado, para os autores, é pouco expectável. Uma maior suspeita clínica de enfarte levar‐nos‐ia, teoricamente, a mais precocemente utilizar a DC‐iP2Y12. Este facto poderá, pelo menos em parte, ser atribuído a uma maior dificuldade de estabelecer o diagnóstico de EAMcST nos doentes com doença coronária e EAM prévios, dada a possível existência de alterações de base no eletrocardiograma10. Quanto ao funcionamento e à eficiência da rede de transporte pré‐hospitalar, verificámos que os doentes do grupo CAT‐DC‐iP2Y12 são mais vezes transportados pela via verde coronária (VVC) e com a VMER e são mais vezes admitidos diretamente no LH sem necessidade de transferências hospitalares, o que lhes confere um benefício prognóstico pela mais atempada AP11,12. Estas diferenças refletem‐se nos tempos até a AP com o tempo S‐B (tempo total de isquemia) a ser significativamente superior nos doentes do grupo PRE‐DC‐iP2Y12, o que lhe confere um pior prognóstico, como comprovado pelas maiores taxas de Mace13. Quando analisamos a escolha do iP2Y12, o prasugrel foi usado em apenas um doente, enquanto o ticagrelor fui usado com mais frequência no grupo CAT‐DC‐iP2Y12, podendo esta diferença ser explicada pela indisponibilidade, durante os primeiros anos da análise, do ticagrelor na VMER. Apesar da maior percentagem de doentes sob ticagrelor prévio no grupo PRE‐DC‐iP2Y12 (não estatisticamente significativa), presumidamente sob dupla antiagregação, foram também estes que mais vezes receberam nova DC‐iP2Y12 pré‐AP, facto pouco expectável, mas que terá pouco impacto nos resultados finais de estudo (trata‐se de < 1% do número total de doentes). Apesar das recomendações indicarem o uso preferencial de ticagrelor ou prasugrel1,2, neste período de estudo, o clopidogrel continuou a ser o iP2Y12 mais utilizado. Na análise aos dados da coronariografia salientamos que os doentes do grupo PRE‐DC‐iP2Y12 utilizaram com menos frequência o acesso radial e têm com mais frequência doença multivaso, dois factores que, mais uma vez, conferem a este grupo consequências prognósticas negativas (adicionalmente o não uso do acesso radial confere um aumento do risco hemorrágico)14–16. Os doentes do grupo PRE‐DC‐iP2Y12 fizeram com muito mais frequência trombectomia aspirativa, o que poderia resultar numa maior taxa de AVC17, situação que não se verificou na nossa amostra. No grupo CAT‐DC‐iP2Y12 foi mais frequente o uso de inibidores da glicoproteína IIb/IIIa, sem que isso aumentasse de forma significativa o número de complicações hemorrágicas. No grupo que fez pré‐tratamento com DC‐iP2Y12 verificou‐se uma percentagem elevada (7,4% versus 0,4%) de doentes com o vaso culprit não identificado, facto provavelmente relacionado com o diagnóstico diferencial com patologias de apresentação clínica semelhante ao EAMcST, como a miocardite ou miocardiopatia de Takotsubo, não associadas a doença coronária. Este grupo de doentes, quando avaliados no LH após visualização da anatomia coronária, já não chegaria a fazer a DC‐iP2Y12, que explicará a diferença observada. O tempo da DC‐iP2Y12 não influenciou a taxa de sucesso da angioplastia, verificando‐se, neste ponto, ausência de benefício do PRE‐DC‐iP2Y12 para melhorar a taxa de sucesso de angioplastia. Por fim, na avaliação prognóstica e de segurança, o grupo PRE‐DC‐iP2Y12 teve uma maior percentagem de eventos, confirmando que as diferenças anteriormente apontadas desfavorecem o prognóstico dos doentes do grupo PRE‐DC‐iP2Y12, no qual se verificaram maiores taxas de reenfarte, Mace, queda de Hb > 2g/dL e Hemats.
Impacto prognóstico da estratégia escolhidaO estudo Atlantic tentou avaliar qual seria o melhor tempo para a DC‐iP2Y125, tratando‐se de um estudo randomizado que englobou 1.875 doentes, divididos em dois grupos para receber ticagrelor no pré‐hospitalar ou no LH. A eficácia foi sobreponível nos dois grupos, medida através da resolução de pelo menos 70% do supradesnivelamento do segmento ST uma hora após a AP e pela presença de fluxo TIMI III após AP. Não se verificaram diferenças na mortalidade, AVC ou hemorragias. A única diferença estatisticamente significativa foi a redução da trombose de stent no grupo que fez ticagrelor no pré‐hospitalar.
Para a utilização do clopidogrel existem apenas alguns registos e um pequeno ensaio randomizado que sugerem um benefício do uso da dose de carga de clopidogrel no pré‐hospitalar.6–8 Um meta‐análise com um total de 37 814 doentes submetidos a angioplastia, mas não obrigatoriamente AP, mostrou que o pré‐tratamento com clopidogrel não alterou a mortalidade e a taxa de hemorragias, mas reduziu o número de eventos trombóticos (EAM, AVC e revascularização urgente).18 Uma outra meta‐análise avaliando o pré‐tratamento com iP2Y12 em doentes com EAM sem supradesnivelamento do segmento ST não mostrou impacto na mortalidade, mas um aumento significativo das complicações hemorrágicas.19 Num outro estudo não randomizado com avaliação por ressonância magnética cardíaca, o pré‐tratamento com clopidogrel associou‐se a uma menor prevalência e menor extensão de oclusão microvascular, mas sem variação na extensão do enfarte.9
Quanto ao prasugrel, num estudo randomizado, o pré‐tratamento com prasugrel em doentes com EAM sem supradesnivelamento do segmento ST não demonstrou benefícios no prognóstico e na segurança para esta estratégia.20
Como podemos constatar, este tem sido um tema com múltiplos estudos, mas com resultados inconstantes, estando assim o benefício inequívoco do pré‐tratamento com DC‐iP2Y12 por demonstrar,21 com o único ensaio randomizado em doentes com EAMcST a não comprovar o seu benefício.5 Por outro lado, é sabido que os novos iP2Y12 têm um início de ação mais rápido do que o clopidogrel,22,23 pelo que os resultados que apontam para um benefício do pré‐tratamento com clopidogrel podem não se manter com o uso dos novos iP2Y12. Um pequeno estudo do mundo real com pré‐tratamento com ticagrelor 1,5 hora antes da AP demonstrou uma melhoria no fluxo TIMI após AP, mas sem impacto na mortalidade, trombose de stent ou hemorragia24.
No nosso estudo, que inclui 4123 doentes com EAMcST e AP, numa análise multivariada, a utilização da DC‐iP2Y12 não teve impacto na mortalidade e no Mace, com a estratégia de PRE‐DC‐iP2Y12 a aumentar o risco de reenfarte, o que, na opinião dos autores, acaba por ser um resultado inesperado, dado que o intuito de fazer pré‐tratamento com iP2Y12 é reduzir eventos trombóticos e melhorar o fluxo coronário no momento da AP pela inibição plaquetar mais precoce. Enquanto numa análise univariada a estratégia PRE‐DC‐iP2Y12 se associou claramente ao aumento do MACE, na análise multivariada esse facto não se manteve, estando o pior prognóstico deste grupo relacionado com o maior número de comorbilidades já citadas anteriormente e com os maiores tempos até a realização de AP. Quando avaliamos os endpoints hemorrágicos, a estratégia PRE‐DC‐iP2Y12 aumentou Hemats e queda de Hb > 2g/dL, mas não hemorragia major ou transfusão de sangue.
Há grandes diferenças entre grupos no acesso por via radial, no uso de inibidores IIb/IIIa e na admissão direta no LH (ambos com taxas muito superiores no grupo CAT‐DC‐iP2Y12), que, como já citado, têm importantes implicações no prognóstico e no risco hemorrágico. É importante referir que estas variáveis foram incluídas no método de regressão logística para atenuar as diferenças entre grupos e para aumentar a fiabilidade dos resultados obtidos.
Analisando de forma global os resultados do nosso estudo, o pré‐tratamento com iP2Y12 não traz benefício prognóstico e aumenta o risco de complicações hemorrágicas nos doentes com EAMcST submetidos a AP, pelo que o uso desta estratégia pode ser pouco vantajosa, contrariando em parte as recomendações internacionais.1,2 Obviamente, o estudo tem limitações importantes, mas se junta a outros que colocam em causa as atuais recomendações.5,19,24 Da análise efetuada, analisando os preditores para Mace e Hemats, é possível notar que muitos dos fatores que aumentam o risco trombótico, também aumentam o risco hemorrágico, de que são exemplo FC > 100/min, doença multi‐vaso, Feve < 40% e KK > 1, fatores que foram preditores tanto para Mace como para Hemats.
Preditores para a estratégia utilizadaA idade < 45 anos, a presença de enfarte de localização indeterminada com BCRE de novo, classe KK > 1, Feve < 50% e tempo S‐B > 120min foram preditores para o uso de PRE‐DC‐iP2Y12. Esta estratégia foi usada em doentes mais jovens, em doentes com evidência de insuficiência cardíaca (com má função ventricular esquerda e pior KK) e em doentes com expectativa de revascularização mais tardia.
Antecedentes de tabagismo, angina de peito, EAM e demência, localização de EAMcST anterior, sintoma predominante de dor torácica, FC > 100/min, PAS < 90mmHg foram preditores para CAT‐DC‐iP2Y12. Esta estratégia foi a preferida em doentes com diagnóstico estabelecido ou provável de doença coronária (tabagismo, angina de peito, EAM prévio e sintoma predominante de dor torácica) e em doentes com enfarte anterior e maior instabilidade hemodinâmica.
Para ambas as situações, e dada a limitação do carácter retrospetivo do estudo, é difícil afirmar, com certeza, se estes preditores são verdadeiros fatores de decisão para a escolha da estratégia ou se na verdade são já consequência da estratégia escolhida, devendo estes dados ser interpretados com precaução.
LimitaçõesO estudo apresenta algumas limitações. Trata‐se de um estudo retrospetivo com todas as desvantagens e limitações associadas a este tipo de estudos. Tem um seguimento curto, apenas até ao momento da alta‐hospitalar. Possui uma grande heterogeneidade entre grupos, com a maioria das diferenças a beneficiarem o prognóstico do grupo CAT‐DC‐iP2Y12, tendo sido efetuada uma análise multivariada ajustada às diferenças entre grupos que as tenta mitigar, mas que também retira poder estatístico à amostra. Outra limitação do estudo é o facto da maioria dos doentes da população em estudo usar o clopidogrel como iP2Y12 quando as recomendações mais recentes recomendam a utilização de ticagrelor e prasugrel. Por fim, a ausência de registos dos tempos exatos da dose de carga no pré‐hospitalar não permitem avaliar a real diferença de tempo entre a DC‐iP2Y12 entre os grupos.
ConclusõesNo nosso estudo, nos doentes com EAMcST submetidos a AP, o clopidogrel continuou a ser o iP2Y12 mais utilizado. A estratégia preferencial em Portugal é o pré‐tratamento com DC‐iP2Y12 antes da AP, com dois terços dos doentes a seguir esta estratégia.
A estratégia PRE‐DC‐iP2Y12 foi a preferida nos doentes mais jovens, naqueles com sinais de insuficiência cardíaca e nos doentes em que o tempo até a AP foi superior. A estratégia CAT‐DC‐iP2Y12 foi preferencial em doentes com enfarte anterior e instabilidade hemodinâmica e em doentes com diagnóstico de doença coronária estabelecida.
Neste estudo, o pré‐tratamento com iP2Y12 não influenciou morte e Mace, tendo sido preditor de um aumento da taxa de reenfarte. Na avaliação de segurança, o pré‐tratamento com iP2Y12 associou‐se a um aumento do risco hemorrágico, sendo preditores de Hemats e queda de Hb > 2g/dL. Em doentes da vida real as conclusões deste estudo não corroboram um benefício do pré‐tratamento com iP2Y12 antes da AP. Estes resultados têm limitações, sobretudo pelo carácter retrospetivo do estudo e pela heterogeneidade entre grupos, no entanto, chama a atenção para a necessidade para um estudo randomizado de larga escala que melhor defina o tempo ótimo de administração da DC‐iP2Y12.
Conflitos de interesseOs autores declaram não haver conflito de interesses