A pericardite constritiva é uma entidade clínica caracterizada pelo aparecimento de sinais e sintomas de insuficiência cardíaca direita, secundários à perda da compliance pericárdica. Atualmente, a cirurgia cardíaca tornou‐se numa das etiologias mais frequentes nos países desenvolvidos, mantendo‐se a tuberculose como a causa mais prevalente nos países em vias de desenvolvimento. As etiologias neoplásicas são mais raras e habitualmente de pior prognóstico. O diagnóstico desta entidade mantém‐se um desafio clínico, sendo necessária a integração dos achados dos métodos de diagnóstico não invasivos (ecocardiografia, ressonância magnética e tomografia computorizada) e por vezes o recurso ao cateterismo cardíaco. Os autores apresentam o caso clínico de um homem de 51 anos de idade, internado por tamponamento cardíaco. A investigação etiológica foi sugestiva de etiologia tuberculosa, que apesar da terapêutica médica dirigida, evoluiu para fisiologia efusiva‐constritiva. Foi submetido a pericardiectomia e o exame anátomo‐patológico sugeriu etiologia neoplásica. O doente veio a falecer no pós‐operatório em falência biventricular.
Constrictive pericarditis is a clinical condition characterized by the appearance of signs and symptoms of right heart failure due to loss of pericardial compliance. Cardiac surgery is now one of the most frequent causes in developed countries, while tuberculosis remains the most prevalent cause in developing countries. Malignancy is a rare cause but usually has a poor prognosis. The diagnosis of constrictive pericarditis remains a clinical challenge and requires a combination of noninvasive diagnostic methods (echocardiography, cardiac magnetic resonance and computed tomography); in some cases, cardiac catheterization is needed to confirm the diagnosis. The authors present the case of a 51‐year‐old man, hospitalized due to cardiac tamponade. Diagnostic investigation was suggestive of tuberculous etiology. Despite directed medical therapy, the patient developed effusive‐constrictive physiology. He underwent pericardiectomy and anatomopathologic study suggested a neoplastic etiology. The patient died in the postoperative period from biventricular failure.
A pericardite constritiva é uma entidade clínica caracterizada pelo aparecimento de sinais e sintomas de insuficiência cardíaca direita, secundários à perda da compliance pericárdica1.
Atualmente, as causas mais frequentes são a cirurgia cardíaca, a radioterapia e a pericardite idiopática. Contudo, a tuberculose permanece como a causa mais frequente nos países em vias de desenvolvimento1.
O diagnóstico pode ser habitualmente estabelecido pela ecocardiografia com estudo Doppler, contudo, nos casos equívocos será necessário o recurso a outros métodos de diagnóstico, como a ressonância magnética (RM) ou a tomografia computorizada (TC) cardíacas e a avaliação hemodinâmica invasiva através do cateterismo cardíaco.
A terapêutica baseia‐se na administração de diuréticos e na terapêutica dirigida à condição subjacente. No entanto, a pericardiectomia é a única terapêutica definitiva e potencialmente curativa e a recomendada para os casos de cronicidade estabelecida.
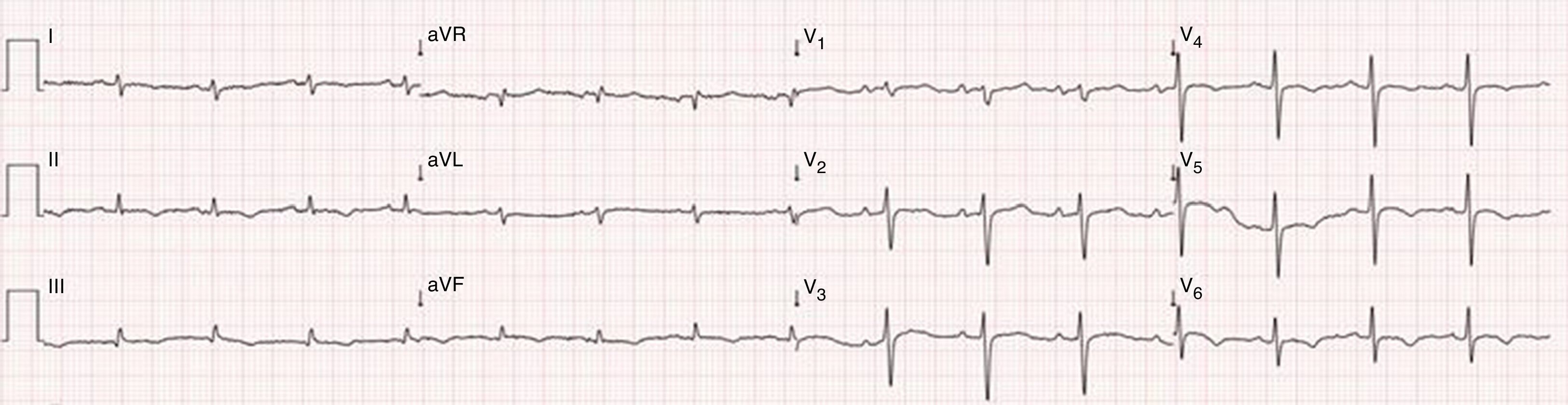
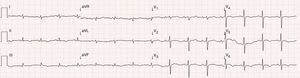
Caso clínicoDoente do sexo masculino, 51 anos de idade, raça negra, desportista habitual, sem antecedentes pessoais patológicos relevantes. Recorreu ao serviço de urgência por quadro clínico, com cerca de uma semana de evolução, de cansaço, de agravamento progressivo, dor precordial tipo picada ocasional, aumento do volume abdominal, anorexia e intolerância alimentar, com vários episódios de vómitos. Três dias antes do internamento teve um episódio de síncope e notou o aparecimento de engorgitamento jugular significativo. Negou febre, calafrios, tosse, expetoração, perda ponderal. À observação apresentava PA 118/78mmHg, FC 98bpm, estava apirético, dispneico, com engorgitamento jugular, tons cardíacos apagados, sem edema periférico. O eletrocardiograma (ECG) mostrava ritmo sinusal, com baixa voltagem dos QRS nas derivações clássicas e dos membros e padrão S1Q3T3 (Figura 1). Analiticamente destacava‐se discreta elevação de parâmetros inflamatórios (leucócitos 11,6x109/L, PCR 3,9mg/dL), marcada elevação dos D‐dímeros (5.153ng/mL), Hb 13,3g/dL, creatinina 1,3mg/dL e marcadores de necrose miocárdica negativos. Realizou angio‐TC de tórax que excluiu tromboembolismo pulmonar, mas revelou volumoso derrame pericárdico e pleural direito. O ecocardiograma mostrou volumoso derrame pericárdico circunferencial de características não límpidas, com dimensão máxima de 32mm e colapso parcial das cavidades direitas (Figura 2). Para fins diagnósticos e terapêuticos, foi realizada pericardiocentese evacuadora sob controlo fluoroscópico, com drenagem de líquido sero‐hemático (4000cc no total). O estudo citoquímico revelou líquido pericárdico com características de exsudado, com níveis de ADA normais. O exame citológico não revelou células neoplásicas e o exame microbiológico direto e cultural foi negativo, nomeadamente para micobactérias. Foram pesquisados vários marcadores de doenças autoimunes (ANA, fator reumatoide, anticardiolipina, anti‐β2 glicoproteína, níveis de C3 e C4) e de doenças hemato‐oncológicas (CEA, CA 19,9, PSA, α‐fetoproteina, β‐2 microglobulina, esfregaço de sangue periférico), não se obtendo nenhum valor com contribuição positiva para o diagnóstico. A pesquisa de anticorpos virais (echovirus, Coxsackie, adenovírus, influenza A e B, VIH, VHB, VHC) foi negativa ou não sugestiva de infeção recente. A TC toraco‐abdomino‐pélvica apenas revelou polisserosite, não mostrando nomeadamente adenopatias ou outras massas suspeitas. Posteriormente, obteve‐se positividade no doseamento do Interferon‐γ release assay (IGRA), pelo que se assumiu o diagnóstico de pericardite tuberculosa e o doente iniciou terapêutica com tuberculostáticos.
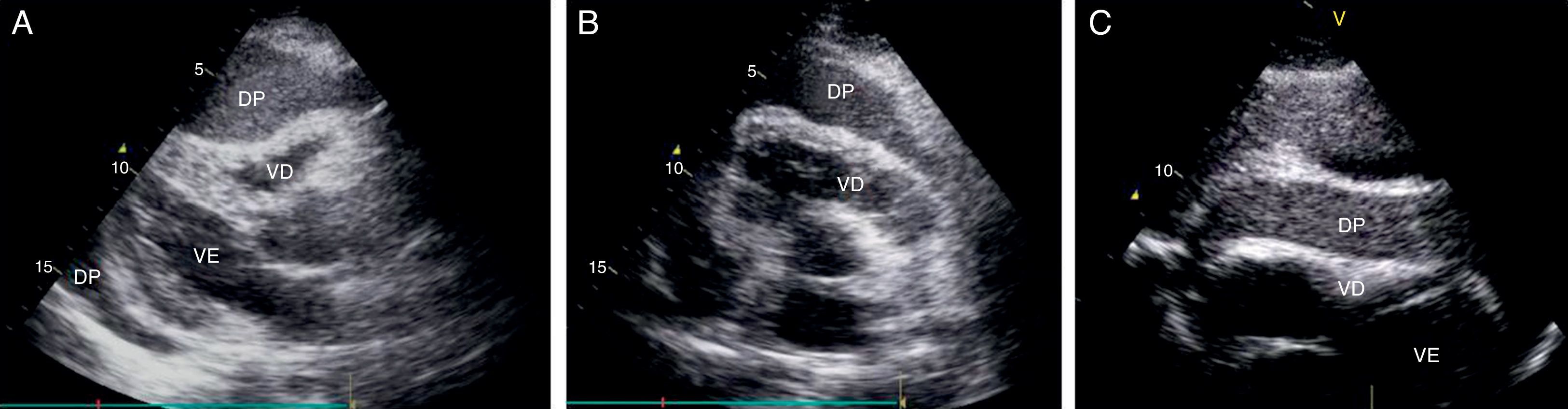
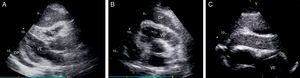
Imagem de ecocardiografia bidimensional transtorácica em plano (A) paraesternal longo eixo, (B) paraesternal curto eixo e (C) subcostal, mostrando volumoso derrame pericárdico circunferencial de características não límpidas, com colapso parcial das cavidades direitas. DP: derrame pericárdico; VD: ventrículo direito; VE: ventrículo esquerdo.
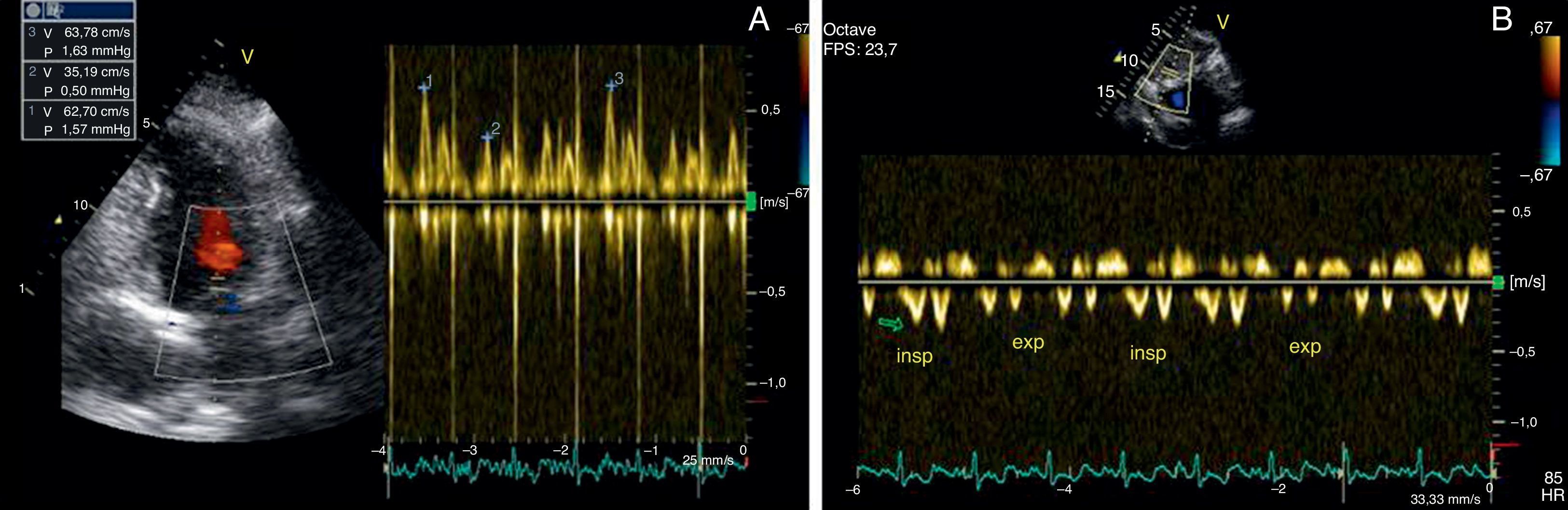
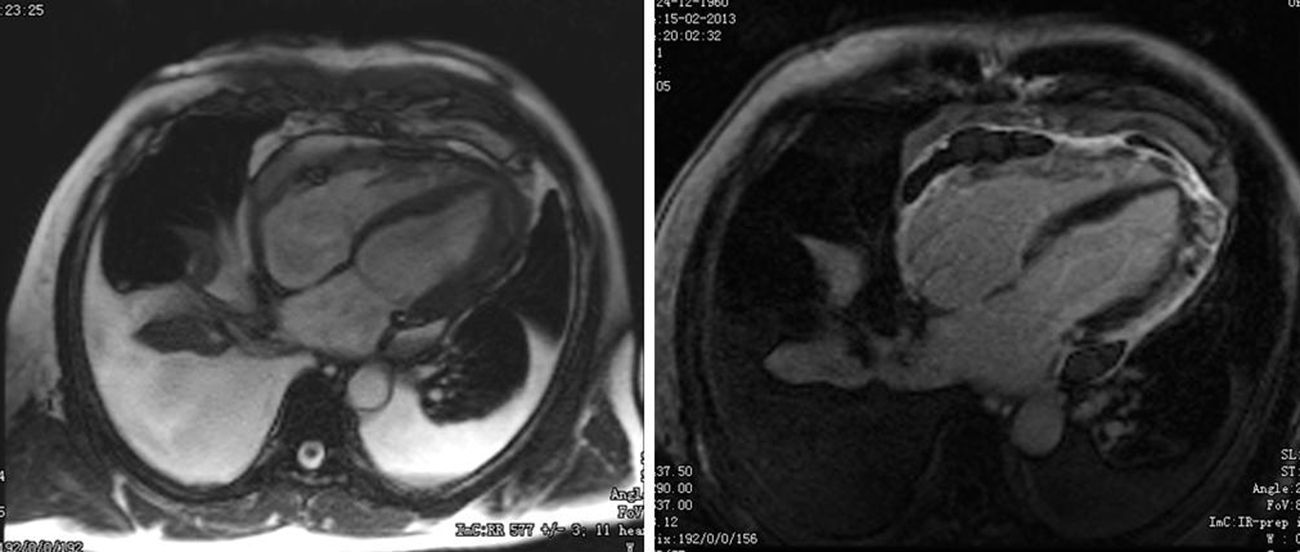
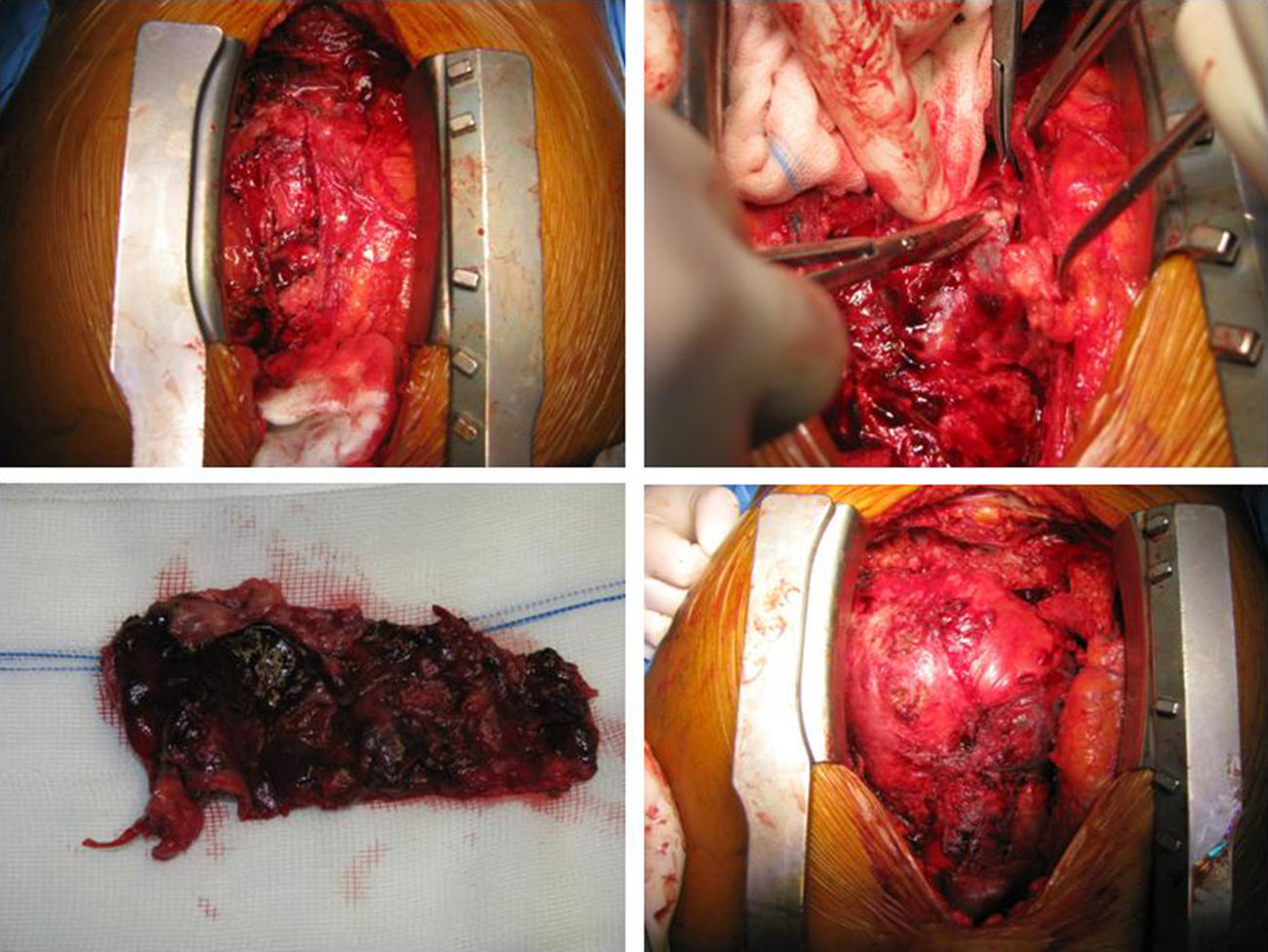
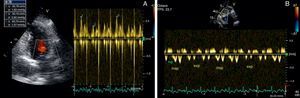
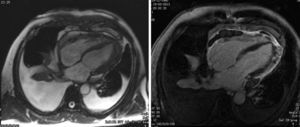
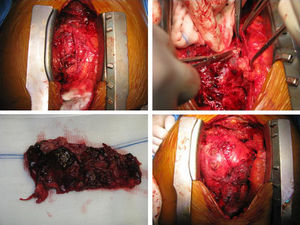
Dois meses após início da terapêutica tuberculostática, a reavaliação ecocardiográfica revelou sinais de constrição pericárdica (septal bounce, variação respiratória significativa do fluxo transvalvular cardíaco e do fluxo venoso hepático – Figura 3) associados a pequena lâmina de derrame pericárdico. Foi solicitada RMN cardíaca, que confirmou estes achados e revelou espessamento do pericárdio, sem aumento da intensidade de sinal após injeção de contraste e com extensa área de realce tardio, bem como zonas de continuidade com o miocárdio e sinais de fisiologia constritiva (septal bounce) (Figura 4). Clinicamente, e durante o terceiro mês de terapêutica dirigida, observou‐se o desenvolvimento de um quadro de insuficiência cardíaca de predomínio direito que motivou novo internamento e que foi rapidamente progressivo, evoluindo para anasarca, disfunção hepática, enteropatia exsudativa e caquexia. Atendendo ao diagnóstico de pericardite efusiva‐constritiva, com deterioração clínica rapidamente progressiva e sinais de cronicidade, foi referenciado para terapêutica cirúrgica e submetido a pericardiectomia. No intraoperatório observou‐se uma sínfise pericárdica completa, com aspeto macroscópico sugestivo de infiltração tumoral (Figura 5). Foi efetuada uma descorticação parcial, atendendo à dificuldade técnica condicionada pela presença de zonas de continuidade entre o pericárdio e o miocárdio.
No pós‐operatório desenvolveu falência biventricular, sem resposta à terapêutica aminérgica, tendo falecido ao 6.° dia de pós‐operatório. O exame anátomo‐patológico da peça operatória revelou pericárdio com metástases sugestivas de carcinoma pavimentocelular pouco diferenciado, com provável origem pulmonar.
DiscussãoA pericardite constritiva deve ser considerada no diagnóstico diferencial do quadro clínico de insuficiência cardíaca direita. A sua etiologia tem variado ao longo do tempo, sobretudo nos países desenvolvidos2. Atualmente, as causas idiopáticas e a cirurgia cardíaca são as etiologias mais frequentes, às quais se seguem a radioterapia, as conectivites, as causas infecciosas e as neoplásicas2. A tuberculose continua a ser a principal etiologia da doença nos países em desenvolvimento e nos doentes imunodeprimidos3. Quanto ao atingimento pericárdico de etiologia neoplásica, este manifesta‐se habitualmente por derrame pericárdico, sendo maioritariamente secundário ao processo de metastização de cancro do pulmão (35%), mama (25%), linfoma e leucemia (15%). Comparativamente, o derrame pericárdico secundário à neoplasia do pulmão e outros tumores sólidos que não os da mama, está associado a pior prognóstico do que os causados por neoplasia da mama ou hematológica4.
Para além da forma clássica, a pericardite constritiva pode apresentar‐se sob as formas localizada, transitória, oculta e efusiva‐constritiva5. A pericardite efusiva‐constritiva é uma variante da constrição pericárdica associada a derrame pericárdico, na qual se verifica persistência da fisiologia constritiva após pericardiocentese6.
Na pericardite constritiva ocorre uma fibrocalcificação do pericárdio que provoca redução da sua compliance, aumento das pressões venosas e restrição do enchimento diastólico ventricular, após uma fase inicial de enchimento adequado. Estas alterações patológicas provocam variações hemodinâmicas características relacionadas com a respiração. O fluxo para o ventrículo esquerdo (VE) diminui durante a inspiração como resultado de dois mecanismos: 1) diminuição do gradiente de pressão entre as veias pulmonares e a aurícula esquerda (AE), devido à rigidez pericárdica que limita a transmissão da redução da pressão intratorácica ao espaço pericárdico; 2) aumento da interdependência ventricular, desencadeado pelo subenchimento do VE, que provoca um desvio do septo interventricular (SIV) para a esquerda, com um consequente aumento do enchimento das cavidades direitas e sobrecarga de pressão sobre o SIV7.
A ecocardiografia tem um papel fundamental no diagnóstico da pericardite constritiva. Os sinais sugestivos são: 1) o espessamento pericárdico, embora a pericardite constritiva possa ocorrer sem que haja aumento da espessura do pericárdio; 2) movimento anómalo do SIV (septal bounce); 3) dilatação e ausência ou diminuição do colapso da veia cava inferior (VCI) e veias supra‐hepáticas; 4) velocidade protodiastólica (é) do anel mitral preservada ou aumentada, sendo este um sinal importante na distinção da miocardiopatia restritiva, na qual o e’ é habitualmente <7cm/seg3. O sinal ecocardiográfico mais característico da pericardite constritiva é o aumento da variação respiratória do fluxo transvalvular, que se expressa por diminuição do fluxo transvalvular do coração esquerdo durante a inspiração e o seu aumento com a expiração, ocorrendo o oposto nas válvulas do coração direito. Este sinal é significativo se a variação da onda E mitral for superior a 25% e raramente ocorre na miocardiopatia restritiva1.
Depois da ecocardiografia, a RM cardíaca é o método de imagem de escolha para o estudo do pericárdio. Devido à sua composição fibrosa, o pericárdio saudável revela‐se como uma estrutura hipointensa nas sequências ponderadas em T1 e T2. Na pericardite constritiva, as características morfológicas típicas são o espessamento global das lâminas do pericárdio (>4mm em espessura) e a presença de realce tardio no pericárdio, que se correlaciona com a fase aguda da inflamação pericárdica8. A RM permite ainda a adequada diferenciação entre derrames pericárdicos de pequenas dimensões e o espessamento pericárdico, a deteção do septal bounce e da aderência entre o pericárdio e o miocárdio2. A TC cardíaca também é útil no diagnóstico da pericardite constritiva, na medida em que permite demonstrar o espessamento e a calcificação pericárdicos, tal como a dilatação da VCI e a angulação do SIV. A perda do comportamento pulsátil das estruturas pulmonares imediatamente adjacentes ao coração, associada ao espessamento pericárdico, é altamente sugestiva de uma fisiologia constritiva3. Destaca‐se o valor adicional destes dois métodos de diagnóstico, sobretudo quando as variações respiratórias ecocardiográficas são equívocas, bem como quando nos encontramos na presença de outras condições clínicas que podem estar associadas ao aumento da variação respiratória dos fluxos transvalvulares, como sejam a obesidade e a doença pulmonar obstrutiva crónica9.
A avaliação hemodinâmica invasiva através do cateterismo cardíaco é importante, mas nem sempre necessária para o diagnóstico da pericardite constritiva, dependendo dos resultados obtidos nas modalidades de imagem não invasivas. Existe caracteristicamente uma equalização de pressões telediastólicas das quatro cavidades, com um diferencial que habitualmente é inferior a 5mmHg1. O traçado de pressões ventriculares mostra um padrão típico dip‐and‐plateau (enchimento ventricular rápido na protodiástole, com cessação subsequente), também descrito como «sinal da raiz quadrada».
Embora seja habitualmente uma condição crónica, a pericardite constritiva pode apresentar‐se sob a forma transitória (exceto nos casos secundários a radioterapia). Nestes casos, na ausência de evidência de cronicidade (caquexia, fibrilhação auricular, disfunção hepática, calcificação pericárdica), alguns autores defendem que os doentes devem ser submetidos a terapêutica médica e vigilância clínica durante dois a três meses, antes de ser considerada a terapêutica cirúrgica, através de pericardiectomia10. No entanto, estes doentes necessitam de uma observação frequente, uma vez que a pericardiectomia deve ser executada assim que se desenvolverem sinais de constrição crónica, tendo em conta que a sobrevida dos doentes com constrição crónica submetidos a pericardiectomia é superior à dos doentes submetidos a terapêutica conservadora11. Contudo, o timing cirúrgico deve ser cuidadosamente escolhido, uma vez que nos casos de constrição avançada a pericardiectomia tem pouco, ou mesmo nenhum, benefício, e o risco cirúrgico destes doentes é inaceitavelmente elevado1. No caso particular da pericardite efusiva‐constritiva, sendo que o responsável pela constrição é o pericárdio visceral, é necessário realizar não só pericardiectomia parietal, mas também visceral, fator que acresce uma maior complexidade técnica a este procedimento1,6.
No caso do doente apresentado, o único achado positivo na marcha diagnóstica direcionou‐nos para o diagnóstico de pericardite tuberculosa, tendo iniciado terapêutica dirigida. Durante o follow‐up clínico e ecocardiográfico, foram detetados sinais de constrição pericárdica e o desenvolvimento de clínica de insuficiência cardíaca direita rapidamente progressiva, com uma rápida progressão para anasarca, disfunção hepática, enteropatia exsudativa e caquexia. O doente foi submetido a pericardiectomia, sendo o aspeto macroscópico do pericárdio sugestivo de etiologia neoplásica, totalmente inesperada atendendo aos exames pré‐operatórios, mas que foi posteriormente confirmada pela análise anátomo‐patológica.
Este caso clínico pretende enfatizar que o diagnóstico da pericardite constritiva continua a ser um desafio clínico. É necessária a integração dos resultados dos métodos de diagnóstico, invasivos e não invasivos, no diagnóstico diferencial e a procura ativa da causa subjacente. Por fim, é de extrema importância o seguimento apertado destes doentes e a deteção precoce de sinais de cronicidade, para possibilitar uma referenciação atempada para a pericardiectomia.
Responsabilidades éticasProteção de pessoas e animaisOs autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dadosOs autores declaram ter seguido os protocolos do seu centro de trabalho acerca da publicação dos dados de pacientes.
Direito à privacidade e consentimento escritoOs autores declaram que não aparecem dados de pacientes neste artigo.
Conflito de interessesOs autores declaram não haver conflito de interesses.