No advento dos stents eluidores de fármaco (DES), a restenose difusa (>20mm) intrastent (RDIS) constituía a principal limitação ao uso de stents metálicos na intervenção coronária (PCI). Das várias soluções propostas para o seu tratamento, a braquiterapia intracoronária (BT) revelou‐se uma das mais eficazes, sendo praticamente abandonada após a introdução dos DES.
ObjetivoAvaliar os resultados clínicos a longo prazo (>10 anos) do uso de BT beta com 90Sr/Y90 para o tratamento RDIS, em termos de eventos cardíacos major (MACE) e restenose angiográfica.
População e métodosEstudo retrospetivo observacional de centro único incluindo 12 doentes (dts) consecutivos entre janeiro e julho de 2001, 11 homens, com a idade média de 58,6±9,9 anos (43‐77 anos). Todos tinham angor estável. Os principais fatores de risco eram dislipidemia (75%), HTA (58%), doença arterial periférica (50%) e diabetes (42%). Havia doença multivaso em seis dts, tratava‐se da 2.a ou 3.a restenose em seis dts e a função ventricular era normal em 11. A BT foi feita após dilatação com balão, usando a fonte emissora de radiação beta 90Sr/Y90 (Beta‐Cath™/Novoste). Todos permaneceram sob dupla antiagregação pelo menos até à angiografia de controlo, programada para todos aos nove meses. Foi considerada a ocorrência de morte global e cardiovascular, enfarte do miocárdio não fatal (EAM), revascularização coronária, trombose de stent e restenose angiográfica. Foi avaliada a incidência do evento hierárquico combinado (MACE) de: morte cardiovascular, EAM, revascularização coronária urgente do vaso alvo (TVRurg).
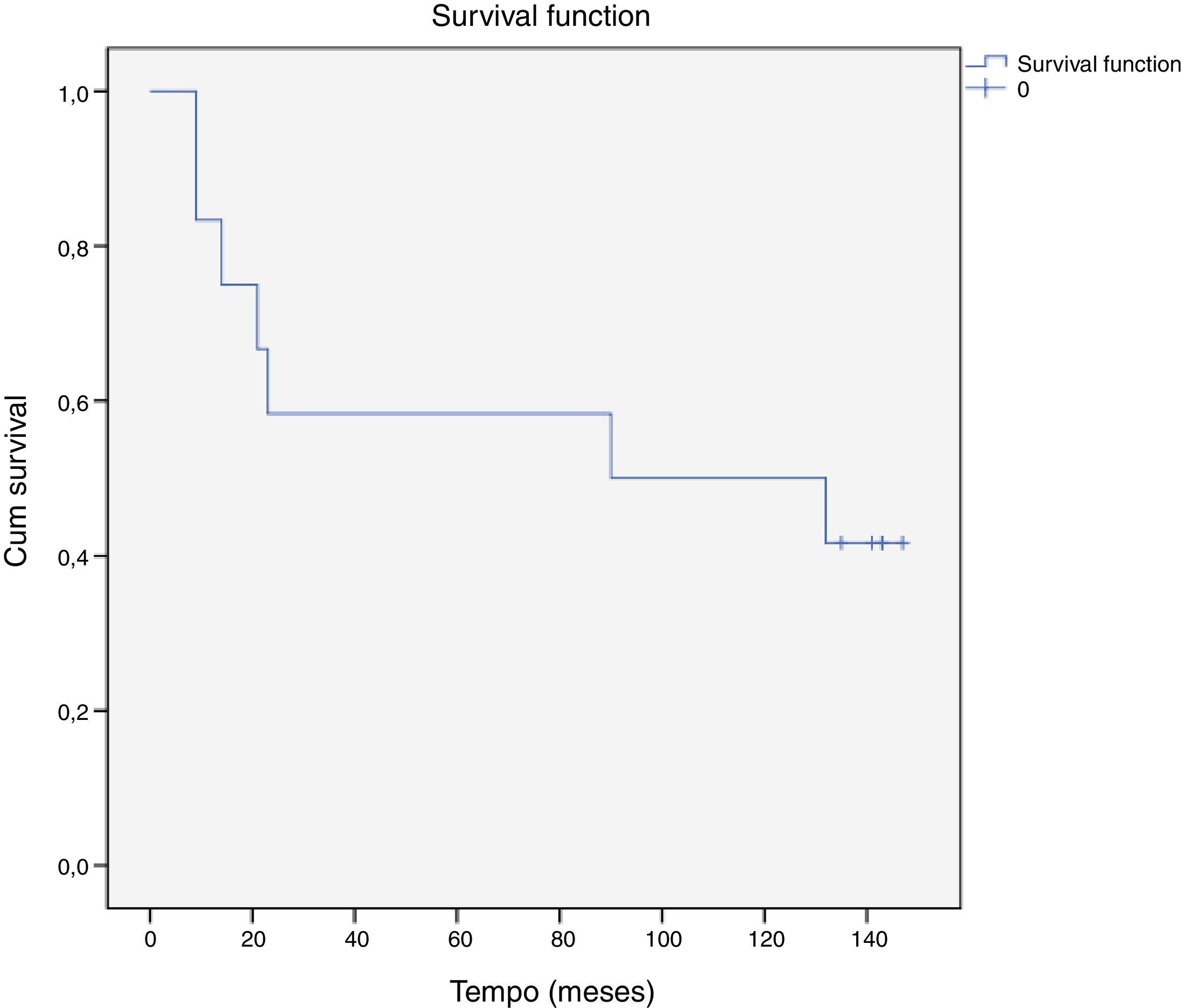
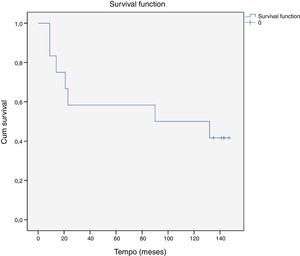
ResultadosVerificou‐se sucesso angiográfico e clínico em 100% dos casos. No seguimento médio de 10,9±2,5 anos, ocorreram 19 eventos em sete dts: morte em três dts (25%), apenas uma cardíaca (8,3%), EAM com elevação de ST (vaso não alvo) num dt (8,3%) e 15 novas revascularizações em cinco dts (42%): nove relacionadas com o vaso alvo (sobretudo nos primeiros dois anos). Apenas se verificou uma trombose de stent, provável. A restenose angiográfica aos nove meses de seguimento foi de 27% (3/11dts) com duas oclusões. A taxa de sobrevivência livre de MACE aos dez anos foi de 42% (cincodts).
ConclusõesA braquiterapia com radiação beta para RDIS, neste pequeno grupo de dts, demonstrou‐se eficaz e segura, sem eventos tardios atribuíveis à radiação intracoronária.
Until the development of drug‐eluting stents (DES), diffuse in‐stent restenosis (ISR) was the main limitation of bare‐metal stents in percutaneous coronary intervention (PCI). Among the different treatments available, intracoronary brachytherapy (BT) emerged as one of the most promising, although it was almost abandoned with the increasing use of DES.
ObjectiveTo assess the Portuguese experience with 90Sr/90Y beta brachytherapy for the treatment of diffuse ISR regarding long‐term (>10 years) major adverse cardiac events (MACE) and angiographic restenosis.
MethodsThis single‐center, retrospective, observational study included 12 consecutive patients treated between January and June 2001, mean age 58.6±9.9 years (range 43‐77 years), 11 male. All had chronic stable angina, 75% had dyslipidemia, 58% had hypertension, 50% had peripheral arterial disease, 42% had diabetes and 50% had multivessel disease. Recurrent ISR was present in half of the patients and 11 had normal left ventricular function. After balloon dilatation, BT was performed using an Sr90/Y90 (Novoste Beta‐CathTM) beta radiation source. All patients remained under dual antiplatelet therapy until scheduled nine‐month follow‐up angiography. Patients were followed for the occurrence of death (all‐cause and cardiovascular), non‐fatal myocardial infarction (MI), revascularization, stent thrombosis and angiographic restenosis. MACE were defined as the combined incidence of cardiac death, MI and urgent target vessel revascularization.
ResultsIn all cases there was both clinical and angiographic success. In a mean follow‐up of 10.9±2.5 years, 19 events occurred in seven patients: death in three (25%), only one cardiac (8.3%); ST‐elevation MI in one (related to a non‐target vessel) (8.3%); and 15 revascularizations in five (42%), of which nine were of the target vessel (mainly in the first two years). There was only one case of probable stent thrombosis. Angiographic restenosis at nine months was 27% (three out of 11 patients), of which two were total occlusions. Ten‐year MACE‐free survival was 42% (5 patients).
ConclusionsIntracoronary beta brachytherapy for the treatment of diffuse ISR in this small cohort of patients proved to be safe and efficacious, with no late adverse events related to intracoronary radiation.
Antes da era dos stents revestidos com fármacos, a restenose, por proliferação tecidular da neoíntima, constituía a principal limitação ao uso mais alargado da implantação de stents metálicos na intervenção coronária percutânea (ICP). A forma mais problemática de restenose intrastent (RIS) foi originalmente descrita com a restenose difusa segundo a classificação angiográfica de Mehran et al1. pela elevada percentagem de recidivas e necessidade de subsequentes revascularizações. Das soluções tentadas para controlar essa hiperplasia da neoíntima, a braquiterapia (BT) com radiação intracoronária pelo seu mais potente efeito antiproliferativo2–6 foi a que apresentou melhores resultados. Vários estudos aleatorizados com radiação gama e beta comprovaram a sua eficácia e segurança6–11. Em novembro de 2000, após a sua aprovação pela Food and Drug Administration (FDA), a técnica ficou estabelecida como adjuvante da angioplastia de balão para RIS até à data12,13. No entanto, a eficácia clínica da BT a longo prazo tem sido questionada14 e poucos estudos têm sido publicados com seguimentos tardios após BT com radiação beta15–20.
O presente estudo tem por objetivo analisar a única experiência portuguesa de BT com radiação beta em 2001 e avaliar a sua eficácia e segurança tardias, num seguimento clínico superior a dez anos.
População e métodosForam incluídos nesta análise 12 doentes consecutivos, submetidos a BT com radiação beta para restenose difusa intrastent, entre janeiro e julho de 2001. Os doentes foram selecionados por apresentarem restenose difusa de stents metálicos previamente implantados que foi definida como tendo estenose ≥50% e comprimento ≥20mm.
A média de idades dos doentes era 58,6±9,9 anos (43‐77 anos), 11 eram do sexo masculino. A prevalência dos principais fatores de risco foi dislipidemia em nove doentes (75%), a hipertensão arterial em sete doentes (58%) e a diabetes em cinco doentes (42%). Seis doentes (50%) tinham doença vascular periférica associada. Todos os doentes tinham angina estável havendo história prévia de enfarte em quatro (33%) e de cirurgia coronária em três (25%). Havia doença de multivaso em oito doentes e apenas um tinha depressão da função ventricular esquerda. Tratava‐se da primeira RIS em seis doentes, da segunda em quatro e da terceira em dois. Apenas uma restenose era proliferativa. Todos os indivíduos faziam terapêutica médica máxima tolerada com aspirina, estatinas, nitratos, bloqueadores beta, antagonistas do cálcio e inibidores da enzima de conversão da angiotensina (Tabela 1).
Características basais
| Doentes (n) | 12 |
| Idade (anos) | 58,6±9,9 |
| Sexo masculino, n (%) | 11 (92) |
| Fatores de risco | |
| Diabetes, n (%) | 5 (42) |
| Dislipidemia, n (%) | 9 (75) |
| Hipertensão, n (%) | 7 (58) |
| Doença arterial periférica, n (%) | 6 (50) |
| Tabagismo, n (%) | 2 (17) |
| História prévia | |
| Enfarte, n (%) | 4 (33) |
| Cirurgia coronária, n (%) | 3 (25) |
| Apresentação clínica | |
| Angina estável, n (%) | 12 (100) |
| Teste de isquemia positivo, n (%) | 10 (83) |
| Doença multivaso, n (%) | 8 (67) |
| Função ventricular preservada, n (%) | 11 (92) |
| Indicação para ICP | |
| Primeira restenose, n (%) | 6 (50) |
| Segunda restenose, n (%) | 4 (33) |
| Terceira restenose, n (%) | 2 (17) |
| Terapêutica médica pré‐intervenção | |
| Aspirina, n (%) | 12 (100) |
| Estatinas, n (%) | 9 (75) |
| Beta bloqueantes, n (%) | 9 (75) |
| Antagonistas do cálcio, n (%) | 9 (75) |
| IECA, n (%) | 7 (58) |
| Nitratos, n (%) | 10 (83) |
ICP: intervenção coronária percutânea; IECA: inibidores da angina de conversão da angiotensina.
A análise quantitativa das coronariografias foi realizada usando o sistema CAAS 2™ (Cardiovascular Angiographic Analysis System). Como referência foi usado o diâmetro do cateter guia de angioplastia. Analisaram‐se quantitativamente o diâmetro do vaso de referência, o comprimento da lesão, o grau de estenose e o diâmetro luminal mínimo (MLD). Foi considerada restenose angiográfica a presença de uma estenose intraluminal e intrastent ≥50%. Importa realçar o comprimento longo das lesões tratadas (de 40‐90mm), em vasos pequenos com diâmetro médio do vaso de referência de 2,5mm (Tabela 2).
Características das lesões tratadas
| Vaso alvo, n (%) | |
| Art. descendente anterior | 4 (33) |
| Art. circunflexa | 2 (17) |
| Art. coronária direita | 6 (50) |
| Tipo stent: total de 20 stents, n (%) | |
| ACS Multilink™ Tetra (Guidant/Advance Cardiovascular Systems) | 8 (40) |
| Bx Velocity™ (Cordis, Johnson&Johnson Company) | 7 (35) |
| AVE GFX‐2™ (Advance Vascular Engineering, Inc) | 2 (10) |
| AVE S670™ (Advance Vascular Engineering, Inc) | 1 (5) |
| NIRoyal™ (Medinol, Scimed Life Systems) | 1 (5) |
| Bx Velocity™ Heparin Coated stent (Cordis, Johnson&Johnson Company) | 1 (5) |
| Análise quantitativa | |
| Diâmetro médio vaso referência (mm) | 2,56±0,58 |
| Diâmetro luminal mínimo médio (mm) | 1,0±0,12 |
| Grau estenose médio (%) | 64,4±16,9 |
| Comprimento médio (mm) | 55,9±19,5 (40‐90mm) |
Usou‐se para a BT a radiação intracoronária beta com 90Sr/Y90 (Beta‐Cath™/Novoste). Foi escolhida a radiação beta porque não requeria alterações logísticas do laboratório de hemodinâmica, necessárias com a radiação gama. Foi estabelecido um protocolo com o Instituto Português de Oncologia Francisco Gentil de Lisboa, do qual fizeram parte radioterapeutas e físicos. Todos os doentes deram o seu consentimento informado e a Comissão de Ética do Hospital de Santa Cruz deu parecer favorável.
Todos os procedimentos foram efetuados por acesso femoral com cateteres guia 8F. Após a angiografia de controlo e a confirmação da RIS, o cateter diagnóstico foi substituído por cateter guia de angioplastia. A lesão foi atravessada por fio guia 0,014¿¿ de angioplastia e foi feita a dilatação da restenose com balão de diâmetro e comprimento adaptado ao diâmetro do vaso e comprimento das lesões. O cateter de fornecimento da BT com radiação beta (Beta‐Cath™ Delivery Catheter) é um cateter 5F de triplo lúmen para o fio guia, para fornecimento da radiação e para preenchimento com soro fisiológico. Usaram‐se exclusivamente cateteres de 40mm de comprimento. O cateter foi avançado através do fio guia, iniciando‐se a aplicação de radiação pela parte mais distal até à parte mais proximal da lesão, ultrapassando‐se sempre para a porção do território vascular adjacente sem doença angiograficamente detetável. Fez‐se um ou mais períodos de BT de acordo com o comprimento das lesões (um em sete doentes, dois em três doentes e três períodos em dois doentes). A dose e o tempo de radiação variou de acordo com tabelas pré‐definidas para o diâmetro do vaso/stent (18,4Gr para diâmetros ≥2,7 e <3,35mm com tempo de radiação de 215seg e 23,0Gr para vasos >3,35 e ≤4,00mm com tempo de radiação de 268seg). Sempre que necessário, as lesões voltaram a ser dilatadas com o cateter de balão usado inicialmente. Todas as manobras de manipulação da radiação desde a sua fonte até ao cateter e a sua aplicação foram efetuadas pelos físicos e radioterapeutas. Todos os outros passos da técnica foram executados por cardiologistas. Foram efetuadas análises quantitativas das várias angiografias antes, durante e após o procedimento. A dose de heparina inicial foi de 5000 unidades e 2500U por cada hora adicional ou de acordo com o tempo de coagulação ativado (ACT) regularmente avaliado. Em 11 dos 12 doentes foi administrado abciximab profilaticamente. O tempo médio de radioescopia foi de 10,9±5min (4,8‐24,4) e o tempo médio do procedimento de 50±16min. (33‐79).Foram definidos, como sucesso angiográfico, a estenose residual máxima no final no segmento tratado < 50% e, como sucesso clinico, a presença de sucesso angiográfico na ausência de complicações clínicas durante o internamento hospitalar.
A medicação inicial foi mantida com instituição de dupla antiagregação plaquetária (DAP) com aspirina e clopidogrel ou ticlopidina. Todos os doentes foram seguidos regularmente até ao presente ou até à morte e em todos foi programada coronariografia de controlo aos nove meses após a intervenção.
No seguimento clínico obtido e de acordo com a definição do Academic Research Consortium (ARC)21 foram considerados os seguintes objetivos para análise: a morte cardiovascular e de qualquer causa, qualquer enfarte do miocárdio, qualquer nova revascularização, restenose angiográfica e incidência de trombose de stent de acordo com a nova definição ARC21. Foi avaliada também a incidência hierárquica do evento combinado de morte cardiovascular, EM não fatal e TVR urgente, definido como MACE.
Análise estatísticaNesta análise, os grupos de doentes foram caracterizados segundo variáveis contínuas e categóricas. As variáveis categóricas foram caracterizadas recorrendo a frequências absolutas e frequências relativas. A caracterização da tendência central e a da dispersão dos valores das variáveis contínuas foi estimada recorrendo à média amostral e ao desvio padrão.
A análise da sobrevivência livre de eventos foi efetuada com recurso às curvas de Kaplan‐Meier.
A análise estatística foi realizada com o software estatístico SPSS, versão 19.0.0.2.
ResultadosObteve‐se sucesso angiográfico e clínico do procedimento em todos os doentes. O grau de estenose reduziu‐se de 64,4±16,9 para 25,9±10,3% e o diâmetro luminal mínimo aumentou de 1,0±0,12 para 2,18±0,32mm. Não se verificaram quaisquer eventos clínicos durante o internamento hospitalar.No seguimento clinico aos 9 meses, apenas 1 doente mantinha queixas de angor, tendo sido documentada restenose e esse doente foi posteriormente submetido a revascularização cirúrgica.
Realizou‐se o seguimento em 100% dos doentes durante 10,9±2,5 anos (130±30 meses). Ocorreram 19 eventos em sete doentes (Tabelas 3 e 4). Três doentes faleceram (25%), um de neoplasia aos 90 meses após a BT e um doente por sépsis aos 132 meses, nenhum dos dois teve qualquer evento cardíaco após a BT. Registou‐se uma morte súbita cardíaca (8,3%) aos 43 meses após a BT, poucos dias depois de ter sido submetido a angioplastia e implantação de dois stents farmacológicos num vaso distinto do tratado por BT.
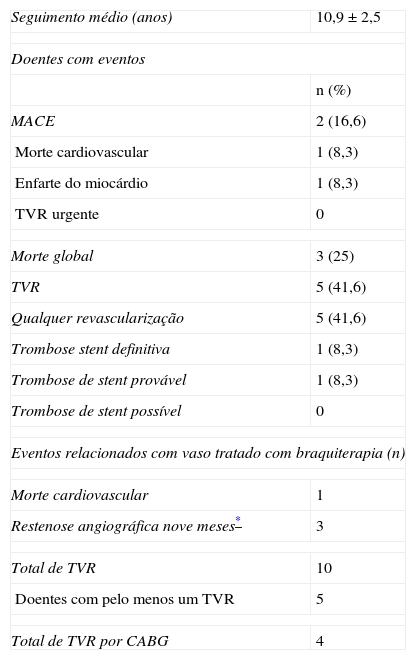
Resultados
| Seguimento médio (anos) | 10,9±2,5 |
| Doentes com eventos | |
| n (%) | |
| MACE | 2 (16,6) |
| Morte cardiovascular | 1 (8,3) |
| Enfarte do miocárdio | 1 (8,3) |
| TVR urgente | 0 |
| Morte global | 3 (25) |
| TVR | 5 (41,6) |
| Qualquer revascularização | 5 (41,6) |
| Trombose stent definitiva | 1 (8,3) |
| Trombose de stent provável | 1 (8,3) |
| Trombose de stent possível | 0 |
| Eventos relacionados com vaso tratado com braquiterapia (n) | |
| Morte cardiovascular | 1 |
| Restenose angiográfica nove meses* | 3 |
| Total de TVR | 10 |
| Doentes com pelo menos um TVR | 5 |
| Total de TVR por CABG | 4 |
CABG: revascularização coronária cirúrgica; MACE: eventos cardíacos major hierárquicos; TVR: revascularização do vaso alvo.
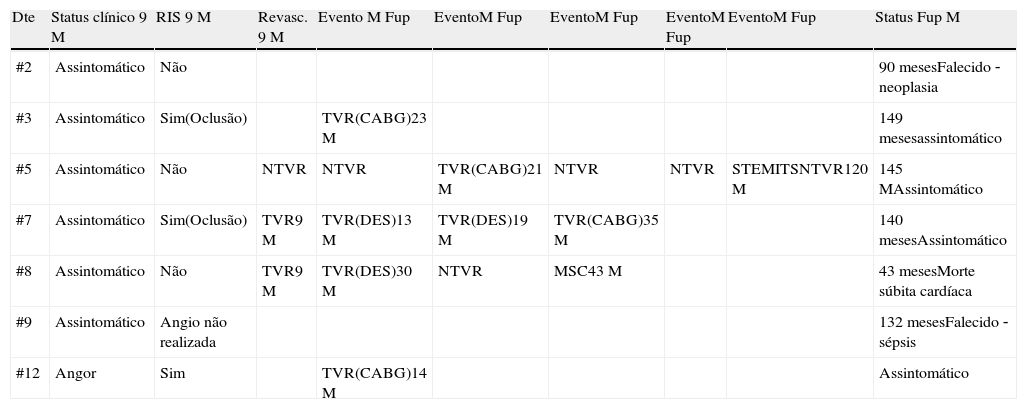
Descrição dos eventos ocorridos
| Dte | Status clínico 9 M | RIS 9 M | Revasc. 9 M | Evento M Fup | EventoM Fup | EventoM Fup | EventoM Fup | EventoM Fup | Status Fup M |
| #2 | Assintomático | Não | 90 mesesFalecido ‐ neoplasia | ||||||
| #3 | Assintomático | Sim(Oclusão) | TVR(CABG)23 M | 149 mesesassintomático | |||||
| #5 | Assintomático | Não | NTVR | NTVR | TVR(CABG)21 M | NTVR | NTVR | STEMITSNTVR120 M | 145 MAssintomático |
| #7 | Assintomático | Sim(Oclusão) | TVR9 M | TVR(DES)13 M | TVR(DES)19 M | TVR(CABG)35 M | 140 mesesAssintomático | ||
| #8 | Assintomático | Não | TVR9 M | TVR(DES)30 M | NTVR | MSC43 M | 43 mesesMorte súbita cardíaca | ||
| #9 | Assintomático | Angio não realizada | 132 mesesFalecido ‐ sépsis | ||||||
| #12 | Angor | Sim | TVR(CABG)14 M | Assintomático |
CABG: cirurgia de revascularização coronária; DES: stent eluidor de fármaco; Dte: número de doente; Fup: follow‐up clínico; M: meses após braquiterapia; MSC: morte súbita cardíaca; Mx: máximo; NTVR: revascularização de vaso não alvo; Revasc: revascularização; RIS: restenose intrastent; Status: situação clínica; TVR: revascularização de alvo alvo.
Aos 120 meses após BT um doente sofreu um EAM com elevação de ST, por trombose de stent implantado num vaso não alvo (8,3%), tendo sido submetido a angioplastia primária com sucesso.
Cinco doentes (42%) foram submetidos a 15 novas revascularizações. Todos estes doentes tiveram pelo menos uma revascularização do vaso alvo (no total de nove), sobretudo nos primeiros dois anos, incluindo quatro doentes (33,3%) submetidos a cirurgia de revascularização coronária.
A primeira revascularização do vaso alvo ocorreu em média 12±4,5 meses após a BT (de 9‐21 meses). De notar que dos cinco doentes que foram submetidos a revascularização do vaso alvo, três foram‐no na sequência da angiografia eletiva agendada, que revelou restenose do vaso alvo, sendo que dois estavam assintomáticos.
Ocorreu uma trombose de stent definitiva, já referida, num vaso não alvo (1/12=8,3%), 120 meses após a BT, num indivíduo submetido três meses antes a angioplastia com balão eluidor de fármaco de uma restenose de stent eluidor de fármaco previamente implantado neste vaso. Um doente teve uma trombose de stent provável (1/12=8,3%), por morte súbita, ocorrida após revascularização dum vaso não alvo, 45 meses após a BT. Não se registaram tromboses de stent possíveis nem qualquer trombose de stent definitiva ou provável nos vasos previamente submetidos a BT.
No seguimento de dez anos a incidência de MACE foi de 16,6% (dois doentes): uma morte súbita e um doente com EAM não fatal com elevação de ST. Nenhum doente teve qualquer revascularização urgente do vaso alvo.
A coronariografia de controlo para avaliação da restenose foi realizada em média 271,6±50,6 dias após a BT, nos 11 doentes que aceitaram realizá‐la. A taxa de restenose angiográfica nestes doentes foi de 27% (3/11 doentes), observando‐se oclusão assintomática do vaso alvo em dois casos (2/11=18%).
A taxa de sobrevivência livre de qualquer evento cardiovascular aos dez anos foi de 42% (5 doentes) (Figura 1).
DiscussãoO presente trabalho apresenta os resultados iniciais e a longo prazo, da única e limitada experiência, da radiação intracoronária para tratamento da restenose difusa intrastents metálicos em Portugal.
O pequeno número de doentes tratados não permite tirar ilações sobre o valor da BT comparativamente a outras técnicas usadas na altura para o tratamento da restenose intrastent. No entanto, o seguimento clínico a tão longo prazo oferece a oportunidade de contribuir para o conhecimento dos efeitos tardios da radiação intracoronária.
Na altura da introdução da técnica em Portugal, a BT constituía a melhor alternativa para o tratamento da RIS, que se revelava a maior limitação ao uso mais alargado de stents metálicos em certas situações, como lesões longas, restenoses repetitivas e em doentes diabéticos. Vários estudos revelaram a sua eficácia e segurança a curto prazo, com vantagem comparativamente a tratamentos farmacológicos, dilatação com balão ou cutting balloon, aterectomia rotacional, laser intracoronário ou stent intrastent2–11,22. As preocupações relativamente à BT resultaram sobretudo de três fatores: 1) o fenómeno chamado geographic miss pelo qual a radiação podia não cobrir os bordos proximais e distais dos stents provocando novas estenoses; 2) a possibilidade de trombose dos stents; e 3) a possibilidade de restenose tardia do vaso alvo da BT (chamado late catch‐up). Na nossa experiência, os dois primeiros problemas tinham sido já incorporados ao termos usado uma fonte de radiação de 40mm com técnica de pull back e por terem todos feito dupla antiagregação plaquetária, com tienopiridinas associadas à aspirina pelo menos até à angiografia de controlo. O longo período de seguimento obtido poderia elucidar o risco e a dimensão da restenose tardia e da trombose de stent do segmento irradiado.
Não houve complicações imediatas, clínicas ou de vaso, em todos os doentes submetidos a BT e os resultados iniciais foram excelentes na angiografia quantificada.
No nosso estudo, a taxa de restenose (27%) na angiografia de controlo aos nove meses está de acordo com o descrito na literatura. Nos vários estudos aleatorizados com radiação beta para RIS, a taxa de restenose aos 6‐9 meses foi em média de 30% (26‐34%)9–11. O que surpreende foi a ocorrência em doentes assintomáticos e sem qualquer síndrome coronária aguda, de duas restenoses por oclusão do vaso alvo (18%) apesar da DAP. Numa revisão de Walksman et al.23 em 473 doentes, após BT com radiação beta e gama, a oclusão tardia (>30 dias) ocorreu em 9,1% dos doentes que fizeram apenas um mês de DAP. Destes, apenas uma minoria (7%) teve oclusão assintomática, enquanto 43% tiveram enfarte agudo e 50% angina instável. A possibilidade de restenose tardia após BT para RIS era reconhecida em estudos de seguimento mais longo até cinco anos, sendo responsável pela continuada e tardia necessidade de revascularização do vaso alvo16,17.
Neste estudo e no seguimento médio de dez anos após o tratamento com BT, a incidência de eventos cardiovasculares major foi de 16,6%. Este valor pode ser considerado baixo tendo em conta a gravidade dos doentes tratados e o longo seguimento clínico. Em estudos com seguimento até um ano, a incidência de eventos major foi em média de 23% (15‐34%)9–11. No único estudo publicado com seguimento a dez anos do Thoraxcenter20, incluiu 124 doentes com BT para tratamento da RIS, a incidência de morte por qualquer causa foi de 16% e de morte ou enfarte não fatal foi de 25%. A incidência associada de mortalidade global, qualquer enfarte e qualquer nova revascularização foi nestes doentes de 70%, devido sobretudo a novas revascularizações do vaso alvo (47%), que ocorreram entre os cinco meses e dois anos de seguimento. A restenose tardia (late catch‐up) após radiação beta verificou‐se sobretudo nos doentes sem stents (lesões de novo).
Em relação aos receios do aumento da incidência de eventos coronários agudos, durante este longo período de seguimento, apenas um doente (8,3%) teve uma síndroma coronária aguda, complicação de uma angioplastia prévia noutro vaso. A única morte cardiovascular ocorre tardiamente e na sequência quase imediata de uma angioplastia complexa num vaso não alvo. Podemos considerar, com alguma segurança, que estes eventos coronários agudos dificilmente poderão ser atribuídos à BT.
Na nossa experiência, 42% dos doentes (n=5) necessitaram de múltiplas (n=9) revascularizações dos vasos previamente tratados por BT. Esta percentagem é elevada, quando comparada com a eficácia atual dos stents eluidores de fármacos, aspeto posto em evidência nos ensaios comparativos com a BT24–28. No entanto, devemos considerar a complexidade da população estudada: 50% com mais de uma restenose prévia do segmento tratado, 67% com doença multivaso, 42% de diabéticos e 50% com doença arterial periférica.
O facto de se ter programado angiografia de controlo aos nove meses poderá ter implicações na taxa de novas revascularizações observadas. É conhecido desde o estudo BENETENT II o fenómeno do reflexo óculo‐estenótico29. Dos cinco doentes submetidos a revascularização do vaso alvo, quatro doentes fizeram‐no por restenose angiográfica sem queixas de angor ou sem teste de isquemia positivo à data do procedimento (angioplastia não guiada por isquemia).
A eficácia demonstrada pelos stents revestidos no tratamento das restenoses intrastent veio diminuir a utilização de BT para esse efeito. Numa meta‐análise de estudos aleatorizados, comparando stents revestidos de primeira geração (sirolimus e paclitaxel) com angioplastia de balão ou BT no tratamento da RIS, verificou‐se uma redução de 64% na taxa de restenose angiográfica e de 65% nas revascularizações do vaso alvo, sem diferenças na incidência de morte ou enfarte, num seguimento clínico de 9‐12 meses24. No estudo TAXUS V ISR25, os stents revestidos com placlitaxel comparados com a BT com radiação beta diminuíram de forma significativa a necessidade da revascularização do vaso alvo por razões isquémicas (18,1 versus 27,5%, p=0,03), num seguimento a dois anos. No estudo SISR26 comparando stents revestidos com sirolimus com BT com radiação beta ou gama e seguimento a três anos, as revascularizações do vaso alvo não foram estatisticamente inferiores com os stents (20,8 versus 29,6%, p=0,073). A revascularização do vaso alvo manteve‐se semelhante no seguimento a cinco anos do mesmo estudo (24,7% com stents de sirolimus versus 31,2% com BT, p=0,179)27. Noutro estudo mais recente de Wiemer et al.28 comparando BT com radiação beta e stents revestidos com sirolimus e seguimento a três anos, a revascularização do vaso alvo que era aos seis meses de 10,4% com BT (versus 2,3% para os stents, p=0,25) aumentou aos três anos para 46,7% (comparativamente aos 11,6% com stents, p<0,0001).
Um aspeto que vale a pena salientar neste seguimento longo é que dos cinco doentes com TVR, em três a opção foi a revascularização cirúrgica e não voltaram a ter mais eventos relacionados com o vaso alvo nos anos seguintes. Pelo contrário, nos dois doentes em que a opção foi a implantação de stents eluidores de fármacos, ambos voltaram a ter restenose clínica: um acabou por ser submetido a cirurgia e não voltou a ter eventos e o outro teve morte súbita após angioplastia de um vaso não alvo. Claro que é necessário esclarecer que nestes dois doentes em que a opção inicial não foi cirúrgica, a artéria descendente anterior não tinha doença obstrutiva significativa.
A hipótese de BT para o tratamento da restenose de stents eluidores de fármaco voltou recentemente a ser considerada, mas o seu uso é atualmente muito limitado30.
Em conclusão, a utilização da radiação intracoronária para o tratamento da restenose difusa de stents metálicos na nossa pequena experiência demonstrou‐se segura com taxa de restenose angiográfica aos nove meses e de eventos cardíacos major aos dez anos aceitável, tendo em conta as características da população tratada. Apesar de o elevado número de novas revascularizações, estas ocorreram apenas em cinco doentes e 41% dos doentes estavam livres de eventos no final do seguimento clínico, confirmando a segurança da BT a longo prazo.
LimitaçõesOs autores reconhecem as seguintes limitações ao presente trabalho:
- 1)
Trata‐se de um estudo retrospetivo observacional de centro único e com pequeno número de doentes.
- 2)
Não foi feita comparação com um grupo controlo, sendo a interpretação dos resultados feita por comparação com a literatura.
- 3)
Os doentes incluídos representam um subgrupo altamente selecionado de doentes com elevada complexidade clínica e angiográfica, seguidos ao longo de dez anos, facto a ter em linha de conta na interpretação da taxa de eventos clínicos verificada no seguimento.
- 4)
Ao descrever a experiência inicial com esta técnica, os resultados incorporam a curva de aprendizagem inerente a qualquer novo procedimento.
- 5)
Os procedimentos efetuados há dez anos podem não refletir a prática contemporânea, com diferenças nas estratégias terapêuticas e nos dispositivos empregues e refletem a evidência científica acumulada.
- 6)
A angiografia de controlo, programada para todos os doentes, independentemente da evidência de isquemia, poderá ter sobrevalorizado a incidência de novas revascularizações.
Os autores declaram que para esta investigação não se realizaram experiências em seres humanos ou animais.
Confidencialidade dos dadosOs autores declaram ter seguido os protocolos do seu centro de trabalho acerca da publicação dos dados de pacientes.
Direito à privacidade e consentimento escritoOs autores declaram ter recebido consentimento escrito dos pacientes e/ou sujeitos mencionados no artigo. O autor para correspondência deve estar na posse deste documento.
Conflito de interessesOs autores declaram não haver conflito de interesses.
Os autores agradecem à firma SOCIME Medical na pessoa do Dr. Paulo Amaro o fornecimento gracioso de todo o material específico para a BT com radiação beta. Agradecem, igualmente, ao Instituto Português de Oncologia Francisco Gentil todo o apoio na constituição da equipa multidisciplinar (Radioterapeutas L. Jorge e M. Roldão e Físicos N. Teixeira e P. Ferreira) e no armazenamento da fonte de radiação, bem como à Bristol Myers Squibb Farmacêutica Lda. o fornecimento do clopidogrel para todos os doentes até aos nove meses de seguimento angiográfico. Por fim, agradecem a todo o pessoal médico, de enfermagem, técnico e de secretariado do Serviço de Cardiologia do Hospital de Santa Cruz, em particular da Unidade de Intervenção Cardíaca e Vascular (UNICARV), por toda a colaboração na realização da técnica de BT.