Analisar a experiência adquirida em dez anos do programa de transplantação cardíaca dos Hospitais da Universidade de Coimbra.
MétodosDe novembro de 2003 a dezembro de 2013, 258 doentes com idade média de 53,0±12,7 anos (limites 3‐72 anos) e predominância do sexo masculino (78%) foram transplantados. Mais de um terço dos doentes tinha miocardiopatia isquémica (37,2%) e 36,4% idiopática. A idade média dos dadores era 34,4±11,3 anos e 195 eram do sexo masculino (76%), com disparidade de sexo entre dador e recetor (F:M) em 32% dos casos e disparidade AB0 (grupos não idênticos mas compatíveis) em 18%. A colheita foi feita à distância em 59% dos casos. Em todos os casos foi utilizada a técnica de transplantação total, com anastomose bicava, modificada neste centro. O tempo médio de isquemia foi 89,7±35,4 minutos. Todos os doentes receberam terapêutica de indução.
ResultadosA mortalidade precoce foi 4,7% (12 doentes), por falência do enxerto e acidente vascular cerebral em cinco cada, e por rejeição hiperaguda em dois. Treze doentes (5%) necessitaram de ventilação prolongada e 25 (11,8%) requereram suporte inotrópico por mais de 48 horas, sete necessitaram de implantação de pacemaker. O tempo médio de internamento foi de 15,8±15,3 dias (mediana, 12 dias). Noventa por cento dos doentes foram mantidos com terapêutica imunossupressora tripla, incluindo ciclosporina. Os restantes receberam tacrolimus. Em 23 doentes foi necessário alterar o esquema de imunossupressão devido a complicações renais e/ou neoplásicas e rejeição humoral. Todos os doentes, exceto dois, são seguidos no centro cirúrgico. Cinquenta doentes (19,4%) faleceram tardiamente por infeção (18 doentes), neoplasia (dez doentes), causa vascular (oito doentes), neuropsiquiátrica (quatro doentes), cardíaca (dois doentes) ou outras (oito doentes). Quarente e seis doentes (17,8%) tiveram episódios de rejeição celular (≥2R da ISHLT) e oito tiveram rejeição humoral (3,1%), e em 22 há evidência de doença vascular enxerto (8,5%). A sobrevivência atuarial a um, cinco, e oito anos foi de 87±2%, 78±3% e 69±4%, respetivamente.
ConclusãoNesta série de dez anos obtiveram‐se resultados equivalentes ou superiores aos referidos em experiências mais vastas e mais longas, progressivamente melhorados pela introdução de fatores suscitados pela própria experiência. Com este programa foi possível elevar e manter a taxa de transplantação cardíaca em valores acima da média europeia.
To analyze the experience gained in 10 years of the heart transplantation program of the University Hospital of Coimbra.
MethodsBetween November 2003 and December 2013, 258 patients with a mean age of 53.0±12.7 years (3‐72 years) and predominantly male (78%) were transplanted. Over a third of patients had ischemic (37.2%) and 36.4% idiopathic cardiomyopathy. The mean age of donors was 34.4±1.3 years and 195 were male (76%), with gender difference between donor and recipient in 32% of cases and ABO disparity (non‐identical groups but compatible) in 18%. Harvest was distant in 59% of cases. In all cases total heart transplantation with bicaval anastomoses, modified at this center, was used. Mean ischemia time was 89.7±35.4 minutes. All patients received induction therapy.
ResultsEarly mortality was 4.7% (12 patients) from graft failure and stroke in five patients each, and hyperacute rejection in two. Thirteen patients (5%) required prolonged ventilation, 25 (11.8%) required inotropic support for more than 48 hours, and seven required pacemaker implantation. Mean hospital stay was 15.8±15.3 days (median 12 days). Ninety percent of patients were maintained on triple immunosuppressive therapy including cyclosporine, the remainder receiving tacrolimus. In 23 patients it was necessary to change the immunosuppression protocol due to renal and/or neoplastic complications and humoral rejection. All but two patients have been followed in the Surgical Center. Fifty patients (19.4%) subsequently died from infection (18), cancer (10), vascular (eight), neuropsychiatric (four), cardiac (two) or other causes (eight). Forty‐six patients (17.8%) had episodes of cellular rejection (>2 R on the ISHLT classification), eight had humoral rejection (3.1%), and 22 have evidence of graft vascular disease (8.5%). Actuarial survival at 1, 5, and 8 years was 87±2%, 78±3% and 69±4%, respectively.
ConclusionThis 10‐year series yielded results equivalent or superior to those of centers with wider and longer experience, and have progressively improved following the introduction of changes prompted by experience. This program has made it possible to raise and maintain the rate of heart transplantation to values above the European average.
A transplantação cardíaca é a alternativa terapêutica mais eficiente na insuficiência cardíaca terminal e refratária a outros tratamentos, uma vez que não só aumenta a sobrevida, como também melhora a qualidade de vida dos doentes1–3. Porém, atualmente assistimos a uma notória diminuição do número de dadores, principal elemento restritivo da transplantação. Nos últimos anos, a redução na oferta de dadores tem obrigado a alargar os critérios de seleção, consequentemente alterando o respetivo perfil para o de um dador de mais idade, falecido por doença neurológica e frequentemente acompanhado de outro tipo de patologias e fatores ou hábitos de risco cardiovascular3,4.
Por outro lado, os avanços no tratamento médico da insuficiência cardíaca avançada têm permitido melhorar a condição dos doentes e atrasar a sua entrada nas listas para transplantação. A utilização de novos agentes inotrópicos e vasodilatadores, dos cardiodesfibrilhadores e ressincronizadores, dos sistemas de assistência mecânica circulatória transitórios e, até, o alargamento das indicações para cirurgia convencional, bem como o estabelecimento de unidades de tratamento intensivo da insuficiência cardíaca avançada (UTICA), têm contribuído para o controle ou atenuação das crises recorrentes de insuficiência cardíaca, conseguindo prolongar a vida, embora com um impacto insuficiente na qualidade de vida dos doentes5–8. Ainda assim, a transplantação continua a constituir a derradeira oportunidade de vida para doentes refratários a estas novas terapêuticas e tecnologias, não tendo sido notada uma diminuição na taxa de referenciação1,4,6.
No nosso centro, o programa de transplantação cardíaca foi iniciado em novembro de 2003 e os resultados globais dos primeiros cinco anos de atividade, tanto em termos de morbilidade como no que respeita à mortalidade, bem como a sobrevivência e qualidade de vida dos doentes transplantados, foram alvo de um relatório pormenorizado anteriormente publicado nesta revista9. Neste trabalho, pretendemos expandir essa análise aos dados de uma década e analisar a experiência entretanto colhida desta atividade.
MétodosDoentesDesde novembro de 2003 até dezembro de 2013 foram transplantados um total de 258 doentes, estando a maioria deles (71%) classificados como urgentes ou emergentes (internados na UTICA).
Na maior parte dos casos, os doentes foram diagnosticados e tratados medicamente nesta instituição antes de serem transplantados. Quase metade dos doentes (126; 48,8%) foi referenciada por instituições de saúde de fora da área natural de referência do Hospital da Universidade de Coimbra (CHUC). Após a transplantação, o pós‐operatório imediato e precoce foi realizado no próprio centro. O seguimento clínico regular e o tratamento das diversas intercorrências, a médio e longo prazo, são aqui também efetuados, por elementos da equipa cirúrgica, incluindo um especialista em medicina interna especialmente dedicado a esta atividade. Só muito esporadicamente se recorreu a assistência de centros mais próximos da residência dos doentes. Este é o caso corrente de dois doentes atualmente residentes no estrangeiro.
Em todos os casos foi realizado o cross‐match prévio, tendo sido transplantados apenas os doentes em que este exame foi negativo. Também foi efetuada a análise do painel de reacividade (PRA), que geralmente só foi conhecido após a transplantação, o que terá condicionado o esquema de imunossupressão nalguns casos.
A colheita do órgão foi sempre efetuada por elementos da equipe transplantadora. A técnica cirúrgica de transplantação utilizada foi anteriormente descrita e segue o método standard de anastomose bicava seguido na maior parte dos centros transplantadores, mas com pequenas alterações e adaptações resultantes da experiência entretanto adquirida, no sentido de minimizar o tempo de isquemia, nomeadamente com a realização precoce da anastomose aórtica e respetiva desclampagem.
O protocolo de imunossupressão utilizado de rotina consiste em terapêutica de indução com basiliximab, corticosteroides e micofenolato de mofetil oral, imediatamente antes e durante a intervenção, seguida de imunossupressão de manutenção tripla com corticosteroides, micofenolato de mofetil e inibidores da calcineurina, ciclosporina na maior parte dos casos, cujas doses são determinadas tendo em conta diferentes fatores, como os respetivos níveis séricos, o valor do PRA, o resultado das biópsias endomiocárdicas seriadas e outros elementos de ordem clínica.
Análise estatísticaDesde o início do programa, e com conhecimento e consentimento dos doentes, está a ser realizada uma análise simultaneamente retrospetiva e prospetiva dos resultados, consistindo na recolha dos dados de ordem clínica relativos ao período pré e peritransplante, bem como os de intercorrências clínicas no período pós‐transplante, utilizando uma extensa base de dados construída em conjunto com a Sociedade Portuguesa da Transplantação (SPT).
As variáveis contínuas são apresentadas como média ± desvio padrão. As variáveis categóricas são expressas em frequências e percentagens. A sobrevivência global e por grupos foi avaliada pelo método de Kaplan‐Meier, tendo o significado estatístico sido analisado através do teste de Log Rank. Valores de p <0,05 foram considerados estatisticamente significativos.
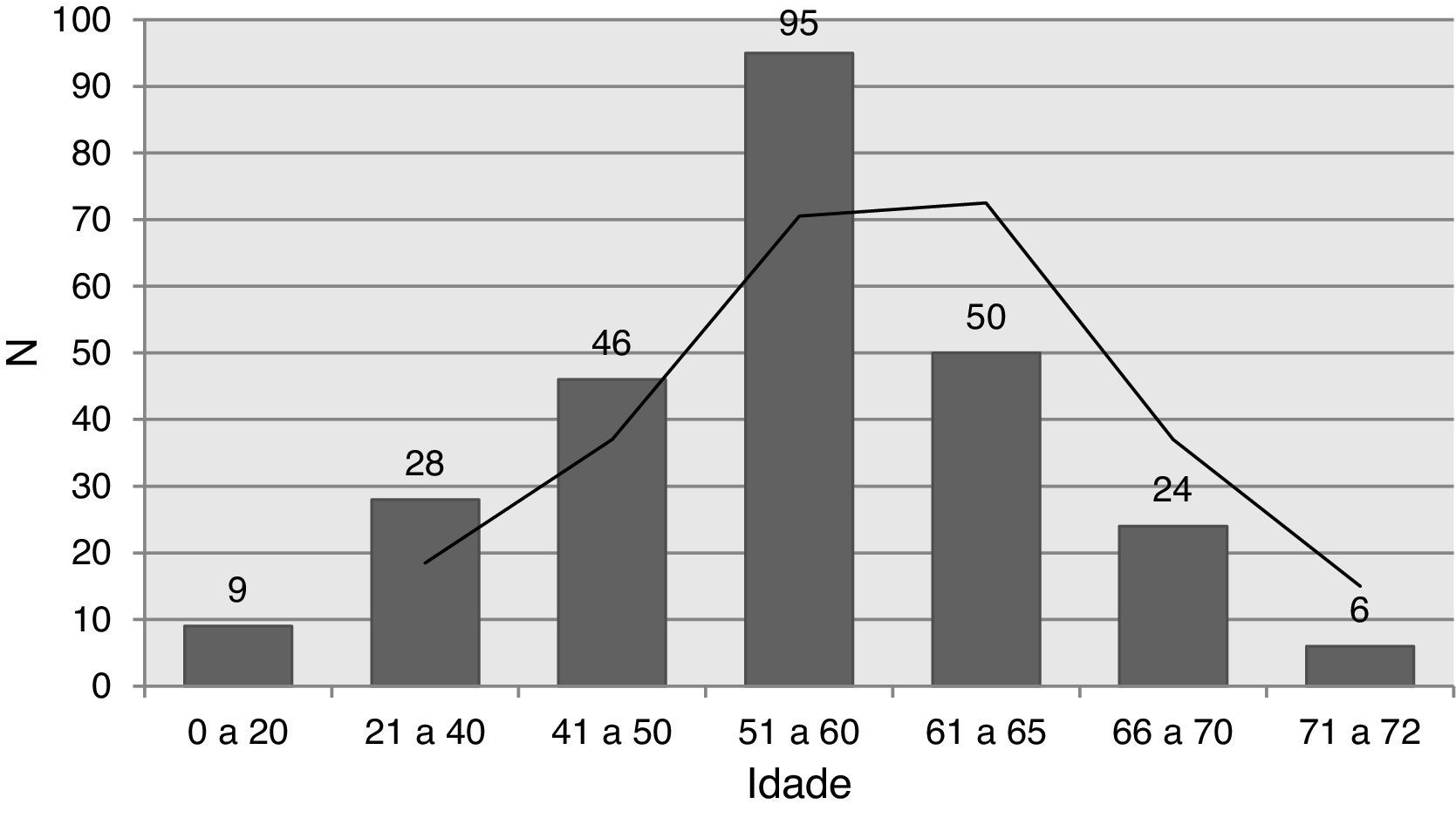
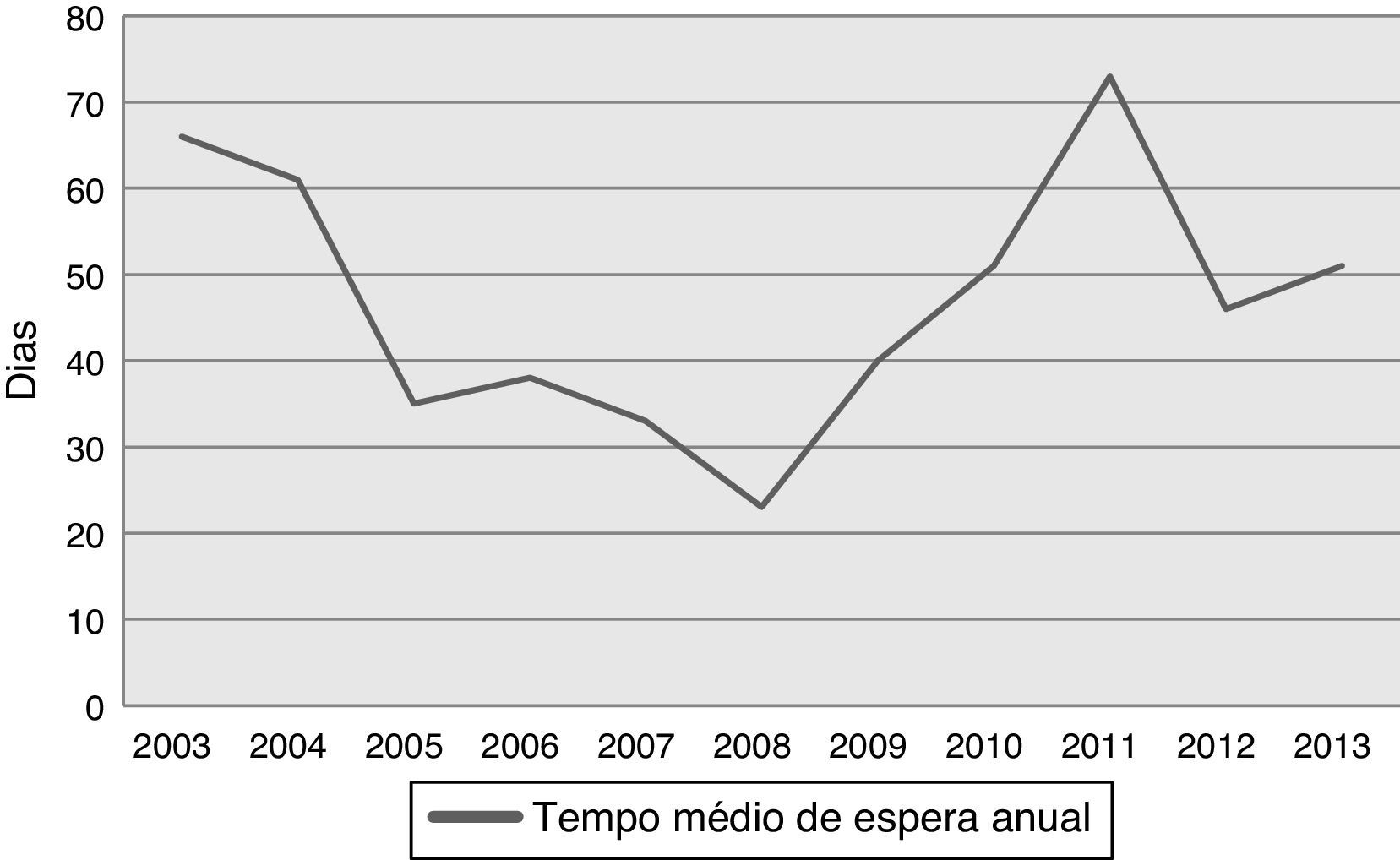
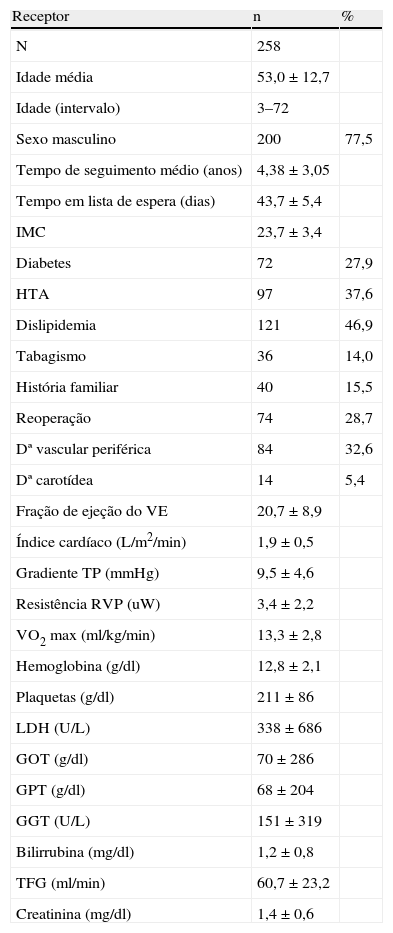
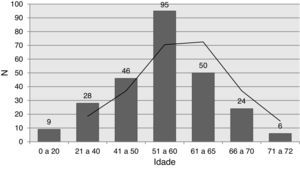
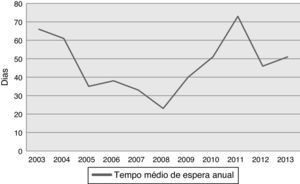
ResultadosDoentesA idade média dos 258 doentes era 53,0±12,7 anos, com um intervalo de 3‐72 anos e predominância do sexo masculino (77,5%) (Tabela 1). A distribuição por idade dos recetores está representada na Figura 1, tendo a maioria dos doentes entre 40‐65 anos. Foram transplantados seis doentes com mais de 70 anos. O tempo médio de espera na lista para transplantação foi 43,7±45,4 dias, com tendência para aumentar nos últimos anos (Figura 2).
Características demográficas e clínicas dos doentes transplantados
| Receptor | n | % |
| N | 258 | |
| Idade média | 53,0±12,7 | |
| Idade (intervalo) | 3–72 | |
| Sexo masculino | 200 | 77,5 |
| Tempo de seguimento médio (anos) | 4,38±3,05 | |
| Tempo em lista de espera (dias) | 43,7±5,4 | |
| IMC | 23,7±3,4 | |
| Diabetes | 72 | 27,9 |
| HTA | 97 | 37,6 |
| Dislipidemia | 121 | 46,9 |
| Tabagismo | 36 | 14,0 |
| História familiar | 40 | 15,5 |
| Reoperação | 74 | 28,7 |
| Dª vascular periférica | 84 | 32,6 |
| Dª carotídea | 14 | 5,4 |
| Fração de ejeção do VE | 20,7±8,9 | |
| Índice cardíaco (L/m2/min) | 1,9±0,5 | |
| Gradiente TP (mmHg) | 9,5±4,6 | |
| Resistência RVP (uW) | 3,4±2,2 | |
| VO2 max (ml/kg/min) | 13,3±2,8 | |
| Hemoglobina (g/dl) | 12,8±2,1 | |
| Plaquetas (g/dl) | 211±86 | |
| LDH (U/L) | 338±686 | |
| GOT (g/dl) | 70±286 | |
| GPT (g/dl) | 68±204 | |
| GGT (U/L) | 151±319 | |
| Bilirrubina (mg/dl) | 1,2±0,8 | |
| TFG (ml/min) | 60,7±23,2 | |
| Creatinina (mg/dl) | 1,4±0,6 |
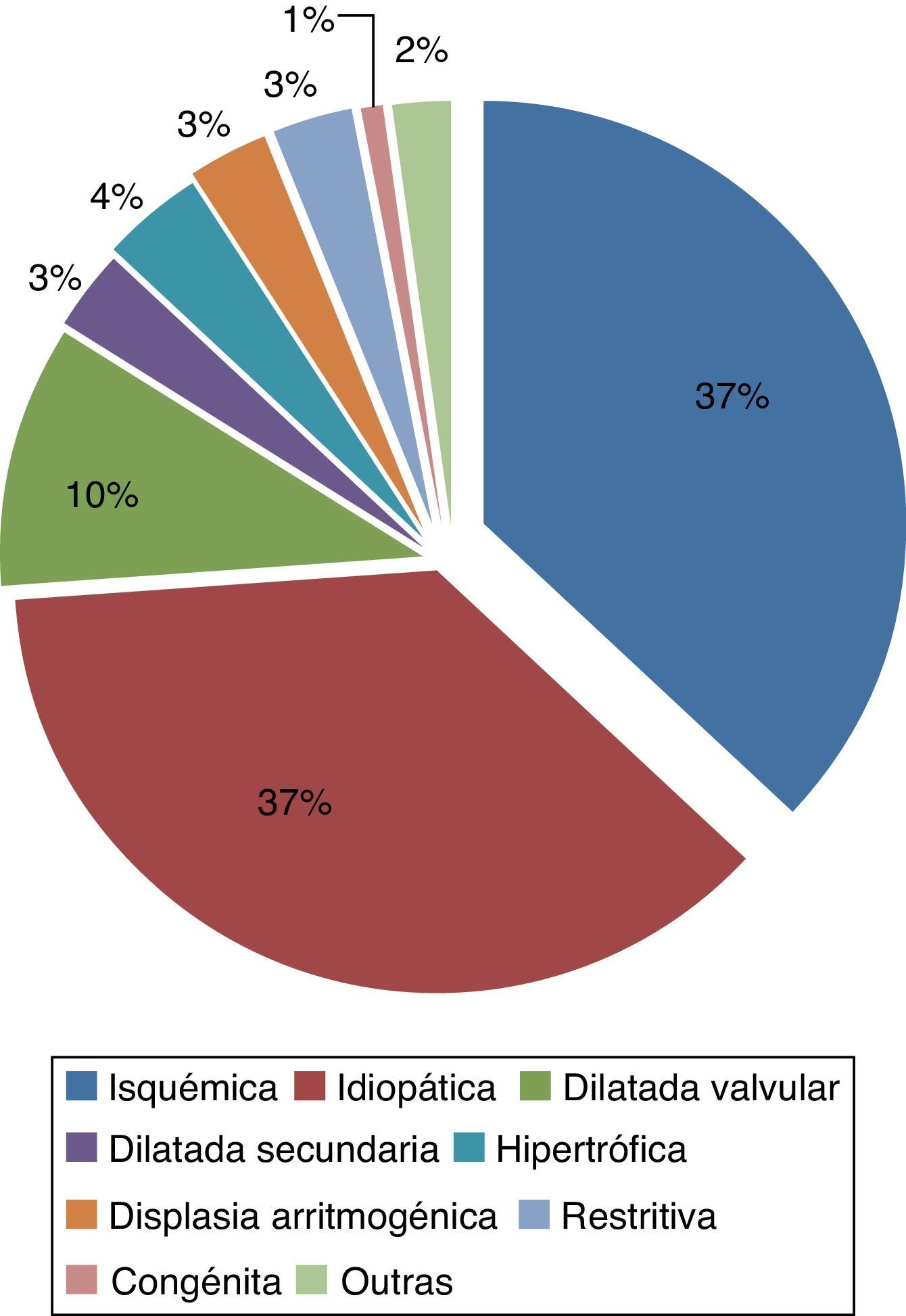
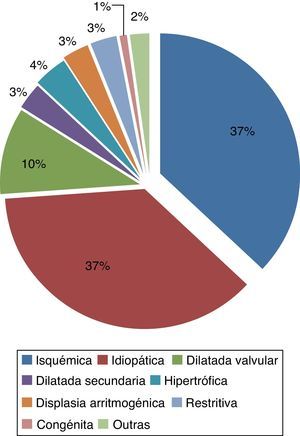
A maior parte dos doentes sofria de cardiomiopatia isquémica (37,2%), seguido da etiologia idiopática (36,4%) e 28,7% tinham tido cirurgia cardíaca prévia (Figura 3).
O índice de massa corporal médio da população à data da transplantação era de 23,7±3,4kg/m2. Quase um terço dos doentes eram diabéticos (27,9%) e a uma percentagem significativa estavam associadas a hipertensão arterial (37,6%), a dislipidemia (46,9%) e o tabagismo (14,0%). Ainda no campo das comorbilidades, registou‐se doença vascular periférica em 32,6% dos doentes e doença carotídea em 5,4%.
A média da fração de ejeção do ventrículo esquerdo era 20,7±8,9%. A pressão sistólica da artéria pulmonar era 48,2±15,3mmHg, as resistências vasculares pulmonares 3,4±2,2 unidades Wood e o gradiente transpulmonar 9,5±4,6mmHg. A creatinina basal era 1,4±0,6 (0,5‐5,6) mg/dl, a hemoglobina 12,8±2,1g/l e a desidrogenase láctica 338±686U/l.
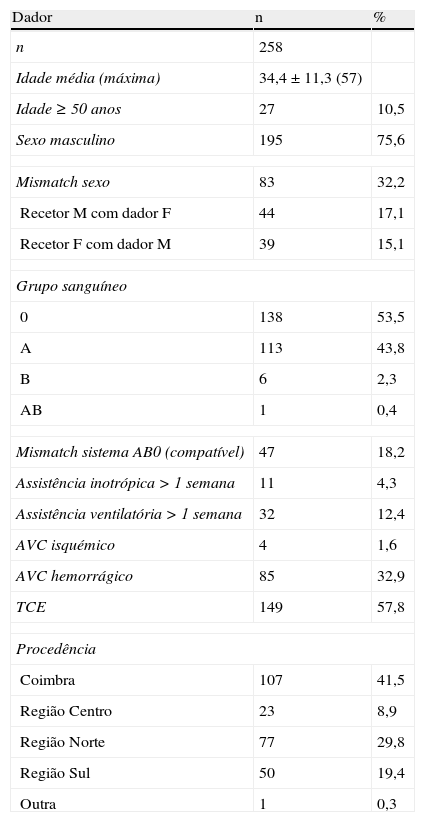
DadoresAs características demográficas e clínicas dos dadores estão detalhadas na Tabela 2. A idade média era 34,4±11,3 anos, o sexo masculino (75,6%) e o grupo sanguíneo 0 (53,5%) foram predominantes. A causa de morte foi maioritariamente traumática (57,8%), seguida de AVC hemorrágico (32,9%), mas com uma tendência crescente no número de dadores vítimas de acidente cerebrovascular, que representam quase 35% da totalidade da série, tendo‐se atualmente já invertido a razão causa traumática/causa neurológica primária.
Características demográficas e clínicas dos dadores
| Dador | n | % |
| n | 258 | |
| Idade média (máxima) | 34,4±11,3 (57) | |
| Idade ≥50 anos | 27 | 10,5 |
| Sexo masculino | 195 | 75,6 |
| Mismatch sexo | 83 | 32,2 |
| Recetor M com dador F | 44 | 17,1 |
| Recetor F com dador M | 39 | 15,1 |
| Grupo sanguíneo | ||
| 0 | 138 | 53,5 |
| A | 113 | 43,8 |
| B | 6 | 2,3 |
| AB | 1 | 0,4 |
| Mismatch sistema AB0 (compatível) | 47 | 18,2 |
| Assistência inotrópica >1 semana | 11 | 4,3 |
| Assistência ventilatória >1 semana | 32 | 12,4 |
| AVC isquémico | 4 | 1,6 |
| AVC hemorrágico | 85 | 32,9 |
| TCE | 149 | 57,8 |
| Procedência | ||
| Coimbra | 107 | 41,5 |
| Região Centro | 23 | 8,9 |
| Região Norte | 77 | 29,8 |
| Região Sul | 50 | 19,4 |
| Outra | 1 | 0,3 |
Um número significativo de dadores estava com apoio ventilatório ou inotrópico prolongado (mais de uma semana; 12,4 e 4,3%, respetivamente).
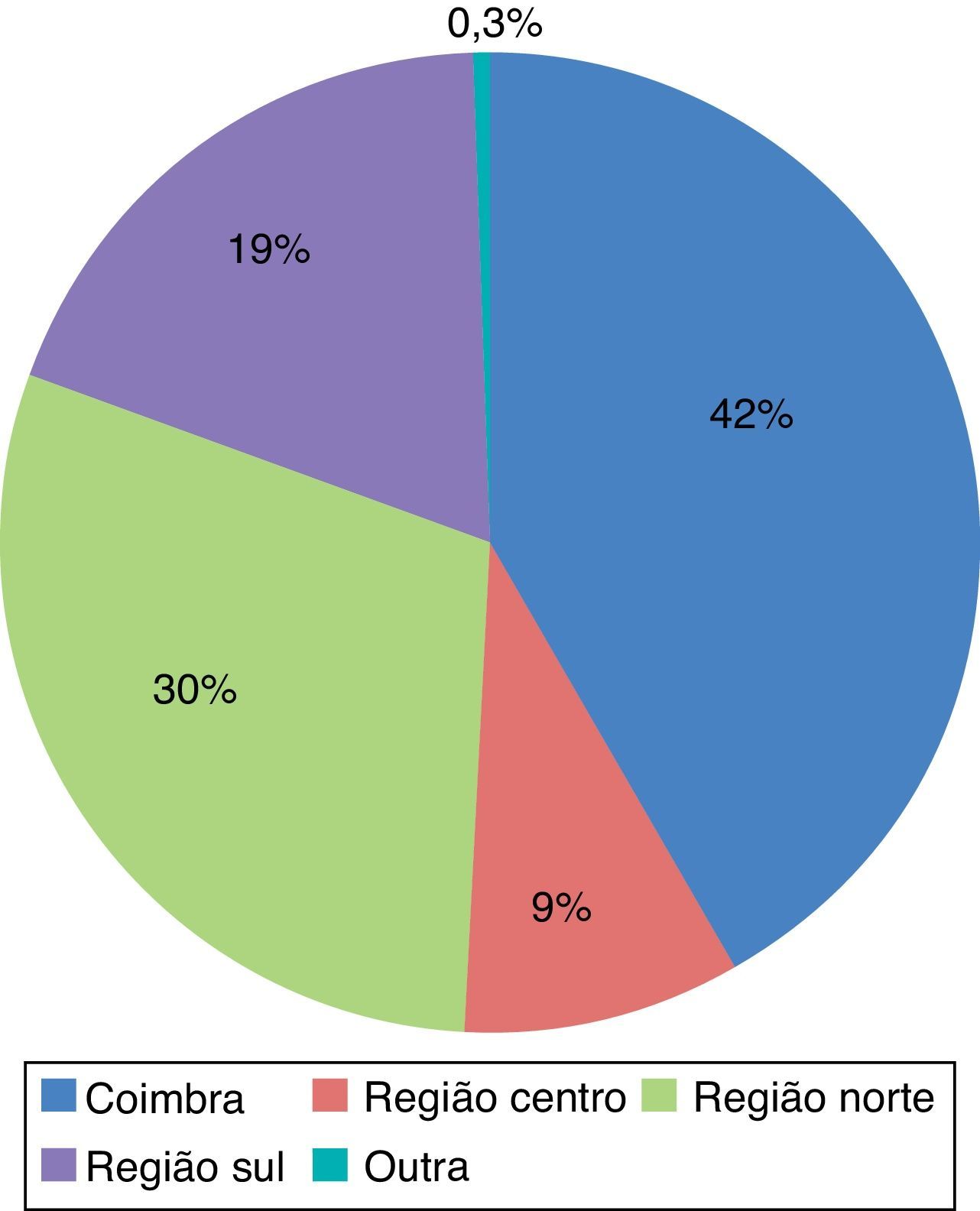
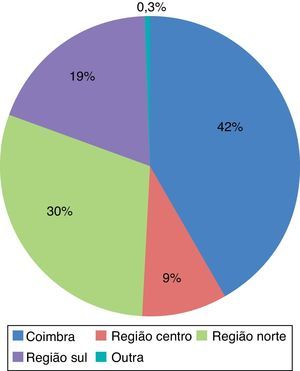
A maioria das colheitas foi realizada nos hospitais de fora de Coimbra (58,5%) e a principal origem à distância foi a região Norte, que contribui com 29,8% dos dadores, tendo sido feita uma colheita na Região Autónoma dos Açores (Figura 4). A média da distância de colheita foi de 97,6±100,9km.
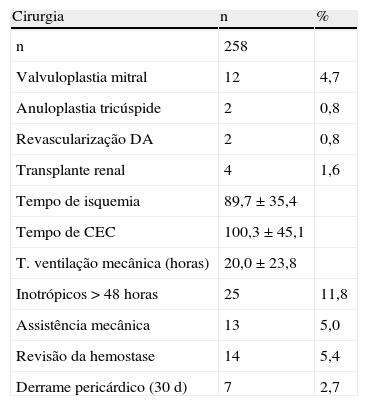
Cirurgia e unidade de cuidados intensivosO tempo médio de isquemia foi 89,7±35,4 minutos, sendo inferior a 45 minutos em todos os casos com colheita local. O tempo de circulação extracorpórea foi 100,3±45,1 minutos. Durante a transplantação foi associada outra cirurgia no coração do dador em 16 casos (6,2%). Assim, foi efetuada valvuloplastia mitral em 12 doentes (4,7%), valvuloplastia tricúspide em dois (0,8%; isolada ou associada à mitral num doente cada) e revascularização da artéria descendente anterior em dois doentes (0,8%). Num outro doente foi necessário proceder à substituição da aorta ascendente. Em quatro doentes (1,6%), que aguardavam transplantação renal, esta foi efetuada simultaneamente com a cardíaca (Tabela 3).
Procedimento cirúrgico
| Cirurgia | n | % |
| n | 258 | |
| Valvuloplastia mitral | 12 | 4,7 |
| Anuloplastia tricúspide | 2 | 0,8 |
| Revascularização DA | 2 | 0,8 |
| Transplante renal | 4 | 1,6 |
| Tempo de isquemia | 89,7±35,4 | |
| Tempo de CEC | 100,3±45,1 | |
| T. ventilação mecânica (horas) | 20,0±23,8 | |
| Inotrópicos >48 horas | 25 | 11,8 |
| Assistência mecânica | 13 | 5,0 |
| Revisão da hemostase | 14 | 5,4 |
| Derrame pericárdico (30d) | 7 | 2,7 |
A maioria dos doentes foram extubados cerca de 12 horas após a intervenção e o tempo médio de ventilação mecânica foi de 20,0±23,8 horas. Disfunção ventricular pós‐transplante, requerendo suporte inotrópico prolongado, afetou 11,8% dos doentes e em 13 destes (5,0%) o suporte inotrópico revelou‐se insuficiente, necessitando de suporte mecânico por balão intra‐aórtico, assistência ventricular esquerda ou ECMO, segundo as situações.
Rejeição e complicações associadasNoventa por cento dos doentes foram mantidos com terapêutica imunossupressora tripla, incluindo ciclosporina. Os restantes receberam tacrolimus em várias combinações. Em 23 doentes foi necessário alterar o esquema de imunossupressão inicial devido a complicações renais e/ou neoplásicas e rejeição humoral.
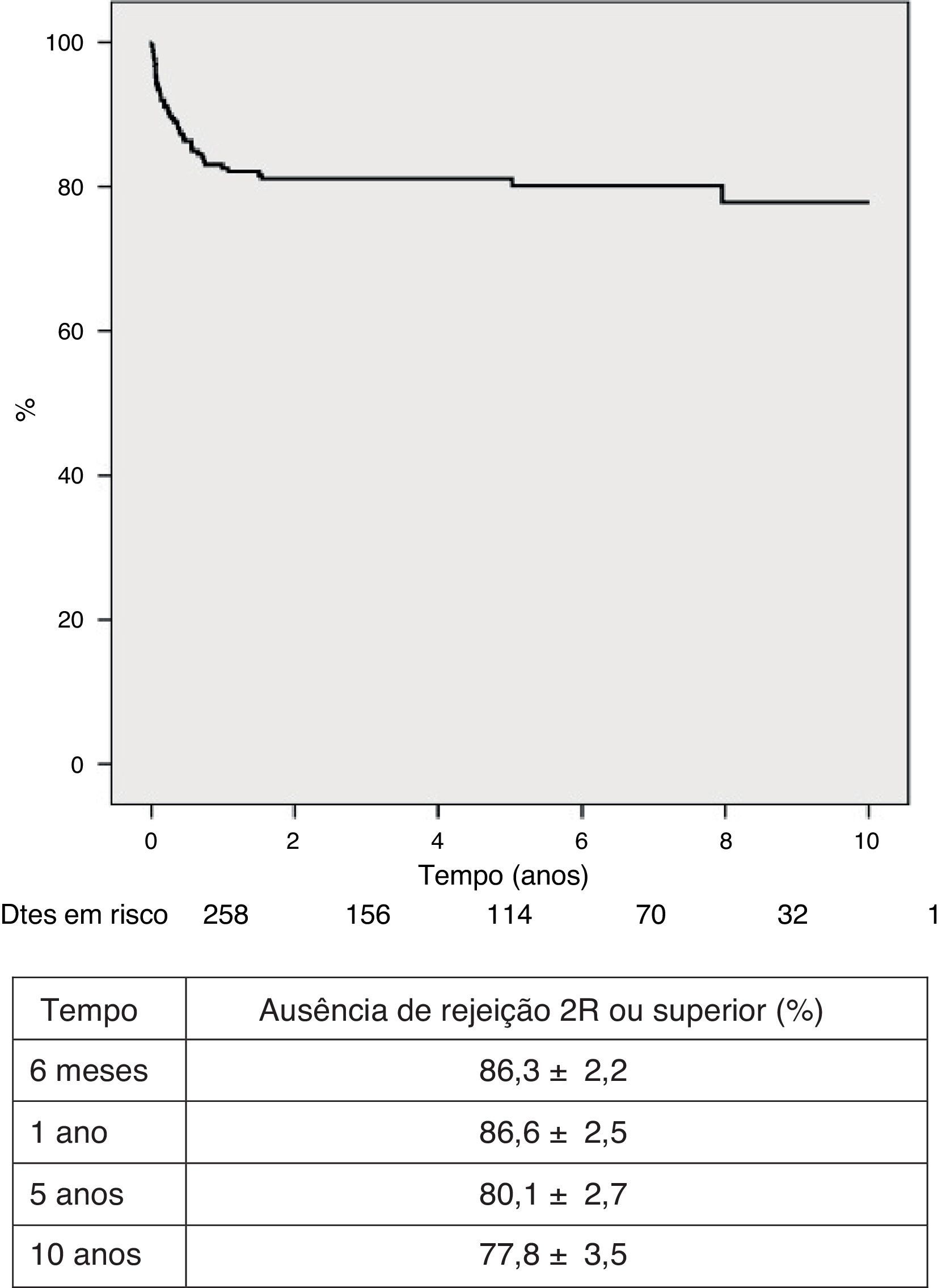
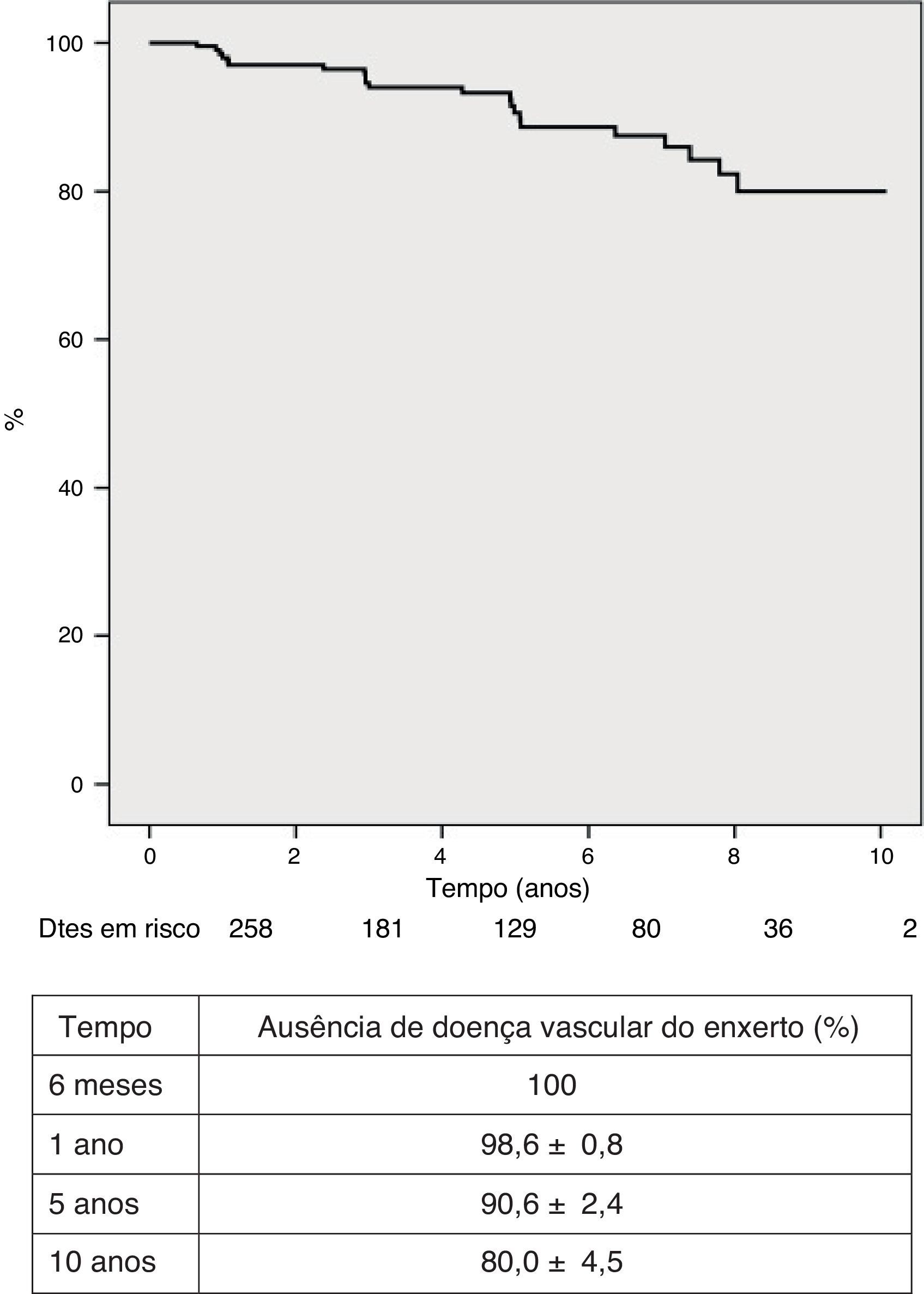
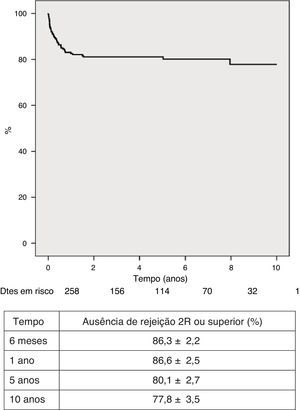
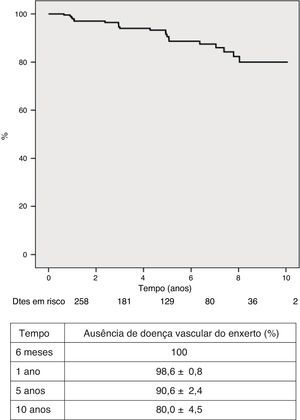
Regularmente, foram realizadas biópsias endomiocárdicas, observação ecocardiográfica e avaliação angiográfica para diagnóstico de rejeição. Quarenta e seis doentes (17,8%) sofreram 60 episódios de rejeição ≥2R da escala da ISHLT, requerendo terapêutica de pulso com corticosteroides e/ou ajustamento das doses de imunossupressores. Cento e sete doentes (41,5%) não tiveram nenhum episódio de rejeição celular (0R). Os restantes tiveram pelo menos um episódio de rejeição ligeira (1R) que não necessitou de tratamento. A maior incidência de rejeição ≥2R aconteceu durante o primeiro ano pós‐transplantação, com uma tendência a diminuir progressivamente nos anos subsequentes. A sobrevivência livre de rejeição 2R ou superior aos seis meses e a um e cinco anos foi de 86,3±2,2%, 82,6±2,5% e 80,1±2,7%, respetivamente (figura 5). Em 8 doentes (3,1%) foi observada rejeição humoral e doença vascular do enxerto (DVE; diagnosticada por angiografia coronária, como algum grau de irregularidade de novo nos grandes vasos coronários ou dos seus ramos principais, ainda que a lesão seja inferior a 50%) foi diagnosticada em 22 (8,5%), sendo ainda de grau ligeiro na maior parte dos casos. A sobrevivência livre de DVE aos dez anos foi 80,0±4,5% (Figura 6).
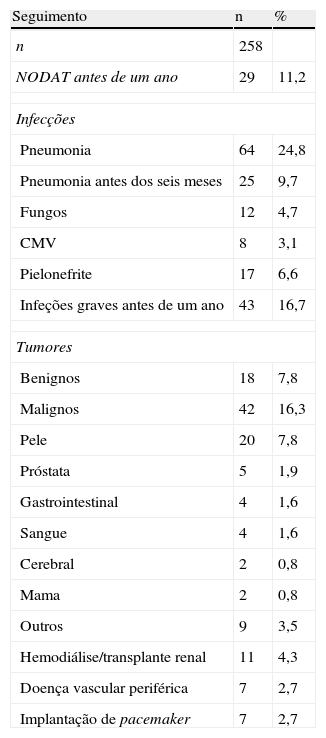
Outra morbilidadeTodos os doentes, exceto dois, foram seguidos no centro cirúrgico, ainda assim, com informação completa de todos. O tempo de seguimento médio foi de 4,38±3,05 anos. Trinta e três doentes (12,8%) desenvolveram diabetes de novo (new onset diabetes after transplantation [NODAT]), 29 dos quais no primeiro ano pós‐transplantação. Infeções graves durante os primeiros 12 meses após a transplantação, que necessitaram de internamento e tratamento antibiótico endovenoso dirigido ocorreram em 43 doentes (16,7%). As pneumonias antes dos seis meses foram o principal tipo de infeção registado (9,7% dos doentes) (Tabela 4).
Complicações pós‐operatórias e durante o follow‐up
| Seguimento | n | % |
| n | 258 | |
| NODAT antes de um ano | 29 | 11,2 |
| Infecções | ||
| Pneumonia | 64 | 24,8 |
| Pneumonia antes dos seis meses | 25 | 9,7 |
| Fungos | 12 | 4,7 |
| CMV | 8 | 3,1 |
| Pielonefrite | 17 | 6,6 |
| Infeções graves antes de um ano | 43 | 16,7 |
| Tumores | ||
| Benignos | 18 | 7,8 |
| Malignos | 42 | 16,3 |
| Pele | 20 | 7,8 |
| Próstata | 5 | 1,9 |
| Gastrointestinal | 4 | 1,6 |
| Sangue | 4 | 1,6 |
| Cerebral | 2 | 0,8 |
| Mama | 2 | 0,8 |
| Outros | 9 | 3,5 |
| Hemodiálise/transplante renal | 11 | 4,3 |
| Doença vascular periférica | 7 | 2,7 |
| Implantação de pacemaker | 7 | 2,7 |
NODAT: diabetes de novo (new onset diabetes after transplantation).
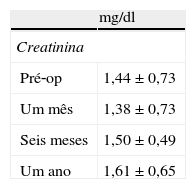
Geralmente observou‐se uma recuperação da função renal nos primeiros meses pós‐transplante, melhoria que persistiu durante o primeiro ano. Apenas cinco doentes (1,9%) necessitaram de terapia de substituição renal precoce (≤1mês pós‐transplante). Porém, a partir dos 12 meses após a operação foi notória uma deterioração progressiva e persistente da função renal, como consequência da terapêutica imunossupressora e antibiótica (Tabela 5). Três doentes foram entretanto submetidos a transplantação renal e outros dois encontram‐se sujeitos a terapêutica de substituição e aguardam transplantação.
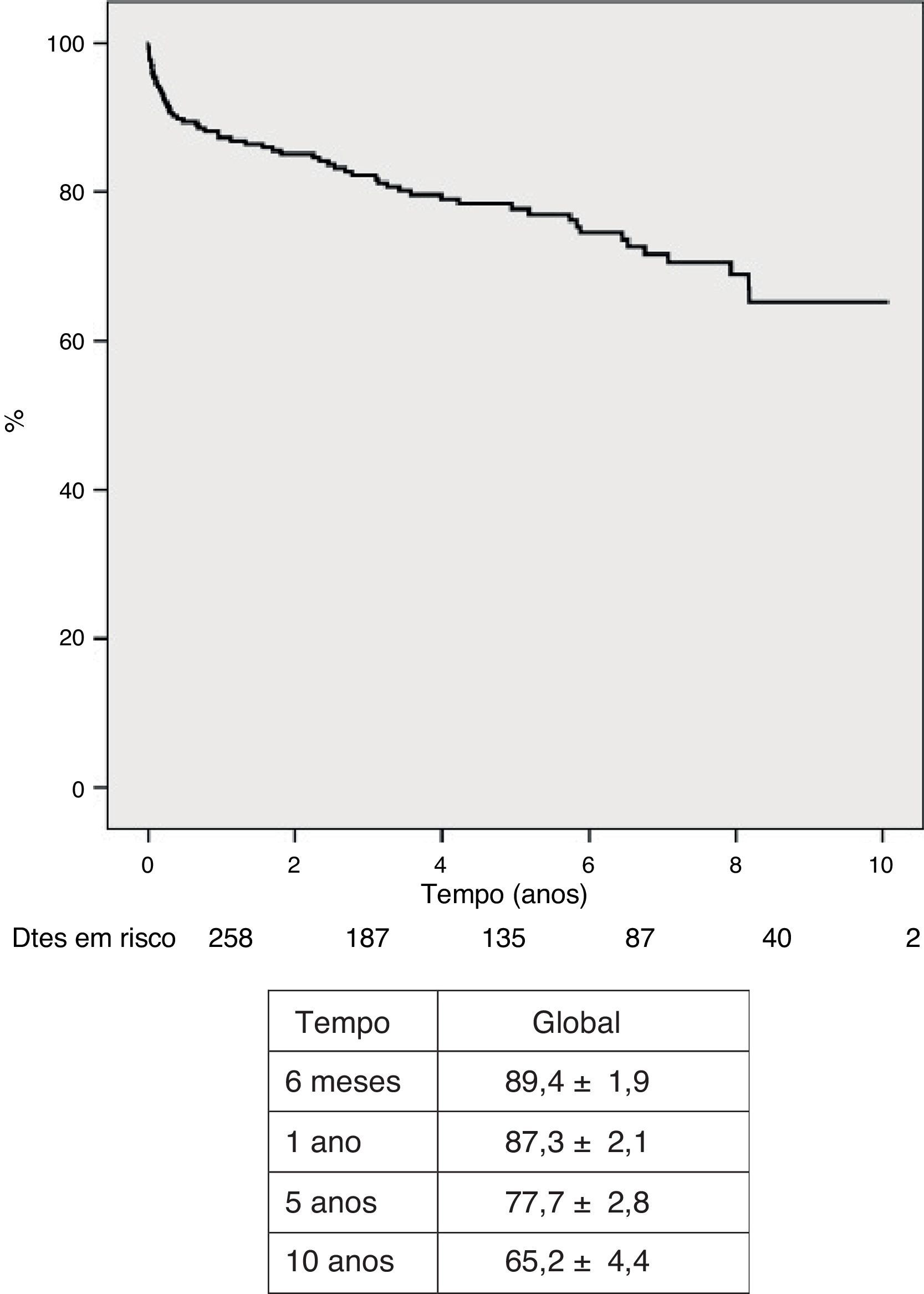
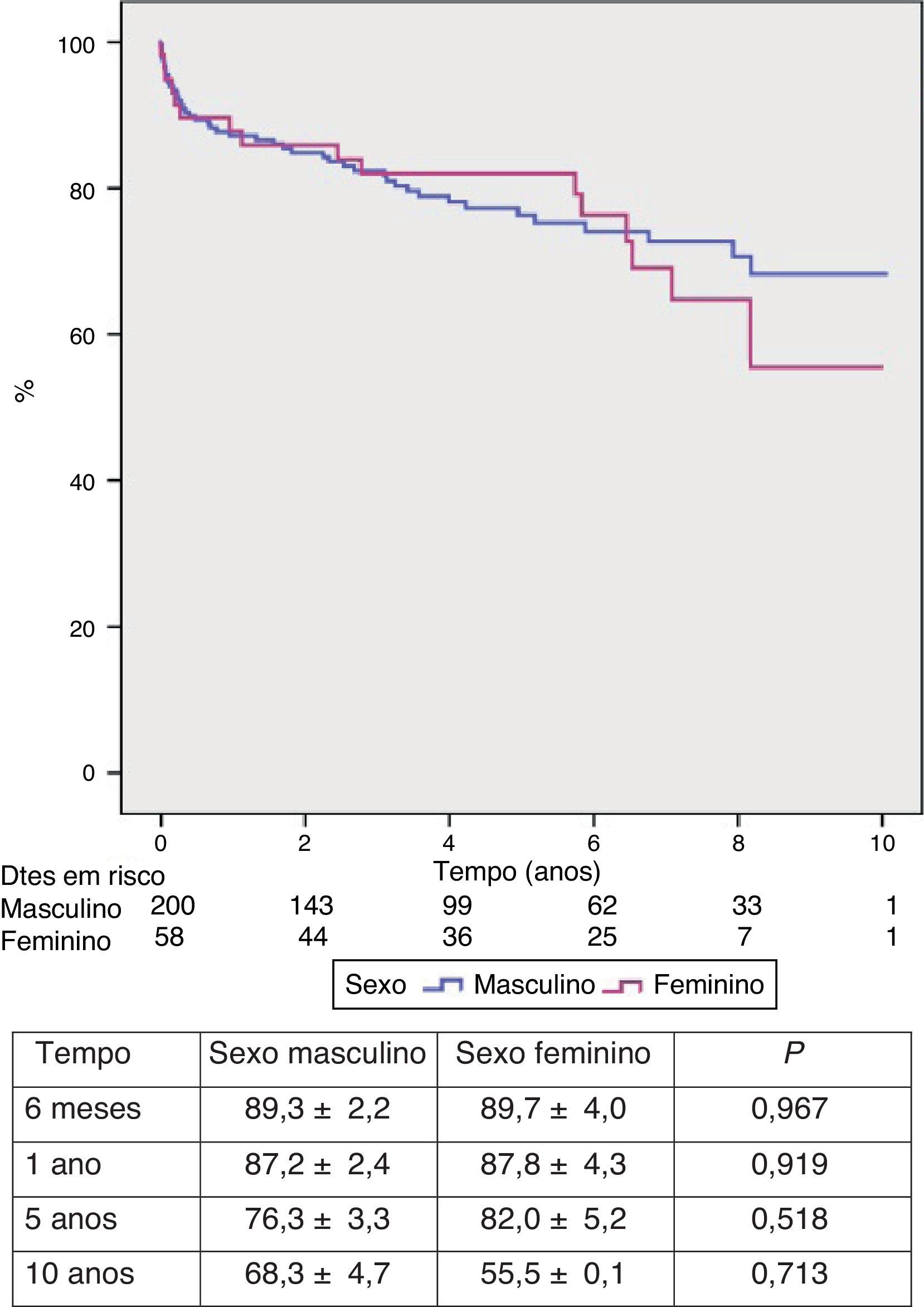
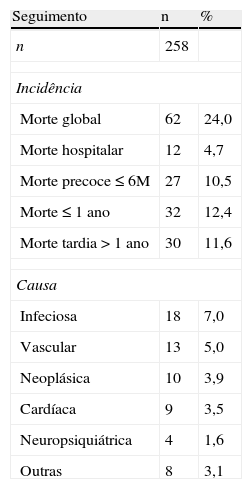
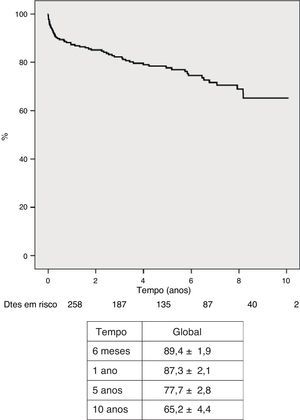
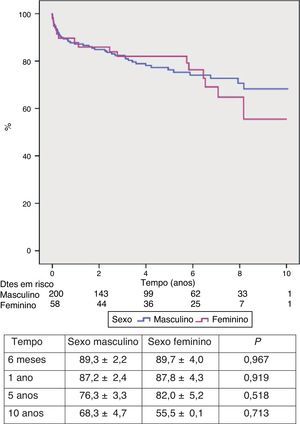
Mortalidade e sobrevidaDoze doentes (4,7%) faleceram nos primeiros 30 dias ou durante o internamento, por falência do enxerto e acidente vascular cerebral em cinco cada, e por rejeição hiperaguda em dois, e outros 50 faleceram durante o follow‐up, para uma mortalidade global de 24,0% (tabela 6). As principais causas de morte tardia foram as complicações infeciosas (7,0%), seguidas das vasculares (5,0%), neoplásicas (3,9%) e cardíacas (3,5%). A sobrevivência global foi de 87,3±1,9% a um ano, 77,7±2,8% aos cinco anos, 68,9±3,8% aos oito anos e 65,2±4,4% aos dez anos (Figura 7). Não se observou diferença significativa na sobrevivência entre doentes dos dois sexos (Figura 8).
Incidência e causas de mortalidade
| Seguimento | n | % |
| n | 258 | |
| Incidência | ||
| Morte global | 62 | 24,0 |
| Morte hospitalar | 12 | 4,7 |
| Morte precoce ≤6M | 27 | 10,5 |
| Morte ≤1 ano | 32 | 12,4 |
| Morte tardia >1 ano | 30 | 11,6 |
| Causa | ||
| Infeciosa | 18 | 7,0 |
| Vascular | 13 | 5,0 |
| Neoplásica | 10 | 3,9 |
| Cardíaca | 9 | 3,5 |
| Neuropsiquiátrica | 4 | 1,6 |
| Outras | 8 | 3,1 |
A transplantação cardíaca tem‐se afirmado como uma modalidade de tratamento eficaz da insuficiência cardíaca terminal e refratária. Contudo, esta intervenção está associada a um conjunto de complicações graves, algumas potencialmente fatais, que fazem com este seja efetivamente um procedimento paliativo a médio e longo prazo. Na atualidade, a sobrevivência a dez anos é de cerca de 50‐60% e a sobrevida média dos sobreviventes à transplantação é de 12‐13 anos1,3.
O programa de transplantação cardíaca do CHUC foi iniciado em novembro de 2003. Os dados dos doentes transplantados nos primeiros cinco anos de atividade foram apresentados e analisados em relatório então publicado na RPC9. Dele constava também uma resenha histórica, bem como outras considerações sobre a atividade de transplantação cardíaca em Portugal e seu contexto europeu, de que recomendamos a leitura, pelo que não abordaremos aqui esse assunto.
No presente trabalho analisamos os resultados obtidos em 258 doentes transplantados na primeira década completa deste programa. Foram, pois, realizados uma média de 25 transplantes anualmente, constituindo o cumprimento global dos objetivos então definidos, considerando‐se esta elevada atividade transplantadora vantajosa, certamente com impacto nos resultados pós‐transplantação, sobretudo nos casos da maior urgência ou de maior risco. Trata‐se, efetivamente, da maior experiência acumulada por qualquer centro nacional. A relação entre a qualidade dos resultados e o volume da atividade de transplantação está bem estabelecida10–12. Por outro lado, a experiência assim adquirida tem permitido o alargamento das indicações, a exploração de alternativas técnicas e o aproveitamento de dadores marginais, deste modo estendendo as fronteiras da doação.
Tem‐se assistido a um aumento progressivo não só da idade média dos recetores como do número de doentes que no momento da transplantação estavam internados por insuficiência cardíaca descompensada, necessitando de apoio farmacológico intensivo e, por vezes, de apoio mecânico cardiocirculatório e ventilatório. O resultado é um crescente número de recetores em pior estado clínico, situação que não só eleva o grau de urgência para a transplantação, mas também tende a aumentar o risco de insucesso.
A escala de prioridade para a transplantação cardíaca utilizada no nosso país (Tabela 7), inicialmente implementada pela Organização Portuguesa de Transplantação (OPT), subsequentemente pela ASST e recentemente pelo IPST, baseada na definição da situação clínica do candidato à data da inscrição na lista de espera, tendo como consequência que o doente mais crítico passe à frente de outros cuja situação clínica lhes permita aguardar mais tempo, também contribui para esta situação. Contudo, esta escala e escalas similares utilizadas noutros países não esclarecem nem quantificam o perfil de risco dos doentes. É sabido que os resultados imediatos da transplantação são muito sensíveis à qualidade dos órgãos do dador e ao estado clínico do candidato13,14. Estes são os principais fatores responsáveis por alguns resultados insatisfatórios na fase imediata à transplantação15,16.
Tabela de graus de prioridade para transplantação em uso no nosso país
| Graus de prioridade | ||
| i | Emergente | Falência aguda do enxerto |
| ii | Choque cardiogénico com assistência ventricular (CEC, ECMO, VAD) | |
| iii | Choque cardiogénico com balão intra‐aórtico | |
| iv | Choque cardiogénico e suporte ventilatório | |
| v | Urgente | Internado com inotrópicos ou arritmias malignas ou hemodiálise |
| vi | Internado na UCI para tratamento da ICC, duas ou mais vezes, nos últimos seis meses | |
| vii | Não urgente | |
Pelo contrário, os doentes em mais baixo grau de prioridade beneficiam do ambiente domiciliar e acompanhamento familiar, e de uma maior mobilidade, factos que contribuem para uma otimização do estado psicológico e físico, e para uma redução drástica da incidência e gravidade das infeções nosocomiais pós‐transplantação. Indubitavelmente, estes são aspetos que ajudam a diminuir o potencial de risco do doente17. Mas Lietz e Mokadam demonstraram que durante o tempo de espera para transplantação há uma deterioração da condição clínica em 32‐48% dos pacientes em status 2da United Network for Organ Sharing (UNOS, organização privada que coordena o sistema de transplantação de órgãos americano), equivalente ao nosso grau de prioridade VI‐VII5,18. Os doentes deste grupo chegam, pois, à transplantação em situação clínica adversa com estados sintomáticos de instabilidade intermitente, descompensações recorrentes e frequentes ou sintomas crónicos persistentes frequentemente associados a uma elevada morbilidade2.
Um outro grupo de risco é o dos doentes diabéticos. Como seria de esperar nesta população, mais de um quarto dos doentes (27,9%) eram diabéticos na altura da transplantação. Por outro lado, 29 doentes (11,27%) adquiriram diabetes de novo no primeiro ano após a transplantação. A relação entre a imunossupressão, especialmente os corticosteroides e o tacrolimus, e o agravamento ou aparecimento de novo da diabetes melitus é bem conhecida e a diabetes é um dos mais importantes fatores de risco para o desenvolvimento da arteriosclerose que envolve tanto a circulação coronária como a sistémica19. Em trabalhos anteriormente publicados não encontrámos diferenças significativas, tanto no que respeita à morbilidade como no que concerne à mortalidade, entre os doentes diabéticos e os não diabéticos, até cinco anos após a transplantação20. Contudo, essa situação parece modificar‐se a mais longo prazo21.
A diabetes é também importante na génese e propagação das infeções. Mais do que a rejeição aguda, que hoje raramente é mortal, as infeções são atualmente a principal causa de morbilidade e mortalidade tardia após a transplantação. Nesta série, 43 doentes (16,7%) sofreram de infeções graves durante o primeiro ano, na maior parte dos casos pneumonias, requerendo internamento e tratamento antibiótico endovenoso, e foram a principal causa de mortalidade tardia, seguidas das causas vasculares e neoplásicas. É provável que tal se possa atribuir a excesso de terapêutica imunossupressora, havendo já centros com excelentes resultados com protocolos imunossupressores muito atenuados em relação aos protocolos clássicos22. No nosso centro o protocolo inicial foi recentemente modificado, sendo ainda cedo para avaliar o impacto nas principais complicações ligadas à transplantação.
Frequentemente relacionada com a rejeição crónica é a DVE que, contudo, continua a ser uma entidade de génese e comportamento largamente desconhecidos. Esta complicação aparece tardiamente, geralmente a partir dos cinco anos, e conduz a disfunção grave progressiva do enxerto, até à perda total, com a morte do doente, a menos que seja retransplantado, o que nesta área é uma raridade23. Estranhamente, nesta série, a maior parte dos casos de DVE foram diagnosticados nos primeiros três anos após a transplantação. No entanto, quando diagnosticada precocemente, a evolução da DVE pode ser significativamente atenuada pela alteração do regime imunossupressor, especialmente com a introdução dos inibidores de mTOR (sirolimus e everolimus).
Num esforço para aumentar o número de dadores, tem‐se vindo progressivamente a aumentar o limite de idade. No entanto, a utilização de dadores mais velhos não parece ser tão relevante como seria de esperar e noutro estudo baseado nesta nossa experiência demonstrámos idêntica sobrevivência entre os recipientes de corações de dadores mais idosos, mesmo em recipientes jovens, pelo que a idade dos dadores, pelo menos até aos 60 anos, não parece ser fator limitativo24–27. Recomenda‐se, contudo, que estes corações não sejam submetidos a tempos de isquemia prolongados28. Por isso, nestas condições temos privilegiado dadores referenciados por instituições mais próximas do nosso centro.
A utilização de corações com ligeiras anomalias estruturais, mas passíveis de correção, enquadra‐se também no esforço para aumentar o aproveitamento de dadores: 12 doentes receberam corações com graus ligeiros a moderados de doença mitral, conhecida antes da colheita em todos menos um, que foi corrigida antes da implantação, e dois doentes receberam uma anuloplastia tricúspide. Finalmente, dois doentes foram submetidos a revascularização da artéria descendente anterior, num deles utilizando a artéria mamária usada na intervenção prévia de revascularização coronária. Alguns destes casos foram alvo de publicações anteriores29,30. Até ao momento, todos os doentes estão bem, sem complicações relacionadas com estes procedimentos, com exceção de um que faleceu algumas semanas pós‐transplantação por AVC.
Em 17% dos nossos casos verificou‐se uma discrepância de sexo (dador feminino em recetor masculino). Esta discrepância tem sido frequentemente associada a resultados inferiores31. No entanto, nesta série não foi observada diferença significativa da incidência de complicações e mortalidade nos casos de discrepância de sexo, quando comparados com os doentes sem discrepância, pelo que continua, neste programa, a não ser causa de rejeição de dadores, desde que observadas outras regras de seleção, como uma adequada correlação morfológica (peso e IMC).
A sobrevida dos doentes transplantados foi de 87% no primeiro ano, 78% aos cinco anos e 65% aos dez anos, o que se compara favoravelmente com os resultados de outras séries publicadas, especialmente do registo de mais de 100 000 casos da International Society for Heart and Lung Transplantation (ISHLT)1, havendo que ter em conta, no entanto, o componente histórico daquele registo. É, talvez, ainda cedo para daqui serem derivadas conclusões, uma vez que a partir da primeira década as curvas de sobrevivência parecem assumir um declive maior, como consequência de mortalidade resultante das complicações de aparecimento mais tardio, como a DVE e as neoplasias, bem como da deterioração progressiva da função renal.
A deterioração da função renal causada pela toxicidade medicamentosa é uma constante nestes doentes32,33. Os valores de creatinina pré‐operatória baixaram no primeiro mês após a transplantação, mas subiram progressivamente até ao final do primeiro ano, ultrapassando os valores iniciais. Na maior parte dos casos os valores tenderam a manter‐se relativamente estáveis nos primeiros cinco anos, mas a partir daí vários doentes tiveram uma deterioração significativa da função renal. Nesta experiência, três doentes foram já submetidos a transplantação renal e outros dois estão presentemente submetidos a terapêutica de substituição, aguardando transplantação.
ConclusãoO número de doentes à espera de transplante tem vindo a aumentar, ao contrário da oferta de dadores. Esta situação torna‐se mais complexa quando se constata um aumento no número de doentes cujo estado clínico se agravou fazendo‐os cair para graus de prioridade elevados (II‐V). Este panorama obriga, por um lado, a forçar as fronteiras da doação e, por outro, a ponderar de forma responsável e pragmática a escolha dos candidatos para transplantação.
De um modo geral, os doentes transplantados derivam grande benefício da transplantação cardíaca, tanto do ponto de vista da qualidade de vida como na da longevidade. Contudo, um número considerável de doentes sofre de complicações graves, algumas fatais, que obrigam a contínua monitorização e assistência. Esta é uma atividade intensa, de grande peso nas equipas transplantadoras, que requer, ainda, uma organização diferente da assistência noutras áreas médicas. Deste modo, e porque os resultados estão muito dependentes da experiência adquirida, a transplantação cardíaca, tal como outras, deveria ser reservada a centros com um nível razoável de atividade, sendo completamente desaconselhada a sua dispersão.
No nosso país, as necessidades nesta área estão atualmente razoavelmente satisfeitas, mas o número de centros é, provavelmente, excessivo para a população assistida, pelo que se recomenda uma reapreciação do problema, de modo a garantir a qualidade da assistência prestada aos doentes com insuficiência cardíaca terminal e refratária às terapêuticas convencionais e conservadoras. A atual situação de competição pelos dadores não serve os objetivos de uma distribuição mais adequada pelos doentes em espera nos vários centros transplantadores.
A diminuição do número de dadores que se tem vindo a verificar nos últimos anos pode vir a alterar a situação relativamente favorável que atingimos na última década após o início do nosso programa de transplantação. No entanto, algumas ações de sensibilização e de reorganização dos programas de identificação e captação de dadores podem já estar a surtir efeito. De facto, o ano de 2013 parece ter marcado um ponto de viragem em todas as áreas da transplantação. Só no nosso centro foram transplantados 30 doentes, um número que antes só havia sido atingido em 2005. No entanto, ainda temos um longo caminho a percorrer até se atingir um grau de aproveitamento máximo das potencialidades existentes.
Responsabilidades éticasProteção de pessoas e animaisOs autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dadosOs autores declaram ter seguido os protocolos do seu centro de trabalho acerca da publicação dos dados de pacientes.
Direito à privacidade e consentimento escritoOs autores declaram ter recebido consentimento escrito dos pacientes e/ ou sujeitos mencionados no artigo. O autor para correspondência deve estar na posse deste documento.
Conflito de interessesOs autores declaram não haver conflito de interesses.
Os autores reconhecem a importantíssima contribuição para estes resultados dos seguintes elementos do Gabinete de Coordenação e Colheitas Órgãos e Transplantação (GCCOT) do HUC no desenvolvimento deste Programa de Transplantação Cardíaca: Dra. Ana Maria Calvão da Silva (Diretora), Enf. Maria João Henriques e Enf. António Manuel Dias Alves. O GCCOT do HUC é o mais ativo do país graças à intensidade e a qualidade do seu trabalho.