O benefício do desfibrilhador implantável está bem demonstrado nos doentes com cardiopatia isquémica. No entanto, a evidência deste benefício é menos robusta em doentes com cardiopatia não isquémica. Pretendeu‐se determinar se os doentes com cardiopatia não isquémica apresentavam a mesma incidência de choque apropriado e mortalidade total, comparativamente àqueles com cardiopatia isquémica.
MétodosEstudo retrospetivo, em que foram analisados todos os doentes com cardioversor‐desfibrilhador implantável ou terapia de ressincronização cardíaca com desfibrilhador, implantados para prevenção primária, entre 2004 a 2014, num único centro. A população foi dividida em dois grupos: doentes com cardiopatia isquémica e doentes com cardiopatia não isquémica. O endpoint primário combinado foi choque apropriado e morte por qualquer causa.
ResultadosForam estudados 281 doentes, dos quais 187 (66%) apresentavam cardiopatia isquémica. Os doentes com cardiopatia isquémica eram mais velhos, mais frequentemente do género masculino e com maior prevalência de fatores de risco cardiovasculares. O follow‐up médio foi de 55±42 meses. Trinta e quatro doentes (18%) com cardiopatia isquémica e 20 doentes (21%) com cardiopatia não isquémica tiveram um choque apropriado (p=0,64). Oitenta e nove doentes (47%) com cardiopatia isquémica e 36 (38%) com cardiopatia não isquémica morreram durante o follow‐up (p=0,19). A curva de Kaplan‐Meier demonstra que a probabilidade de choque ou morte ao longo do tempo é semelhante nos dois grupos (logrank, p=0.14).
ConclusãoNa população estudada, não existiram diferenças na probabilidade de choque apropriado ou na mortalidade total nos doentes com cardiopatia não isquémica comparativamente aqueles com cardiopatia isquémica.
The benefits of implanted defibrillators in patients with ischemic heart disease (IHD) are well known. However, the evidence is less robust in patients with non‐ischemic heart disease (non‐IHD). We aimed to determine whether patients with non‐IHD have a similar incidence of appropriate shocks and all‐cause mortality compared to those with IHD.
MethodsIn a retrospective single‐center study we analyzed all patients with implantable cardioverter‐defibrillators or cardiac resynchronization therapy‐defibrillators implanted for primary prevention between 2004 and 2014. The population was divided into two groups: patients with IHD and patients with non‐IHD. The composite endpoint was appropriate shock and all‐cause mortality.
ResultsTwo hundred and eighty‐one patients were studied, of whom 187 (66%) had IHD. Patients with IHD were older, more frequently male and with more cardiovascular risk factors. Mean follow‐up was 55±42 months. Thirty‐four patients (18%) with IHD and 20 patients (21%) with non‐IHD had an appropriate shock (p=0.64). Eighty‐nine patients (47%) with IHD and 36 (38%) with non‐IHD died during follow‐up (p=0.19). The rate of shocks or death over time was similar in patients with IHD and non‐IHD according to Kaplan‐Meier survival curve analysis (log‐rank p=0.10).
ConclusionIn this population, there were no differences in appropriate shocks or all‐cause mortality in the two groups.
De acordo com as recomendações europeias publicadas em 2016, o cardioversor‐desfibrilhador implantável (CDI) está indicado para reduzir o risco de morte súbita cardíaca (MSC) e mortalidade nos doentes com insuficiência cardíaca (IC) sintomática e com fração de ejeção do ventrículo esquerdo (FEVE)≤35%, apesar da terapêutica médica otimizada (recomendação classe I)1. Dado que a evidência do benefício é superior nos doentes com cardiopatia isquémica (CI), o nível de recomendação é A (dados provenientes de múltiplos ensaios clínicos aleatorizados e meta‐análises2–4), enquanto na cardiopatia não isquémica (CNI), o nível de recomendação é B (dados provenientes de um único ensaio clínico não aleatorizado ou de estudos grandes não aleatorizados3–5). Os estudos em que se baseiam estas recomendações foram publicados há mais de uma década e, por esse motivo, as terapias médica e de ressincronização cardíaca (CRT) estavam aquém da realidade atual, tornando o benefício do desfibrilhador superior. Além disso, após a publicação destas recomendações, o estudo DANISH demonstrou que a utilização de CDI profilático nos doentes com CNI não reduziu a mortalidade total, apesar de reduzir o risco de MSC6. Como tal, o benefício do desfibrilhador nos doentes com CNI tem sido recentemente questionado7.
ObjetivoO objetivo do trabalho foi verificar se o benefício da terapêutica com desfibrilhador (CDI ou CRT com desfibrilhador (CRT‐D)), em prevenção primária, seria diferente nos doentes com CNI comparativamente aos doentes com CI, numa população do mundo real.
MétodosPopulaçãoForam estudados todos os doentes que implantaram CDI ou CRT‐D entre 2004 e 2014, para prevenção primária de MSC, num único centro.
Desenho do estudoTratou‐se de um estudo retrospetivo, unicêntrico e observacional.
A população foi dividida em dois grupos: doentes com CI e doentes com CNI.
Foram analisadas as caraterísticas basais (idade, género, índice de massa corporal (IMC)), sintomas (nomeadamente classe New York Heart Association (NYHA)), fatores de risco cardiovasculares e comorbilidades, avaliação ecocardiográfica (nomeadamente FE VE), dados laboratoriais (valor de creatinina e péptido natriurético tipo B [BNP]), medicação em curso e tipo de desfibrilhador implantado (CDI ou CRT‐D) nos dois grupos, no momento de implantação do dispositivo.
DefiniçõesConsiderou‐se como CI a disfunção sistólica ventricular esquerda (FE VE≤35%) na presença de no mínimo 75% de estenose no tronco comum ou na descendente anterior proximal ou em dois ou mais vasos epicárdicos ou caso existisse história de enfarte agudo do miocárdio (EAM) ou revascularização prévia. Na ausência destes critérios, foi assumida CNI.
A hipertensão arterial (HTA) foi considerada sempre que o doente tivesse uma pressão arterial sistólica ou diastólica em repouso ≥140/90mmHg em duas ocasiões ou quando se encontrava medicado com anti‐hipertensores. A diabetes mellitus foi definida como uma glicose em jejum≥126mg/dL ou quando presente a prescrição de medicação anti‐diabética. O tabagismo foi classificado como fumador atual ou não fumador. A classe de NYHA foi classificada de acordo com o médico assistente na altura de implantação do dispositivo. Os diagnósticos de fibrilhação auricular (FA), doença pulmonar obstrutiva crónica (DPOC), síndrome de apneia obstrutiva do sono (SAOS), acidente vascular cerebral (AVC), acidente isquémico transitório (AIT) e doença arterial periférica (DAP) foram assumidos sempre que o médico assistente assim o tivesse considerado. Os ecocardiogramas transtorácicos foram retrospetivamente revistos e reavaliados pelos investigadores e foi calculada a FEVE pelo método biplano de Simpson modificado.
SeguimentoTodos os registos da consulta de seguimento de CDI/CRT‐D, bem como da monitorização remota (sempre que disponível) foram avaliados, para colheita de dados quanto aos eventos relacionados com o desfibrilhador. O choque foi considerado apropriado sempre que o investigador assim o considerasse, tendo em conta a análise do eletrograma intracavitário e de choque. Foram ainda analisados todos os registos médicos relativos a consultas, internamentos hospitalares ou vindas ao Serviço de Urgência e confirmados registos relativos ao óbito.
OutcomesO endpoint primário combinado foi choque apropriado e mortalidade total. Os endpoints secundários foram, separadamente, choque apropriado e mortalidade total. Foram avaliados os preditores independentemente associados a cada um dos endpoints secundários, bem como classificadas as causas de morte. O perfil de segurança de implantação do dispositivo foi também analisado, tendo em conta as infeções associadas ao dispositivo e o choque inapropriado. Foi realizada a análise de subgrupos de doentes mais velhos, definidos com tendo idade maior ou igual a 68 anos (o cut‐off usado no estudo DANISH6), e de doentes com CRT‐D versus CDI.
Análise estatísticaA análise estastística foi realizada através do SPSS versão 23 (SPSS Inc., Chicago, Illinois). Os dados foram expressos como média±desvio‐padrão nas variáveis contínuas e como frequência e percentagem nas variáveis categóricas. As características basais foram comparadas usando o teste do Qui‐quadrado no caso de variáveis categóricas e o teste t de Student no caso de variáveis contínuas. A curva de sobrevida de Kaplan‐Meier e o teste de log‐rank foram usadas para comparar os outcomes entre os dois grupos estudados. O modelo de regressão de Cox multivariado foi usado para calcular o hazard ratio (HR) e os intervalos de confiança (IC) a 95% para choque apropriado e morte total. Um valor p <0,05 foi considerado estatisticamente significativo.
ResultadosForam estudados 281 doentes, dos quais 187 (66%) apresentavam CI. As características da população no momento de implantação de CDI ou CRT‐D estão representadas na Tabela 1. Os doentes com CI eram mais velhos, mais frequentemente do género masculino e com mais fatores de risco cardiovasculares (CV) e doença arterial. No entanto, não se verificaram diferenças significativas entre os dois grupos quanto à classe NYHA, valor de creatinina e BNP, FE VE e presença de FA. Os doentes com CNI implantaram mais frequentemente um CRT‐D, enquanto a maioria daqueles com CI implantaram um CDI.
Características dos doentes no momento de implantação do desfibrilhador
| Cardiopatia isquémican= 187 | Cardiopatia não isquémican= 94 | Valor‐p | |
|---|---|---|---|
| Idade (anos) | 65 ± 9 | 62 ± 12 | 0,02 |
| Género masculino (%) | 167 (89) | 63 (67) | <0,0001 |
| IMC (Kg/m2) | 26,9 ± 4,1 | 27,7 ± 4,3 | 0,14 |
| Sintomas | |||
| NHYA classe II | 101 (54) | 52 (55) | 0,97 |
| NHYA classe III | 81 (43) | 38 (40) | 0,72 |
| Dados laboratoriais | |||
| BNP | 739 ± 1651 | 758 ± 1328 | 0,92 |
| Creatinina (mg/dL) | 1,4 ± 0,9 | 1,2 ± 0,5 | 0,20 |
| Achados ecocardiográficos | |||
| FE VE (%) | 27,3 ± 6,9 | 26,9 ± 6,7 | 0,61 |
| Fatores de risco cardiovasculares | |||
| HTA (%) | 140 (75) | 43 (46) | <0,0001 |
| DM (%) | 97 (52) | 33 (35) | 0,01 |
| Dislipidémia (%) | 142 (76) | 42 (45) | <0,0001 |
| Tabaco (%) | 93 (50) | 15 (16) | <0,0001 |
| FA (%) | 85 (45) | 47 (50) | 0,55 |
| Comorbilidades | |||
| DPOC (%) | 22 (12) | 6 (6) | 0,17 |
| SAOS (%) | 14 (8) | 12(13) | 0,22 |
| AVC/AIT (%) | 28 (15) | 5 (5) | 0,03 |
| DAP (%) | 14 (8) | 0 (0) | 0,01 |
| Tipo de desfibrilhador | |||
| CDI | 108 (58) | 32 (34) | 0,03 |
| CRT‐D | 79 (42) | 62 (66) | 0,01 |
| Medicação | |||
| iECA/ARAII (%) | 175 (94) | 91 (97) | 0,42 |
| Beta‐bloqueante (%) | 158 (85) | 84 (89) | 0,40 |
| Espironolactona (%) | 71 (38) | 32 (34) | 0,59 |
| Furosemida (dose) | 37 ± 29 | 37 ± 25 | 0,97 |
| Anti‐arrítmicos a (%) | 43 (23) | 26 (28) | 0,44 |
| ACO (%) | 95 (51) | 54 (57) | 0,36 |
ACO: anticoagulação oral. AIT: acidente isquémico transitório. ARAII: antagonistas do recetor da angiotensina II. AVC: acidente vascular cerebral. BNP: péptido natriurético tipo B. CDI: cardioversor‐desfibrilhador implantável. DAP: Doença arterial periférica. DM: Diabetes mellitus. DPOC: doença pulmonar obstrutiva crónica. IMC: índice de massa corporal. iECA: inibidores da enzima de conversão da angiotensina. FA: fibrilhação auricular. FE VE: fração de ejeção do ventriculo esquerdo. HTA: hipertensão arterial. NYHA: classe funcional da NewYork Heart Association. SAOS: sindrome apneia obstrutiva do sono. CRT‐D: Terapia de ressincronização cardíaca com desfibrilhador.
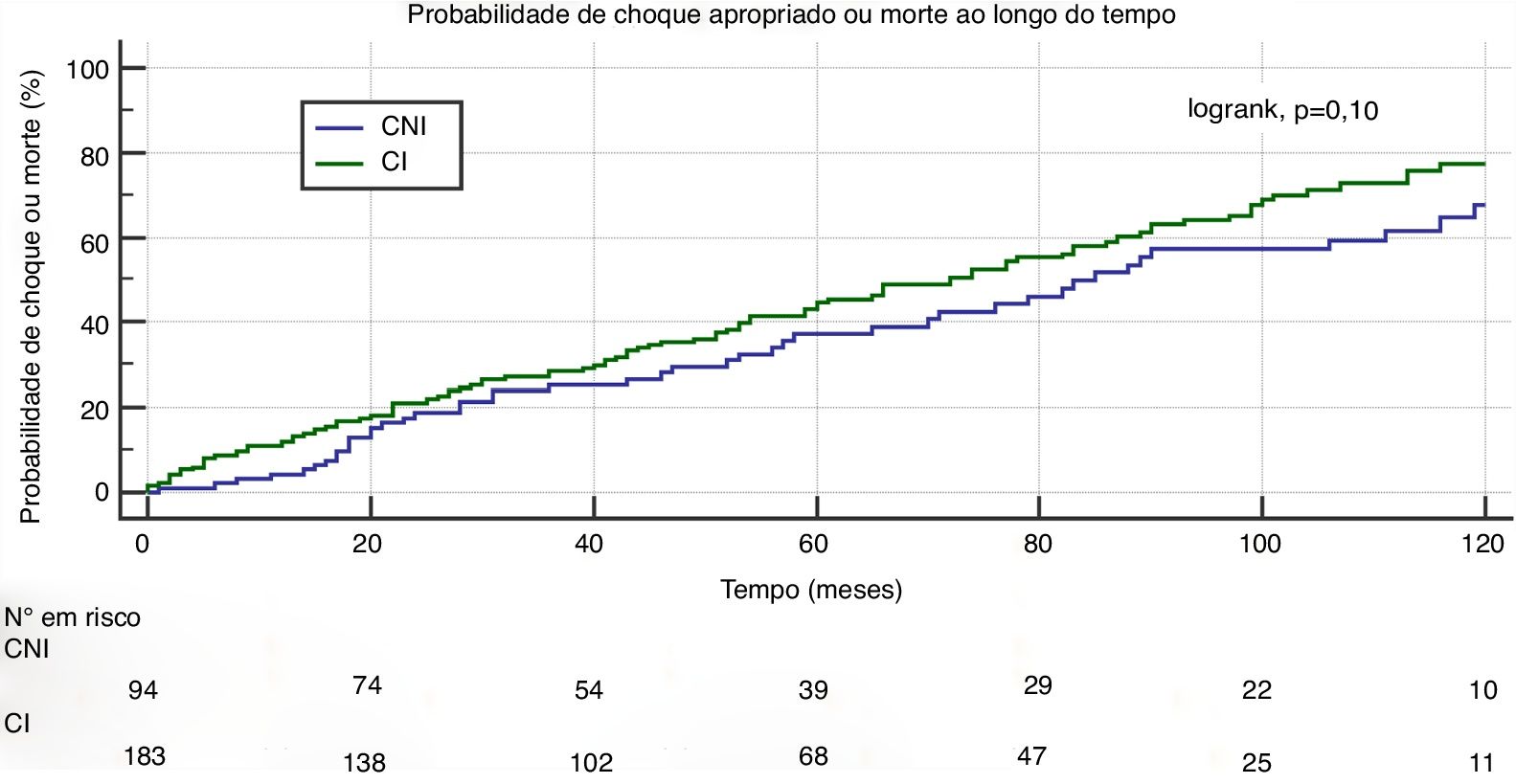
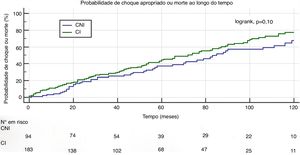
Durante um follow‐up médio de 55±42 meses, o endpoint combinado (choque apropriado e mortalidade total) ocorreu em 150 doentes (53%): no grupo com CI em 105 doentes (56%) e no grupo com CNI em 45 (46%) (p=0.15). A curva de Kaplan‐Meier, representada na Figura 1, demonstra que a probabilidade de choque apropriado ou morte ao longo do tempo foi semelhante nos dois grupos estudados (logrank, p=0.10).
Endpoints secundáriosVinte doentes (21%) com CNI e 34 doentes (18%) com CI tiveram um choque apropriado (p=0,64) durante o período de follow‐up. A taxa de incidência de choque apropriado foi de 3,75 choques por 100 pessoas‐ano no grupo com CNI e de 3,08 choques por 100 pessoas‐ano no grupo com CI (p=0,19).
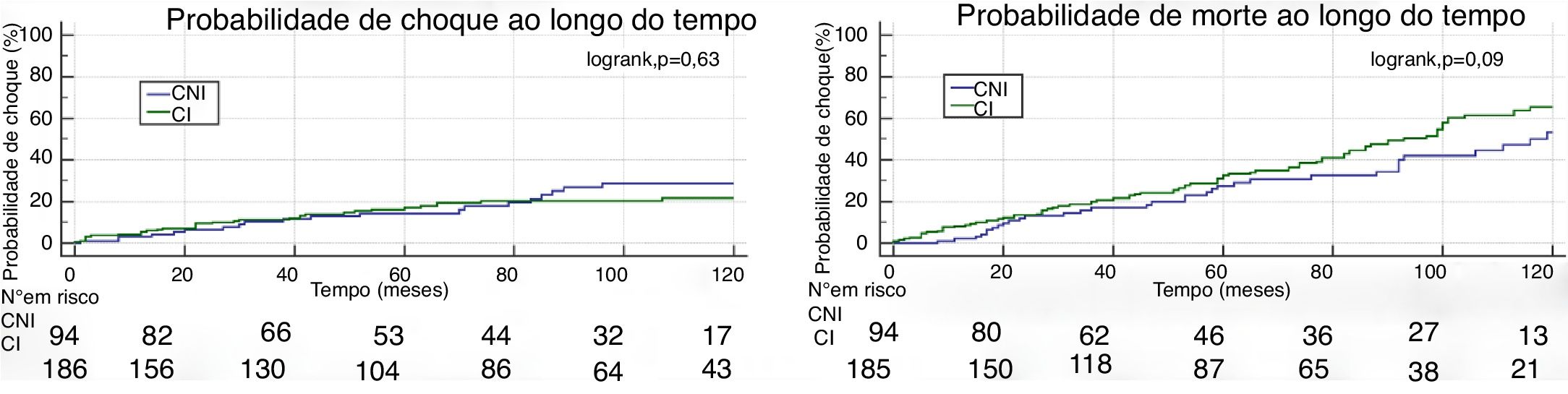
Nos doentes com choque apropriado, o tempo médio para a ocorrência do primeiro choque foi de 3,5±2,7 anos no grupo com CNI e de 2,9±2,3 anos no grupo com CI (p=0,07). A curva de Kaplan‐Meier para a ocorrência de choque apropriado nos dois grupos estudados encontra‐se representada na Figura 2A, demonstrando que probabilidade de choque apropriado foi também semelhante nos dois grupos estudados (logrank, p=0,63).
A análise por regressão multivariada mostrou que a FEVE (HR 1,02, IC 1,01–1,04, p =0,001 ‐ por cada aumento percentual da FE VE) e a idade (HR 0,97, IC 0,95‐0,99, p=0,04 ‐ por cada ano) estão independentemente associados ao choque apropriado.
Trinta de seis doentes (38%) com CNI e 89 doentes (47%) com CI morreram durante o follow‐up (p=0,19). A taxa de mortalidade foi de 7,5 mortes por 100 pessoas‐ano no grupo com CNI e de 9,0 mortes por 100 pessoas‐ano no grupo com CI (p=0,11).
O tempo médio para a morte foi de 3,9±2,8 anos no grupo com CNI e de 4,1±3,1 anos no grupo com CI (p=0,67). A probabilidade de mortalidade total ao longo do tempo foi semelhante nos dois grupos (logrank, p=0,09) (Figura 2B).
Estiveram independentemente associados a um maior risco de morte: aumento da creatinina, idade, classe NYHA e maior dose de furosemida no momento de implantação do dispositivo. O uso de beta‐bloquentes actuou como factor portector para a mortalidade (Tabela 2).
Análise de regressão multivariada para a mortalidade total
| HR | IC 95% | Valor‐p | |
|---|---|---|---|
| Creatinina (mg/dL) | 1,42 | 1,19‐1,69 | 0,0001 |
| Idade (anos) | 1,03 | 1,01 – 1,05 | 0,002 |
| Classe NYHA | 1,37 | 1,01 – 1,86 | 0,04 |
| Furosemida (mg) | 1,01 | 1,01‐1,02 | 0,004 |
| Uso de beta‐bloqueante | 0,61 | 0,39 – 0,97 | 0,04 |
HR: Hazard ratio. IC: interval de confiança. mg: miligramas. mg/dL: miligramas por decilitro.
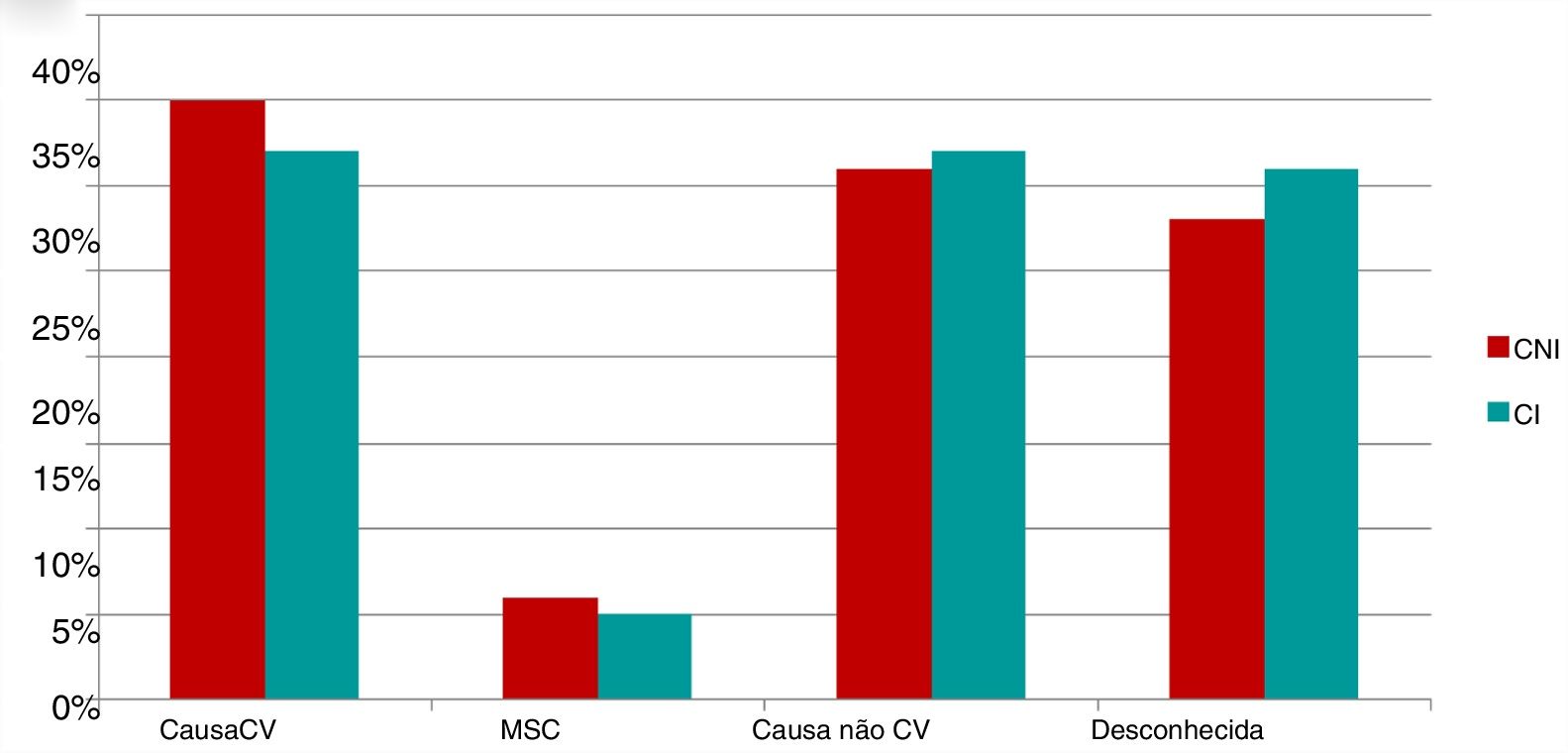
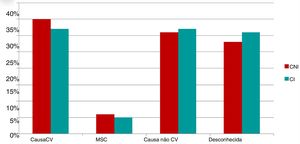
Nos 88 doentes em que foi possivel apurar a causa de morte (70% dos óbitos), 42 doentes morreram de causa CV, 7 com MSC e 39 doentes morreram de causa não‐cardiovascular. As causas de morte foram semelhantes nos dois grupos estudados (Figura 3).
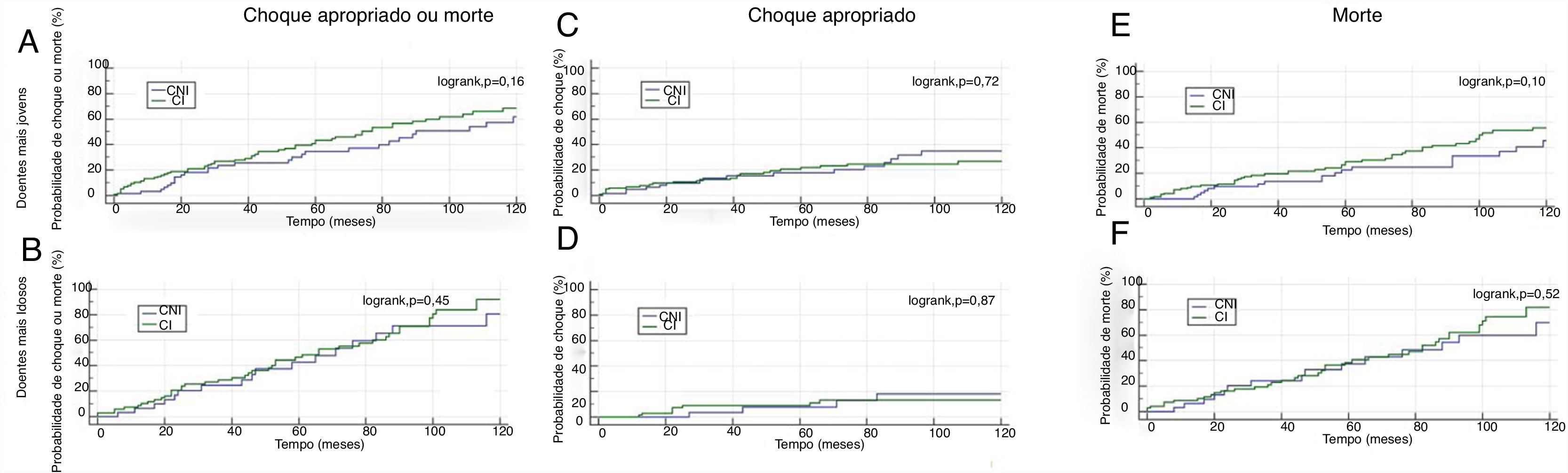
Análise de subgruposNo subgrupo de doentes com menos de 68 anos (n=181), verificou‐se uma maior probabilidade de choque apropriado (Figura 4C e 4D). No entanto, não se verificaram diferenças estatisticamente significativas entre os grupos com CI e CNI nos doentes mais idosos (≥68 anos) ou mais jovens (<68 anos) (Figura 4).
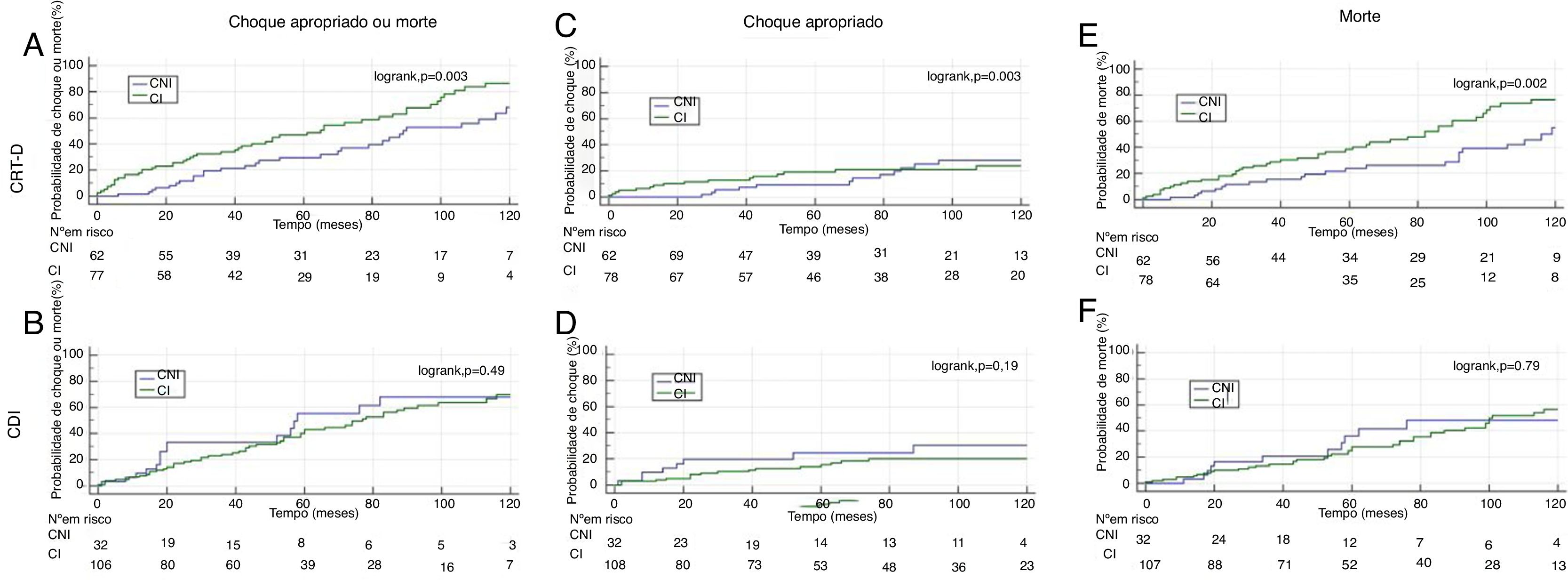
A subanálise de acordo com o tipo de desfibrilhador implantado mostra que nos doentes com CRT‐D, houve maior redução no endpoint combinado de choque apropriado e morte, bem como no endpoint secundário de mortalidade total, no grupo com CNI, o que foi evidente desde o início do follow‐up (logrank, p=0,003 e p=0,002, respetivamente) (Figura 5A e 5E).
Curvas de Kaplan‐Meier para os endpoints primário e secundários de acordo com tipo de desfibrilhador implantado (CRT‐D ou CDI)
CI: cardiopatia isquémica. CNI: cardiopatia não isquémica.
CDI: cardioversor‐desfibrilhador implantado. CRT‐D: terapia de ressincronização cardíaca com desfibrilhador.
As infecções de dispositivo ocorreram em seis doentes (1,6%), três em doentes com CI e três em doentes com CNI. Das seis infecções, quatro ocorreram em doentes que implantaram CRT‐D e duas em doentes que implantaram CDI (um de câmara única e um de câmara dupla).
Os choques inapropriados ocorreram em 16 doentes (9%) durante o follow‐up. Em nove doentes (56%) por episódios de fibrilhação auricular ou flutter auricular. Os restantes, foram devidos a outra taquicárdia supra‐ventricular (n=2); taquicárdia sinusal (n=1), fratura do eléctrodo (n=2), oversensing da onda T (n=1) e interferência externa (n=1).
DiscussãoPermanece ainda alguma controvérsia quanto ao benefício da implantação de desfibrilhador nos doentes com CNI. Os estudos clínicos que mostraram benefício na implantação de desfibrilhador (SCD‐HeFT4 e o COMPANION8) incluíram também doentes com CI e o efeito estudado baseou‐se na subanálise dos doentes com CNI. Os estudos que não demonstraram benefício do desfibrilhador na redução da mortalidade total envolveram exclusivamente doentes com CNI (DEFINITE5, CAT9, AMIOVIRT10 e, mais recentemente DANISH6). A diferença temporal destes estudos influenciou claramente a restante terapêutica para a IC, nomeadamente quando à proporção de doentes medicados com antagonistas da aldosterona e CRT, o que teve seguramente efeito na sua sobrevida. O estudo DANISH, publicado há cerca de um ano, não demonstrou benefício da implantação de desfibrilador na redução de mortalidade total (endpoint primário do estudo), apesar de ter havido redução na mortalidade de causa arrítmica. Porém, no subgrupo de doentes mais jovens (<68 anos) mostrou diminuir a mortalidade total (HR 0,64; IC 95% 0,45‐0,90, p=0,01).
Na tentativa de responder a esta questão, foi recentemente publicada uma meta‐análise11, que incluiu o estudo DANISH, além do CAT, DEFINITE e SCD‐HeFT. Segundo os autores, o CDI implantado como prevenção primária foi eficaz a reduzir a mortalidade total nos doentes com CNI, o que suporta as actuais recomendações.
Haugaa e colaboradores (2017)12 estudaram o impacto do estudo DANISH na prática clínica europeia e concluiram que a maioria dos centros estudados não implanta CDI para prevenção primária por rotina em doentes com CNI, apesar das recomendações. Pelo contrário, nos doentes com CI, as recomendações para prevenção primária são cumpridas e não se verificam alterações recentes na prática clínica actual. De salientar que a maior parte dos centros admitiu ter mudado as indicações para a implantação de desfibrilhador na CNI após a publicação do estudo DANISH. Assim, verifica‐se que um único estudo foi capaz de alterar rapidamente a atitude dos clínicos de forma generalizada.
Os nossos resultados sugerem que a implantação de um desfibrilhador tem um benefício semelhante nos doentes com CNI e naqueles com CI, no que diz respeito à incidência de choque apropriado e à mortalidade total, que foram semelhantes nos dois grupos. Este benefício, ao contrário do que se verificou no estudo DANISH, foi igualmente observado nos doentes mais velhos, nos quais também não se verificaram diferenças nos endpoints estudados.
A probabilidade de choque apropriado foi praticamente sobreponível nos doentes com CNI e com CI, o que demonstra que os doentes com CNI têm um risco semelhante de apresentar eventos arrítmicos fatais ou potencialmente fatais.
Comparativamente ao estudo DANISH6, a incidência de choque apropriado nos doentes com CNI foi superior (21% no nosso estudo, comparativamente a 12% no estudo DANISH). Tal facto deve‐se muito provavelmente à programação das zonas de terapêutica/choque nos primeiros anos de seguimento, pois, como se sabe, a programação das zonas de terapêutica com choque era mais agressiva antigamente. No entanto, a programação foi idêntica nos dois grupos.
Os nossos resultados mostram ainda que o tempo para o primeiro choque apropriado é superior nos doentes com CNI (3,5±2,7 anos versus 2,9±2,3 anos no grupo com CI), o que já foi demonstrado em estudos prévios8, salientando a necessidade de que os fatores que contribuem para a morte não súbita não sejam demasiado elevados, para que o risco de morte não seja superior ao de choque apropriado.
Quanto à mortalidade total, não existiram igualmente diferenças nos dois grupos estudados, exceptuando na análise do subgrupo de doentes com CRT‐D, nos quais aqueles com CNI tiveram menor mortalidade. Tem sido demonstrado que os doentes com CNI têm uma taxa de resposta ao CRT‐D superior aos doentes com CI, provavelmente por diferenças no substrato miocárdico13. Assim, a menor mortalidade demonstrada nos doentes com CRT‐D e CNI (que não se verifica naqueles com CDI e CNI) pode ser explicada pela melhor resposta ao CRT‐D e consequente impacto na sobrevida. Este é, aliás, um dos motivos que tem sido apontado como responsável pela baixa mortalidade nos doentes incluídos no estudo DANISH, no qual cerca de 60% dos doentes em cada braço implantou CRT9,10.
Quanto às causas de morte, verificamos que, apesar da elevada proporção de morte de causa desconhecida, a MSC foi responsável por cerca de 5% das mortes, o que comprova o benefício do desfibrilhador a diminuir a morte súbita arrítmica.
Apesar de se tratar de um estudo observacional, retrospectivo e unicêntrico, este trabalho espelha a realidade dos últimos anos quanto à utilidade do desfibrilhador na vida real. Dada a impossibilidade ética de comparar grupos com e sem desfibrilhador nos tempos atuais (pela privação de uma terapêutica que demonstrou eficácia em ensaios clínicos aleatorizados e meta‐análises), este estudo comparou doentes com CI (nos quais está demonstrado de forma robusta o benefício do desfibrilhador) com aqueles com CNI (nos quais permanece alguma controvérsia). Existem algumas limitações inerentes ao estudo, nomeadamente na programação das zonas de terapia do desfibrilhador (numa fase inicial tendencialmente mais agressivas e por isso potencialmente evitáveis); ausência de informação quanto à causa de morte de todos os doentes; ausência de seguimento quanto à terapêutica médica ao longo do tempo de follow‐up e número relativamente reduzido de doentes.
ConclusõesNa população estudada, não existiram diferenças na probabilidade de choque apropriado ou mortalidade total nos doentes com CNI, comparativamente aqueles com CI. Assim, parece existir benefício na implantação de desfibrilhador (CDI ou CRT‐D) em ambos os grupos estudados.
Conflito de interessesOs autores declaram não haver conflito de interesses.